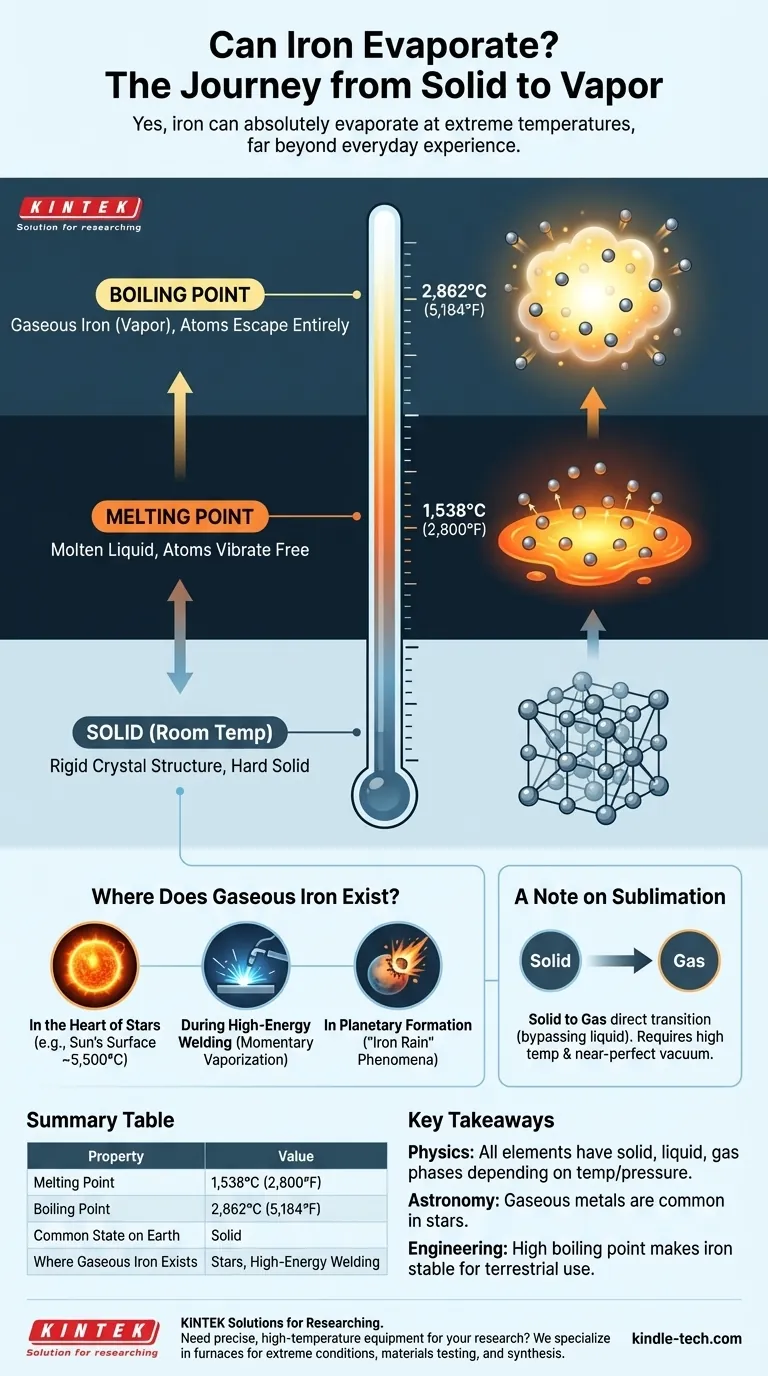
Oui, le fer peut absolument s'évaporer. Comme pratiquement toute matière, le fer peut exister sous forme solide, liquide et gazeuse. Cependant, les conditions requises pour transformer le fer solide en gaz, ou vapeur, impliquent des températures si extrêmes qu'elles sont bien au-delà de l'expérience humaine quotidienne.
Le principe fondamental est que tout élément passera à l'état gazeux s'il est chauffé jusqu'à son point d'ébullition. Pour le fer, cette température est incroyablement élevée, atteignant 2 862 °C (5 184 °F), c'est pourquoi nous le percevons comme un matériau en permanence solide dans toutes les conditions normales.

Comprendre le parcours vers la vapeur de fer
Pour comprendre comment le fer s'évapore, il est préférable de penser au même processus que l'eau subit, mais à une échelle de température beaucoup plus élevée. L'état de toute matière – solide, liquide ou gazeux – est déterminé par l'énergie et le mouvement de ses atomes.
Première étape : du solide au liquide
Avant que le fer ne puisse bouillir, il doit d'abord fondre. À température ambiante, les atomes de fer sont enfermés dans une structure cristalline rigide, ce qui en fait un solide dur.
Lorsque vous ajoutez une chaleur immense, les atomes vibrent de plus en plus violemment jusqu'à ce qu'ils se libèrent de cette structure. Cela se produit au point de fusion du fer de 1 538 °C (2 800 °F), le transformant en un liquide en fusion.
Deuxième étape : du liquide au gaz
Pour s'évaporer, ou bouillir, les atomes de fer ont besoin d'encore plus d'énergie pour surmonter complètement les forces qui les maintiennent ensemble en tant que liquide.
Lorsque la température atteint le point d'ébullition du fer de 2 862 °C (5 184 °F), les atomes s'échappent entièrement, formant un nuage surchauffé d'atomes de fer individuels. C'est de la vapeur de fer, ou du fer gazeux.
Où existe réellement le fer gazeux ?
Bien que vous ne verrez jamais une flaque de fer s'évaporer par une chaude journée, ce processus est courant dans certains environnements extrêmes de l'univers et dans des applications industrielles spécialisées.
Au cœur des étoiles
L'endroit le plus courant pour trouver du fer gazeux est à l'intérieur des étoiles, y compris notre Soleil. La surface du Soleil est d'environ 5 500 °C (9 940 °F), bien au-dessus du point d'ébullition du fer. Ici, le fer existe en tant que composant du plasma solaire.
Pendant le soudage à haute énergie
À une échelle beaucoup plus petite et plus contrôlée, la chaleur intense d'un arc de soudage industriel peut momentanément vaporiser une infime quantité du métal en cours de soudage. Cette vapeur de fer refroidit et se resolidifie immédiatement pour faire partie de la soudure.
Dans la formation planétaire
Lors de la formation de notre système solaire, les impacts massifs entre les corps célestes auraient généré suffisamment d'énergie pour vaporiser la roche et le fer. Cela aurait pu conduire à des phénomènes tels que la "pluie de fer" sur les protoplanètes à mesure que la vapeur refroidissait et se condensait.
Une note sur la sublimation
Il existe une autre voie vers l'état gazeux appelée sublimation, où un matériau passe directement de l'état solide à l'état gazeux, contournant complètement la phase liquide. C'est ce que fait la glace sèche (dioxyde de carbone solide) à température ambiante.
Théoriquement, le fer peut aussi se sublimer. Cependant, cela nécessiterait une combinaison de très hautes températures et d'une pression extrêmement basse (un vide quasi parfait). Sous une pression atmosphérique normale, le taux de sublimation du fer est pratiquement nul.
Points clés à retenir pour comprendre la matière
- Si votre objectif principal est la physique fondamentale : Rappelez-vous que tous les éléments peuvent exister en phases solide, liquide et gazeuse ; il ne s'agit que d'atteindre la bonne température et la bonne pression.
- Si vous êtes intéressé par l'astronomie : Reconnaissez que les métaux gazeux, y compris le fer, sont un composant courant et important des étoiles et jouent un rôle clé dans les événements cosmiques.
- Si vous pensez à l'ingénierie : Appréciez que le point d'ébullition incroyablement élevé du fer est la propriété fondamentale qui en fait un matériau stable et fiable pour presque toutes les applications terrestres.
En fin de compte, savoir que même quelque chose d'aussi solide que le fer peut être transformé en gaz renforce les lois physiques universelles qui régissent toute matière.
Tableau récapitulatif :
| Propriété | Valeur |
|---|---|
| Point de fusion | 1 538 °C (2 800 °F) |
| Point d'ébullition | 2 862 °C (5 184 °F) |
| État courant sur Terre | Solide |
| Où le fer gazeux existe | Étoiles, soudage à haute énergie |
Besoin d'équipements de haute précision et haute température pour vos recherches ou processus industriels ? KINTEK est spécialisé dans les équipements et consommables de laboratoire, y compris les fours capables de supporter des conditions extrêmes pour les tests et la synthèse de matériaux. Que vous étudiiez les transitions de phase ou développiez de nouveaux alliages, nos solutions fiables vous aident à obtenir des résultats précis et reproductibles. Contactez nos experts dès aujourd'hui pour discuter de la manière dont nous pouvons répondre aux besoins de haute température de votre laboratoire !
Guide Visuel