En bref, la validation d'autoclave est effectuée en utilisant une combinaison de trois méthodes distinctes : les moniteurs physiques, les indicateurs chimiques et les indicateurs biologiques. Ces méthodes sont utilisées ensemble dans un processus structuré pour fournir une confirmation complète et fiable que l'autoclave atteint le niveau de stérilité requis.
La validation d'autoclave n'est pas une action unique, mais un processus formel et documenté qui prouve que l'équipement stérilise constamment son contenu dans des conditions réelles. Elle va au-delà de la simple utilisation de la machine pour fournir des preuves objectives qu'un niveau d'assurance de stérilité (NAS) défini a été atteint.

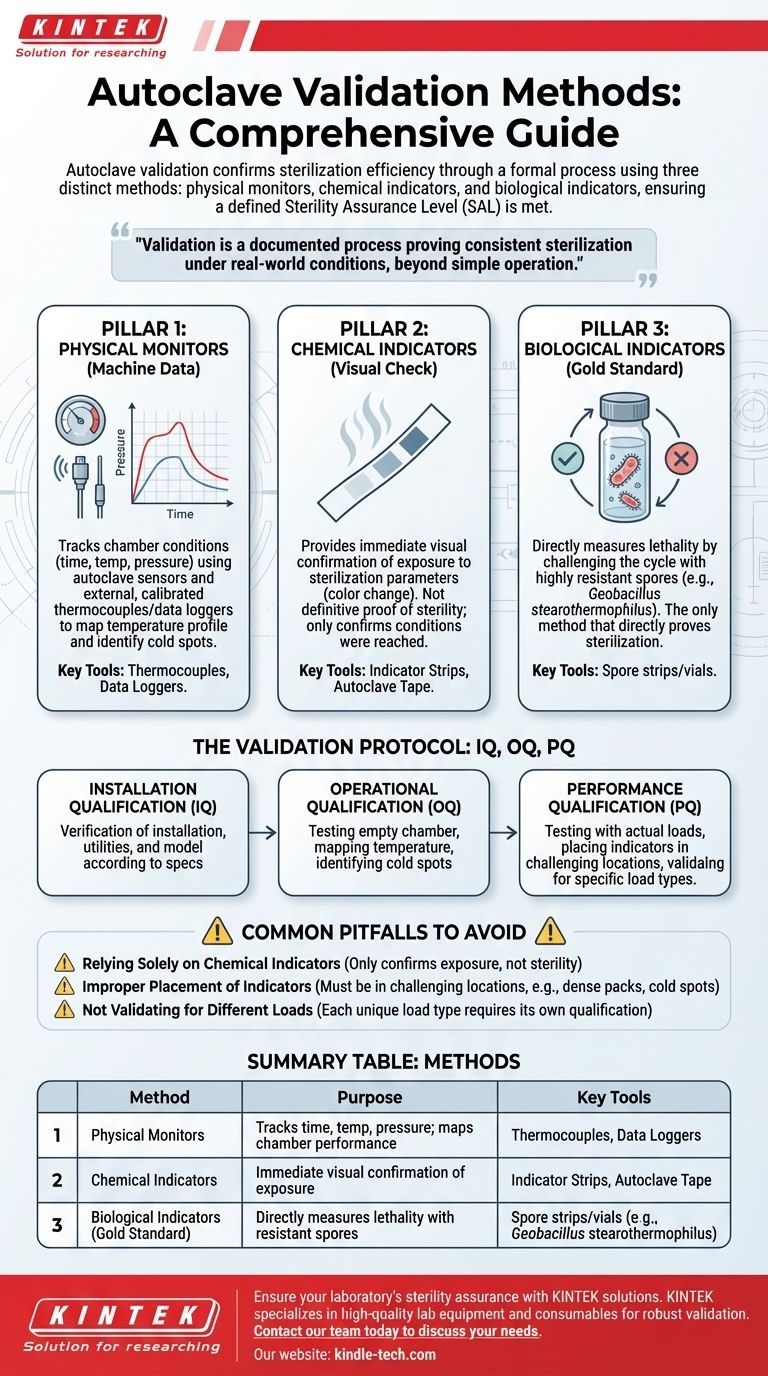
Les trois piliers de la validation d'autoclave
Une véritable validation repose sur une approche multifacette. Chaque méthode apporte une pièce différente du puzzle, et ce n'est que lorsqu'elles sont utilisées ensemble qu'elles offrent une image complète des performances de l'autoclave.
Pilier 1 : Moniteurs physiques (les données de la machine)
Les moniteurs physiques sont les capteurs et les enregistreurs de données qui suivent les conditions physiques à l'intérieur de la chambre de l'autoclave pendant un cycle.
Ceux-ci incluent les sondes de température, les capteurs de pression et les minuteries propres à l'autoclave. Pour une validation formelle, des thermocouples et des enregistreurs de données externes et calibrés sont placés dans toute la chambre pour cartographier son profil de température et identifier les "points froids".
Cette méthode fournit un enregistrement précis et horodaté des paramètres physiques du cycle, confirmant si la température et la pression cibles ont été atteintes et maintenues pendant la durée requise.
Pilier 2 : Indicateurs chimiques (le contrôle visuel)
Les indicateurs chimiques sont des matériaux qui subissent un changement visible, généralement de couleur, lorsqu'ils sont exposés à un ou plusieurs paramètres de stérilisation spécifiques comme la température ou la vapeur.
Ceux-ci sont le plus souvent vus sous forme de bandelettes ou de rubans indicateurs. Ils fournissent une confirmation visuelle rapide que les articles à l'intérieur de l'autoclave ont été exposés au processus de stérilisation.
Cependant, ils ne constituent pas une preuve définitive de stérilité. Un indicateur chimique qui change de couleur ne confirme que l'atteinte d'une certaine température, et non qu'elle a été maintenue suffisamment longtemps ou que la vapeur a pénétré efficacement la charge pour tuer les micro-organismes.
Pilier 3 : Indicateurs biologiques (la référence absolue)
Les indicateurs biologiques (IB) sont l'outil le plus critique pour la validation car ils mesurent directement la létalité du processus de stérilisation.
Les IB sont constitués d'une population standardisée de spores bactériennes hautement résistantes, le plus souvent Geobacillus stearothermophilus. Ces spores sont connues pour être beaucoup plus difficiles à tuer que les micro-organismes courants trouvés dans un laboratoire.
Après un cycle, l'IB est incubé. Si aucune croissance ne se produit, cela procure un degré élevé de confiance que toutes les autres charges biologiques potentielles dans la charge ont été détruites avec succès. C'est la seule méthode qui prouve directement que la stérilisation a été réalisée.
Assemblage : Le protocole de validation
Ces trois piliers sont intégrés dans un processus de qualification formel, le plus souvent divisé en trois phases connues sous le nom d'IQ, OQ et PQ.
Qualification d'installation (QI)
Il s'agit de la vérification documentée initiale. Elle vérifie que l'autoclave est le bon modèle, qu'il a été installé correctement conformément aux spécifications du fabricant et que tous les services publics nécessaires (électricité, eau) sont correctement connectés.
Qualification opérationnelle (QO)
En QO, l'autoclave est testé pour confirmer qu'il fonctionne correctement à vide. Cette phase implique la cartographie de la température de la chambre avec plusieurs thermocouples pour assurer une distribution uniforme de la chaleur et pour identifier les endroits les plus froids à l'intérieur de la chambre.
Qualification de performance (QP)
C'est la phase la plus cruciale. L'autoclave est testé avec des charges réelles qui représentent les matériaux que vous stériliserez quotidiennement (par exemple, liquides, instruments, sacs de déchets).
Pendant la QP, des indicateurs chimiques et biologiques sont placés stratégiquement dans toute la charge, avec un accent particulier sur les "points froids" identifiés pendant la QO. Des essais de QP réussis démontrent que l'autoclave peut stériliser efficacement son contenu prévu dans des conditions réelles.
Pièges courants à éviter
Une validation fiable implique d'être conscient des erreurs courantes qui peuvent conduire à un faux sentiment de sécurité.
Se fier uniquement aux indicateurs chimiques
L'erreur la plus fréquente est de supposer qu'un changement de couleur sur un ruban indicateur équivaut à la stérilité. Ce n'est pas le cas. Les indicateurs chimiques ne confirment que l'exposition à la chaleur et doivent être utilisés pour la surveillance de routine, et non comme seule base de validation.
Placement incorrect des indicateurs
Placer les IB dans une zone facilement accessible et ouverte de la chambre n'est pas un test valide. Ils doivent être placés dans les endroits les plus difficiles d'accès pour la vapeur : à l'intérieur de paquets denses, dans des récipients de liquide ou dans les points froids identifiés.
Ne pas valider pour différentes charges
Un cycle de stérilisation qui fonctionne pour un plateau de verrerie peut échouer pour un grand flacon de milieu liquide. Chaque type et configuration de charge unique nécessite sa propre qualification de performance pour s'assurer qu'elle peut être stérilisée de manière fiable.
Faire le bon choix pour votre objectif
Votre approche de la validation doit correspondre à vos besoins opérationnels spécifiques et à vos exigences réglementaires.
- Si votre objectif principal est la vérification opérationnelle de routine : Utilisez un indicateur chimique dans chaque charge pour une confirmation visuelle immédiate, et effectuez un test avec un indicateur biologique à une fréquence définie (par exemple, hebdomadaire ou mensuelle) pour vérifier les performances continues.
- Si votre objectif principal est la qualification initiale ou la validation après réparation : Vous devez mener un protocole complet d'IQ, OQ et PQ en utilisant des thermocouples externes et des indicateurs biologiques placés stratégiquement pour documenter formellement la capacité de la machine.
- Si votre objectif principal est la conformité GxP ou réglementaire : Documentez méticuleusement tous les résultats d'IQ, OQ et PQ pour chaque type de charge, établissez un calendrier de requalification récurrent et disposez d'un protocole clair pour enquêter sur toute défaillance d'IB.
En fin de compte, une validation robuste est le fondement de la confiance, garantissant que chaque cycle assure la stérilité dont votre travail dépend.
Tableau récapitulatif :
| Méthode | Objectif | Outils clés |
|---|---|---|
| Moniteurs physiques | Suit le temps, la température et la pression ; cartographie les performances de la chambre. | Thermocouples, Enregistreurs de données |
| Indicateurs chimiques | Fournit une confirmation visuelle immédiate de l'exposition à la chaleur/vapeur. | Bandelettes indicatrices, Ruban d'autoclave |
| Indicateurs biologiques (Référence absolue) | Mesure directement la létalité en défiant le cycle avec des spores résistantes. | Bandelettes/flacons de spores (par exemple, Geobacillus stearothermophilus) |
Assurez la stérilité de votre laboratoire avec les solutions KINTEK.
Une validation correcte de l'autoclave est essentielle pour l'intégrité de votre recherche, de vos diagnostics et de votre production. KINTEK est spécialisé dans la fourniture d'équipements de laboratoire et de consommables de haute qualité – des autoclaves fiables aux indicateurs biologiques certifiés – dont dépendent vos protocoles de validation.
Laissez nos experts vous aider à élaborer un programme de validation et de surveillance robuste, adapté à vos besoins spécifiques et à vos exigences de conformité.
Contactez notre équipe dès aujourd'hui pour discuter de vos besoins en matière de validation d'autoclave et d'assurance de stérilité.
Guide Visuel
Produits associés
- Autoclave de laboratoire portable à haute pression, stérilisateur à vapeur pour usage en laboratoire
- Stérilisateur automatique de laboratoire d'affichage numérique portable Autoclave de laboratoire pour la stérilisation sous pression
- Stérilisateur d'autoclave de laboratoire de haute pression rapide de bureau 16L 24L pour l'usage de laboratoire
- Stérilisateur Autoclave Rapide de Laboratoire de Bureau 35L 50L 90L pour Usage en Laboratoire
- Autoclave de stérilisation de laboratoire rapide de bureau 20L 24L pour usage en laboratoire
Les gens demandent aussi
- Quels sont les deux types d'autoclaves utilisés en laboratoire ? Gravité contre Pré-vide expliqués
- Pourquoi un autoclave de stérilisation à haute pression de laboratoire est-il nécessaire ? Assurer l'exactitude de la recherche antibactérienne
- Qu'est-ce qu'un autoclave de laboratoire ? Un guide sur la stérilisation à la vapeur sous pression
- Qu'est-ce qu'un autoclave de laboratoire ? Le guide ultime de la stérilisation à la vapeur
- Quelle est l'importance de l'utilisation d'un autoclave de laboratoire dans la synthèse du ZSM-5 ? Obtenir une cristallisation parfaite des zéolithes














