Dans tout système électrochimique, le but de l'électrode de référence est de fournir un potentiel stable, constant et bien connu. Elle sert de ligne de base fixe, ou de point zéro, par rapport à laquelle le potentiel d'une deuxième électrode — l'électrode de travail — peut être mesuré. En complétant le circuit électrique, elle rend possible une mesure significative.
Vous ne pouvez pas mesurer le potentiel d'une seule électrode isolément ; le potentiel est toujours une différence entre deux points. L'électrode de référence fournit une moitié fiable et immuable du système, garantissant que tout changement que vous mesurez est dû uniquement à la réaction chimique que vous étudiez à l'électrode de travail.

Le fondement de la mesure électrochimique
Pour comprendre l'électrode de référence, vous devez d'abord comprendre que toute mesure électrochimique nécessite deux électrodes pour former une cellule complète. L'électrode de référence est l'un de ces composants essentiels.
Fournir une ligne de base stable
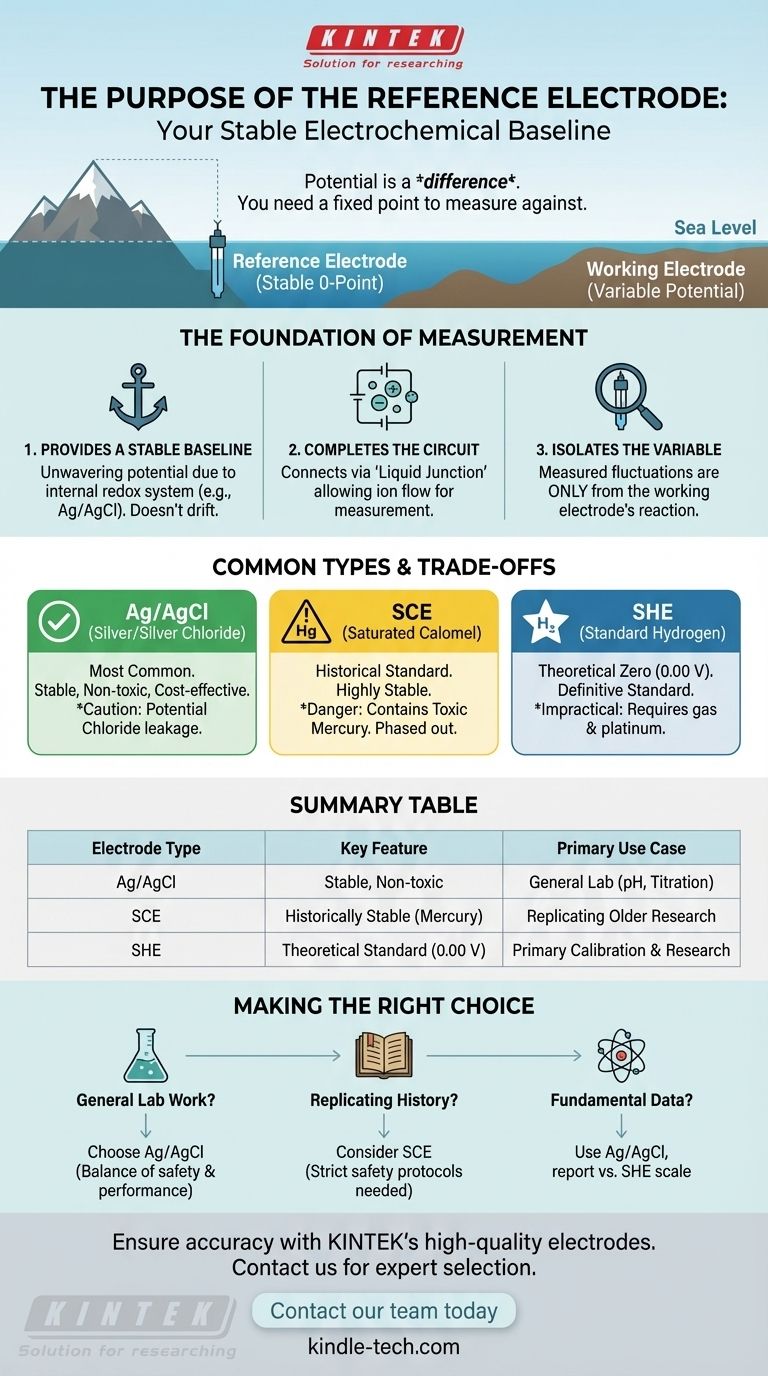
Le potentiel est une valeur relative, tout comme la hauteur d'une montagne est mesurée par rapport au niveau de la mer. L'électrode de référence agit comme le « niveau de la mer » immuable pour votre mesure.
Sa chimie interne est soigneusement conçue à l'aide d'un système redox (comme l'argent et le chlorure d'argent) avec des solutions saturées ou tamponnées. Cela garantit que son propre potentiel ne dérive pas ou ne change pas pendant l'expérience.
Compléter le circuit électrique
Une ligne de base théorique est inutile sans connexion physique. L'électrode de référence entre en contact avec la solution échantillon par l'intermédiaire d'un composant appelé jonction liquide.
Cette jonction permet aux ions de circuler, complétant ainsi le circuit électrique entre les électrodes de référence et de travail. Sans cette connexion, aucune mesure ne pourrait être effectuée.
Isoler la variable d'intérêt
En fournissant un potentiel constant, l'électrode de référence permet au potentiel total mesuré de la cellule de refléter uniquement ce qui se passe au niveau de l'électrode de travail.
Toute fluctuation détectée est donc directement attribuable à la concentration de l'analyte ou à la réaction étudiée, ce qui est l'objectif même de la mesure.
Types courants et leurs compromis
Bien que toutes les électrodes de référence servent le même objectif, elles ne sont pas toutes égales. Le choix de l'électrode implique des compromis pratiques en matière de stabilité, de coût et de sécurité.
Argent/Chlorure d'Argent (Ag/AgCl)
C'est l'électrode de référence la plus utilisée aujourd'hui. Elle est connue pour être relativement peu coûteuse, très stable et non toxique.
Son principal inconvénient est le risque que la solution de pont salin interne (chlorure de potassium) fuie dans l'échantillon, ce qui peut poser problème dans les applications sensibles aux ions chlorure.
Électrode Calomel Saturée (ECS)
L'ECS est une électrode historiquement significative réputée pour sa stabilité et sa fiabilité exceptionnelles. Elle était autrefois une norme de laboratoire.
Cependant, elle contient du mercure, qui est très toxique. En raison des préoccupations de sécurité et des défis d'élimination, son utilisation a été largement abandonnée au profit de l'électrode Ag/AgCl.
Électrode Standard à Hydrogène (ESH)
L'ESH est la référence théorique définitive par rapport à laquelle tous les autres potentiels d'électrode sont définis. Son potentiel est fixé à exactement 0,00 volt par convention.
Malgré son importance en tant que standard, l'ESH est extrêmement peu pratique pour une utilisation quotidienne. Elle nécessite un approvisionnement constant en gaz hydrogène inflammable et une électrode en platine spécialement préparée, ce qui la rend adaptée uniquement à l'étalonnage primaire et à la recherche.
Faire le bon choix pour votre objectif
Votre choix d'électrode de référence est généralement guidé par les exigences de votre application en matière de compatibilité, de précision et de sécurité.
- Si votre objectif principal est le travail général en laboratoire (par exemple, pH, titrage) : L'électrode Argent/Chlorure d'Argent (Ag/AgCl) est le choix standard pour son excellent équilibre entre performance, sécurité et coût.
- Si votre objectif principal est de reproduire des recherches plus anciennes : Vous devrez peut-être utiliser une électrode Calomel Saturée (ECS) pour maintenir la cohérence avec les données historiques, mais vous devez respecter des protocoles de sécurité stricts.
- Si votre objectif principal est d'établir des données électrochimiques fondamentales : Vous utiliserez une électrode pratique comme Ag/AgCl mais rapporterez vos résultats par rapport à l'échelle de l'Électrode Standard à Hydrogène (ESH) pour une comparaison universelle.
En fin de compte, l'électrode de référence est un outil simple mais essentiel qui élimine l'ambiguïté, vous permettant de vous concentrer sur la chimie qui compte.
Tableau récapitulatif :
| Type d'électrode | Caractéristique clé | Cas d'utilisation principal |
|---|---|---|
| Argent/Chlorure d'Argent (Ag/AgCl) | Stable, non toxique, économique | Travail général en laboratoire (pH, titrage) |
| Calomel Saturée (ECS) | Stable historiquement, contient du mercure | Reproduction de recherches plus anciennes (avec protocoles de sécurité) |
| Standard à Hydrogène (ESH) | Standard théorique (0,00 V) | Étalonnage primaire et recherche fondamentale |
Assurez la précision et la fiabilité de vos expériences électrochimiques avec la bonne électrode de référence.
KINTEK se spécialise dans les équipements de laboratoire et les consommables de haute qualité, y compris une gamme d'électrodes de référence fiables adaptées aux besoins du laboratoire. Nos experts peuvent vous aider à choisir l'électrode idéale pour votre application spécifique, garantissant des mesures précises et stables.
Contactez notre équipe dès aujourd'hui pour discuter de vos besoins et améliorer les capacités analytiques de votre laboratoire !
Guide Visuel
Produits associés
- Électrode de référence au calomel, chlorure d'argent, sulfate de mercure pour usage en laboratoire
- Électrode de référence au sulfate de cuivre pour usage en laboratoire
- Électrode électrochimique à disque métallique
- Électrode Électrochimique en Feuille d'Or Électrode en Or
- Électrode en feuille de platine pour applications en laboratoire de batteries
Les gens demandent aussi
- Quelle est la fonction d'une électrode de référence ? Maîtriser la précision dans la reconstruction de réacteurs à trois électrodes
- Quel est l'entretien recommandé pour la solution de remplissage d'une électrode de référence ? Un guide pour des lectures stables et précises
- Pourquoi la sélection d'une électrode de référence de haute qualité est-elle essentielle en synthèse électrochimique ? | KINTEK
- Quel type d'électrode peut être utilisé comme point de référence ? Sélectionnez la bonne pour des mesures précises
- Quelle électrode est utilisée comme référence de masse ? Maîtrisez la clé des mesures électrochimiques précises


















