Dans de nombreux contextes de laboratoire, les matériaux d'anode les plus couramment utilisés sont le platine, l'or et le carbone (souvent sous forme de graphite ou de carbone vitreux). Ces matériaux sont choisis pour leur inertie chimique et leur conductivité électrique, garantissant qu'ils facilitent une réaction sans y interférer. Cependant, ce n'est qu'une partie d'un tableau beaucoup plus vaste.
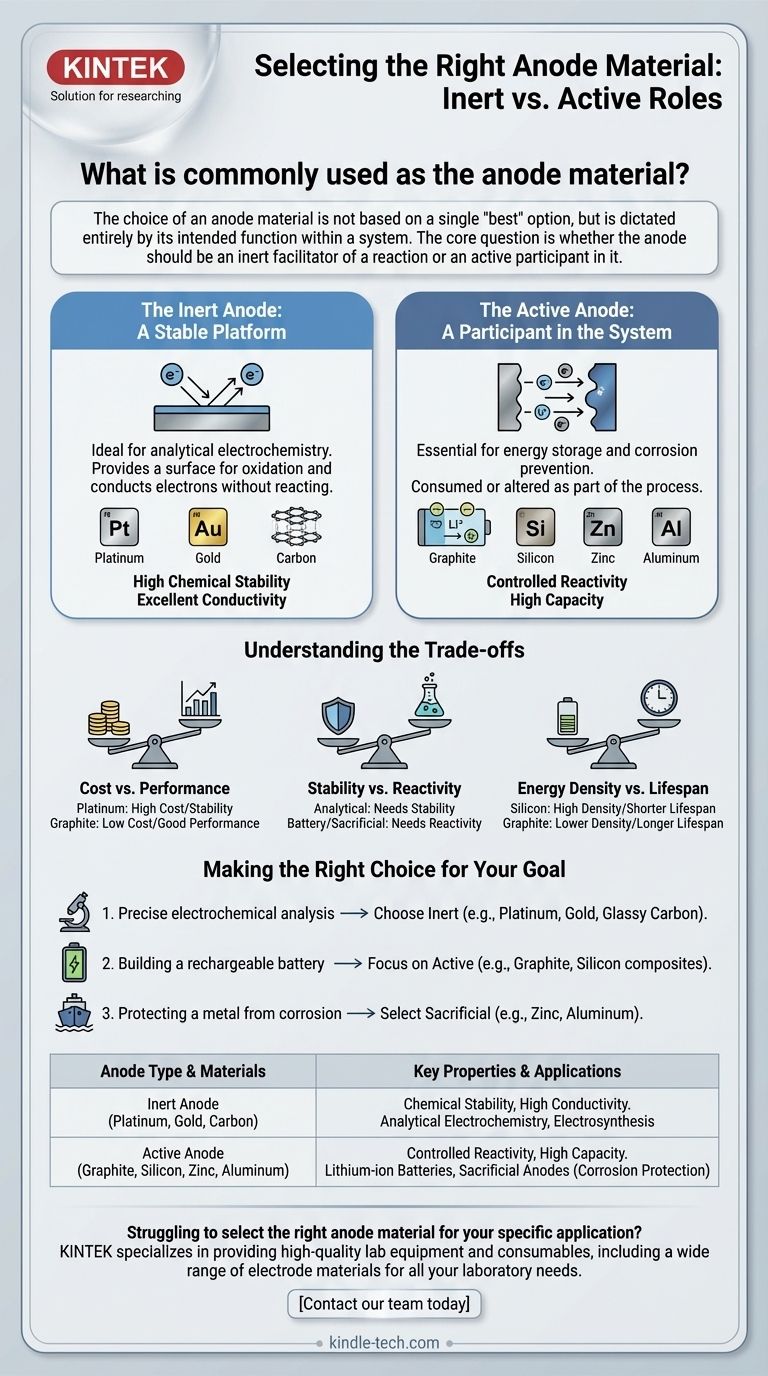
Le choix d'un matériau d'anode n'est pas basé sur une seule option "optimale", mais est entièrement dicté par sa fonction prévue au sein d'un système. La question fondamentale est de savoir si l'anode doit être un facilitateur inerte d'une réaction ou un participant actif à celle-ci.

Les deux rôles fondamentaux d'une anode
Le terme "anode" désigne simplement l'électrode où se produit l'oxydation (la perte d'électrons). Le matériau idéal pour ce rôle change radicalement en fonction de l'objectif de l'application. Nous pouvons séparer ces applications en deux catégories principales : celles nécessitant une anode inerte et celles nécessitant une anode active.
L'anode inerte : une plateforme stable
Dans des applications comme l'électrochimie analytique, une anode inerte est essentielle. Son seul rôle est de fournir une surface pour que l'oxydation se produise et de conduire les électrons hors du système.
Le matériau lui-même ne doit pas changer ni réagir. Cela garantit que les mesures prises reflètent la chimie de la solution, et non la dégradation de l'électrode.
C'est pourquoi des matériaux comme le platine, l'or et le carbone sont des choix standard. Ils possèdent les propriétés critiques de haute conductivité et d'une stabilité chimique exceptionnelle dans une large gamme de conditions.
L'anode active : un participant au système
Dans de nombreuses autres technologies critiques, l'anode est conçue pour être un participant actif et essentiel au processus chimique. Ici, le matériau est consommé ou altéré dans le cadre de la fonction du système.
C'est le cas le plus courant dans le stockage d'énergie et la prévention de la corrosion. Le matériau est choisi spécifiquement pour ses propriétés réactives.
Un excellent exemple est une batterie lithium-ion, où l'anode est généralement en graphite. Le rôle du graphite est d'absorber et de libérer des ions lithium pendant la charge et la décharge. Sa réactivité chimique est sa principale caractéristique.
Un autre exemple clé est la prévention de la corrosion, où une anode sacrificielle en zinc, aluminium ou magnésium est fixée à une structure en acier comme la coque d'un navire. Le zinc, plus réactif, se corrode (s'oxyde) en premier, se sacrifiant pour protéger l'acier.
Comprendre les compromis
La sélection d'un matériau d'anode implique toujours un équilibre entre des facteurs concurrents. Il n'existe pas de matériau unique parfait pour toutes les situations.
Coût vs. Performance
Le platine offre une stabilité et des propriétés catalytiques exceptionnelles, mais il est extrêmement coûteux. Le graphite et d'autres formes de carbone offrent d'excellentes performances pour de nombreuses applications à une fraction du coût, ce qui les rend omniprésents dans les produits commerciaux.
Stabilité vs. Réactivité
C'est le compromis central. Pour une mesure analytique, vous avez besoin d'une stabilité maximale afin que l'anode n'interfère pas. Pour une batterie ou un système sacrificiel, vous avez besoin d'une réactivité précisément contrôlée pour que l'appareil fonctionne.
Densité d'énergie vs. Durée de vie
Dans la technologie des batteries, c'est un défi critique. Le silicium fait l'objet de recherches intensives en tant que matériau d'anode de nouvelle génération car il peut contenir beaucoup plus d'ions lithium que le graphite. Cependant, il gonfle et rétrécit considérablement physiquement pendant la charge et la décharge, ce qui peut le faire se dégrader et tomber en panne rapidement.
Faire le bon choix pour votre objectif
La bonne anode est celle qui répond à l'objectif spécifique de votre système électrochimique. Votre objectif principal réduira immédiatement les options.
- Si votre objectif principal est une analyse électrochimique précise : Choisissez un matériau inerte comme le platine, l'or ou le carbone vitreux pour vous assurer que vos mesures ne sont pas influencées par l'électrode elle-même.
- Si votre objectif principal est de construire une batterie rechargeable : Concentrez-vous sur les matériaux actifs à haute capacité et stabilité cyclique, tels que le graphite ou les matériaux émergents comme les composites de silicium.
- Si votre objectif principal est de protéger un métal de la corrosion : Sélectionnez un matériau sacrificiel plus électrochimiquement actif que le métal que vous protégez, tel que le zinc ou l'aluminium pour l'acier.
En fin de compte, comprendre le rôle de l'anode – qu'il s'agisse d'une scène stable ou d'un participant actif – est la clé pour sélectionner le matériau correct pour la tâche.
Tableau récapitulatif :
| Type d'anode | Matériaux courants | Propriétés clés | Applications principales |
|---|---|---|---|
| Anode inerte | Platine, Or, Carbone (Graphite, Carbone vitreux) | Stabilité chimique, Haute conductivité | Électrochimie analytique, Électrosynthèse |
| Anode active | Graphite, Silicium, Zinc, Aluminium | Réactivité contrôlée, Haute capacité | Batteries lithium-ion, Anodes sacrificielles (Protection contre la corrosion) |
Vous avez du mal à choisir le bon matériau d'anode pour votre application spécifique ? KINTEK est spécialisé dans la fourniture d'équipements et de consommables de laboratoire de haute qualité, y compris une large gamme de matériaux d'électrodes pour tous vos besoins de laboratoire. Que vous ayez besoin d'électrodes inertes pour une analyse précise ou que vous développiez une technologie de batterie de nouvelle génération, nos experts peuvent vous aider à trouver la solution optimale. Contactez notre équipe dès aujourd'hui pour discuter de votre projet et améliorer les capacités de votre laboratoire !
Guide Visuel
Produits associés
- Four à vide graphite pour la graphitisation de matériaux négatifs
- Tissu de carbone conducteur, papier de carbone, feutre de carbone pour électrodes et batteries
- Matériau de polissage d'électrodes pour expériences électrochimiques
- Dioxyde d'iridium IrO2 pour l'électrolyse de l'eau
- Collecteur de courant en feuille d'aluminium pour batterie au lithium
Les gens demandent aussi
- Quel est le principe du four à graphite ? Atteindre des températures extrêmes grâce au chauffage résistif direct
- Qu'est-ce qu'un four à graphite mesure ? Un outil clé pour l'analyse des traces et le traitement à haute température
- Quels sont les inconvénients du four à graphite ? Limitations clés et coûts opérationnels
- Quels sont les avantages du four à graphite ? Atteindre une précision et une pureté à haute température
- Qu'est-ce qu'un four à graphite ? Atteignez des températures et une pureté extrêmes pour les matériaux avancés

















