L'illusion de la simplicité
Au laboratoire, les moments les plus critiques sont souvent les plus calmes.
Nous avons tendance à nous obséder de la chimie complexe — les réactifs exotiques, la tension précise, le rendement théorique. Mais en électrochimie, toute l'expérience repose sur un acte mécanique qui prend moins de cinq minutes : l'installation des électrodes.
Cela semble anodin. Vous mettez le métal dans le verre. Vous allumez le courant.
Mais cette vision est dangereuse.
Une cellule électrolytique n'est pas juste un récipient ; c'est un circuit. L'électrode est l'interface où le monde physique rencontre le monde chimique. Si cette interface est défectueuse — même d'un millimètre — les données ne sont pas juste légèrement faussées. Elles sont fictives.
Voici comment aborder le processus d'installation avec la précision d'un ingénieur et la discipline d'un chirurgien.
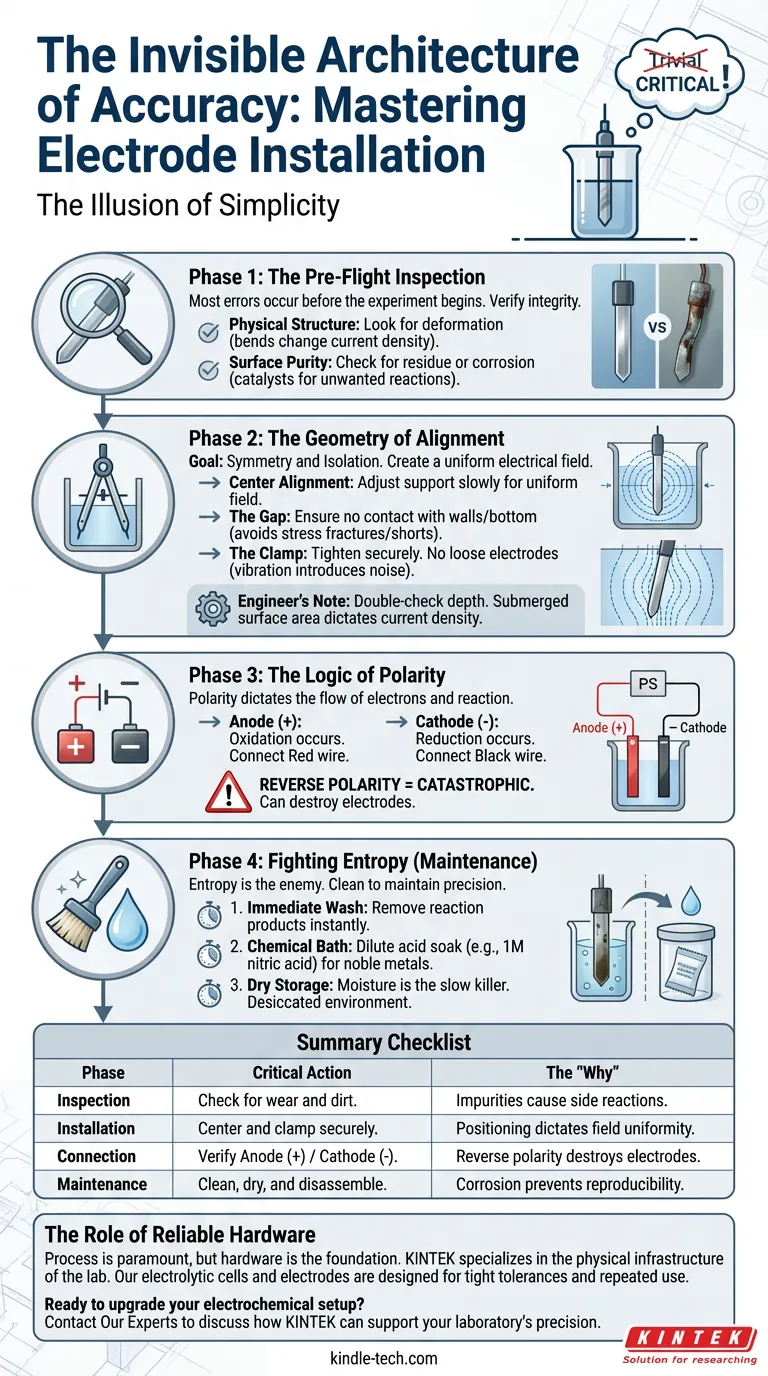
Phase 1 : L'inspection avant le vol
La plupart des erreurs se produisent avant le début de l'expérience.
Nous supposons souvent que parce qu'une électrode semble solide, elle est fonctionnelle. C'est un biais cognitif connu sous le nom de « ce que vous voyez est tout ce qu'il y a ». Cependant, en électrochimie, la chimie de surface est primordiale.
Avant que l'électrode ne touche la cellule, vous devez vérifier son intégrité :
- Structure physique : Recherchez toute déformation. Une électrode tordue modifie la distribution de la densité de courant.
- Pureté de la surface : Vérifiez la présence de résidus ou de corrosion. Une tache de saleté n'est pas juste de la saleté ; c'est un catalyseur de réactions secondaires indésirables.
Si la surface est compromise, l'expérience est condamnée avant même de commencer. Les surfaces propres ne sont pas un luxe ; elles sont une condition préalable.
Phase 2 : La géométrie de l'alignement
Une fois l'inspection terminée, nous passons à l'installation physique.
C'est un jeu de géométrie. L'objectif est la symétrie et l'isolation.
Lorsque vous abaissez les électrodes dans la cellule, vous essayez de créer un champ électrique uniforme. Si une électrode est de travers, le champ se déforme. Les vitesses de réaction changent. La reproductibilité disparaît.
Les règles de placement
- Alignement centré : Ajustez le mécanisme de support lentement. L'électrode doit être l'axe autour duquel la cellule tourne.
- L'espace : Assurez-vous que l'électrode ne touche jamais le fond ou les parois de la cellule. Le contact avec le verre peut provoquer des fractures de contrainte. Le contact avec l'autre électrode provoque un court-circuit.
- Le collier de serrage : Une fois positionné, serrez les colliers de serrage du support. Ne vous fiez pas à la gravité ou à la friction. Une électrode lâche vibre, et la vibration introduit du bruit dans vos données.
Note de l'ingénieur : Vérifiez deux fois votre profondeur. La surface immergée dicte la densité de courant. Si la profondeur change, vos calculs sont faussés.
Phase 3 : La logique de la polarité
La chimie a une direction.
Connecter l'alimentation n'est pas comme brancher un grille-pain. La polarité dicte le flux des électrons, et par conséquent, le flux de la réaction.
- Anode (+) : L'oxydation se produit ici.
- Cathode (-) : La réduction se produit ici.
Une inversion ici est catastrophique. Elle n'arrête pas seulement l'expérience ; elle détruit souvent les électrodes en forçant l'oxydation sur un matériau conçu pour la réduction.
Tracez toujours le fil de la source à la cellule. Rouge vers l'anode. Noir vers la cathode. Ne vous fiez pas à votre mémoire. Faites confiance au fil.
Phase 4 : Combattre l'entropie (Maintenance)
L'expérience ne se termine pas lorsque le courant est coupé.
L'entropie est l'ennemi de l'équipement de laboratoire. Si vous laissez une électrode humide d'électrolyte, la corrosion commence immédiatement. Les sels cristallisent. Le métal se dégrade.
Pour maintenir le « romantisme » d'une machinerie précise, vous devez la nettoyer.
- Lavage immédiat : Retirez les produits de réaction immédiatement.
- Bain chimique : Pour les métaux nobles comme le platine, un bain d'acide dilué (par exemple, de l'acide nitrique 1M) restaure la surface.
- Stockage à sec : L'humidité est le tueur lent. Stockez les composants dans un environnement déshydraté.
Si vous stockez la cellule à long terme, démontez-la. Laisser de l'électrolyte dans une cellule scellée, c'est inviter la dégradation.
Liste de contrôle récapitulative
Un professionnel traite ce processus comme un système, pas comme une corvée.
| Phase | Action critique | Le « Pourquoi » |
|---|---|---|
| Inspection | Vérifier l'usure et la saleté. | Les impuretés provoquent des réactions secondaires. |
| Installation | Centrer et serrer fermement. | Le positionnement dicte l'uniformité du champ. |
| Connexion | Vérifier Anode (+) / Cathode (-). | L'inversion de polarité détruit les électrodes. |
| Maintenance | Nettoyer, sécher et démonter. | La corrosion empêche la reproductibilité. |
Le rôle du matériel fiable
Le processus est primordial, mais le matériel en est le fondement.
Vous ne pouvez pas effectuer un travail précis avec des colliers de serrage instables ou des métaux impurs. Le meilleur protocole au monde ne peut compenser une électrode qui se dégrade de manière imprévisible ou une cellule qui se déforme sous contrainte thermique.
C'est là qu'intervient KINTEK.
Nous sommes spécialisés dans l'infrastructure physique du laboratoire. Nos cellules électrolytiques et nos électrodes en platine ou en graphite sont conçues pour résister aux rigueurs d'une utilisation répétée. Nous construisons notre équipement avec des tolérances serrées que les ingénieurs apprécient, garantissant que lorsque vous centrez une électrode, elle reste centrée.
Votre recherche mérite un équipement aussi discipliné que vous.
Prêt à améliorer votre configuration électrochimique ?
Contactez nos experts pour discuter de la manière dont KINTEK peut soutenir la précision de votre laboratoire.
Guide Visuel
Produits associés
- Électrode de référence au calomel, chlorure d'argent, sulfate de mercure pour usage en laboratoire
- Électrode électrochimique à disque métallique
- Électrode à disque rotatif (disque-anneau) RRDE / Compatible avec PINE, ALS japonais, Metrohm suisse carbone vitreux platine
- Électrode à disque de platine rotatif pour applications électrochimiques
- Électrode en feuille de platine pour applications en laboratoire de batteries
Articles associés
- Comment choisir la bonne électrode de référence pour votre application
- Guide complet des électrodes de référence : Types, applications et critères de sélection
- Électrodes de référence communes dans les études électrochimiques
- Conception et application d'électrodes de référence dans les piles au lithium
- Utilisation et entretien des électrodes de référence




















