À la base, le principe de l'électrodéposition est le processus d'utilisation d'un courant électrique continu pour réduire les ions métalliques dissous d'une solution et former un revêtement métallique mince et solide sur un objet conducteur. Cette réaction électrochimique contrôlée vous permet de « plaquer » un métal sur un autre, modifiant fondamentalement les propriétés de surface du matériau de base.
L'ensemble du processus repose sur la création d'un circuit électrolytique. Dans ce circuit, l'électricité entraîne une réaction chimique non spontanée, forçant les ions métalliques chargés positivement dans un bain liquide à accepter des électrons et à se déposer sous forme de couche métallique neutre sur une surface cible.
Les composants essentiels d'un système d'électrodéposition
Pour comprendre le principe en pratique, vous devez d'abord comprendre ses quatre composants essentiels fonctionnant ensemble dans une cellule électrolytique.
L'électrolyte (le bain)
L'électrolyte est une solution contenant une forte concentration des ions métalliques que vous souhaitez déposer. Il est généralement préparé en dissolvant des sels métalliques (comme le sulfate de cuivre ou le chlorure de nickel) dans l'eau. Le bain contient également d'autres additifs pour contrôler la qualité du revêtement final.
La cathode (le substrat)
La cathode est l'objet que vous avez l'intention de revêtir. Elle est connectée à la borne négative de l'alimentation électrique. Cette charge négative attire les ions métalliques chargés positivement de l'électrolyte.
L'anode (la source de métal)
L'anode est connectée à la borne positive de l'alimentation électrique. Elle peut être de deux types :
- Anode active : Fabriquée dans le même métal que celui déposé. Elle se dissout lentement, réapprovisionnant les ions métalliques dans l'électrolyte à mesure qu'ils sont déposés sur la cathode.
- Anode inerte : Fabriquée dans un matériau non réactif (comme le platine ou le carbone). Elle ne se dissout pas mais sert à compléter le circuit électrique. Dans ce cas, les ions métalliques du bain s'épuisent avec le temps.
L'alimentation électrique
Une alimentation en courant continu (CC) agit comme le moteur de l'ensemble du processus. Elle fournit le potentiel électrique nécessaire pour acheminer les électrons vers la cathode et les retirer de l'anode, forçant la réaction de dépôt à se produire.
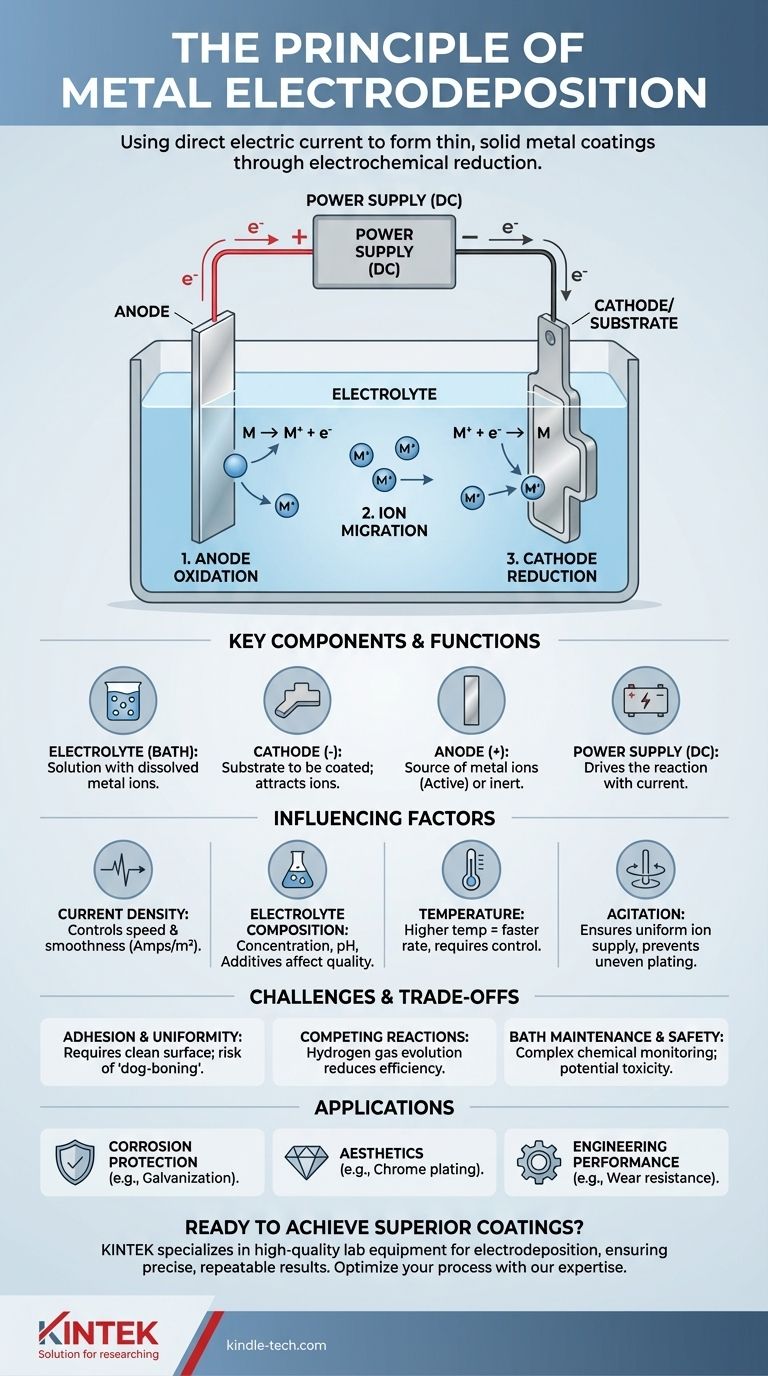
Le processus électrochimique, étape par étape
Le processus de dépôt est une boucle continue d'oxydation et de réduction entraînée par l'alimentation externe.
Étape 1 : Oxydation à l'anode
À l'anode positive, une réaction d'oxydation se produit. Si l'anode est active, ses atomes métalliques perdent des électrons et deviennent des ions chargés positivement, se dissolvant dans l'électrolyte. Cela maintient un approvisionnement constant en ions métalliques.
Étape 2 : Migration des ions dans l'électrolyte
Les ions métalliques chargés positivement (cations) présents dans l'électrolyte sont attirés à travers la solution vers la cathode chargée négativement. Simultanément, les ions négatifs (anions) dérivent vers l'anode positive, maintenant la solution électriquement neutre.
Étape 3 : Réduction à la cathode
C'est l'étape de dépôt. Lorsque les ions métalliques atteignent la cathode, ils gagnent des électrons fournis par la source d'alimentation. Cette réaction de réduction neutralise leur charge, provoquant leur précipitation hors de la solution et leur liaison à la surface sous forme d'atomes métalliques solides, construisant le revêtement couche par couche.
Facteurs clés influençant la qualité du dépôt
La qualité, l'épaisseur et l'apparence du revêtement final ne sont pas automatiques. Elles dépendent du contrôle minutieux de plusieurs variables clés.
Densité de courant
C'est la quantité de courant par unité de surface de la cathode (mesurée en ampères/m²).
- Une faible densité de courant entraîne un revêtement lent mais souvent plus lisse et plus uniforme.
- Une densité de courant élevée accélère le dépôt mais peut entraîner des dépôts rugueux, poreux ou brûlés s'ils ne sont pas gérés correctement.
Composition de l'électrolyte
La concentration des ions métalliques, le niveau de pH et la présence d'additifs (tels que les agents de brillance et les agents de nivellement) ont un impact énorme. Ces additifs peuvent modifier la structure cristalline du métal déposé, changeant son aspect de terne à brillant comme un miroir.
Température
Des températures de bain plus élevées augmentent généralement la conductivité de l'électrolyte et le taux de dépôt. Cependant, des températures excessivement élevées peuvent provoquer des réactions secondaires indésirables ou la décomposition des additifs.
Agitation
Remuer ou agiter autrement le bain est essentiel. Cela garantit qu'un approvisionnement frais en ions métalliques atteint la surface de la cathode, empêchant l'appauvrissement localisé qui provoque un placage inégal, en particulier sur des formes complexes.
Comprendre les compromis et les défis
Bien que puissante, l'électrodéposition est un processus précis avec des points de défaillance courants.
Adhérence et uniformité du revêtement
Le facteur le plus critique pour le succès est la préparation du substrat. Une surface sale ou oxydée entraînera une mauvaise adhérence, provoquant le pelage ou l'écaillage du revêtement. De plus, le courant électrique se concentre naturellement sur les bords vifs et les coins, entraînant des dépôts plus épais à ces endroits et des dépôts plus minces dans les évidements — un problème connu sous le nom d'effet « dog-boning » (effet d'os de chien).
Réactions concurrentes
La principale réaction concurrente, en particulier dans les électrolytes aqueux, est la réduction de l'eau pour produire de l'hydrogène gazeux à la cathode. Ce processus consomme le courant électrique qui serait autrement utilisé pour le dépôt métallique, réduisant l'efficacité globale. Dans certains cas, l'hydrogène absorbé peut également rendre le substrat cassant.
Entretien du bain et sécurité
Les bains d'électrodéposition sont des systèmes chimiques complexes qui nécessitent une surveillance et un ajustement constants du pH, de la température et des concentrations chimiques. De nombreuses solutions de placage industrielles, telles que celles contenant du cyanure ou du chrome hexavalent, sont très toxiques et présentent des risques importants pour l'environnement et la sécurité des opérateurs.
Faire le bon choix pour votre application
Comprendre le principe de base vous permet d'adapter le processus à votre objectif spécifique.
- Si votre objectif principal est la protection contre la corrosion : Votre objectif est une couche dense et non poreuse, utilisant souvent un métal sacrificiel comme le zinc sur l'acier (galvanisation) ou un métal noble comme l'or.
- Si votre objectif principal est l'esthétique : Vous devez contrôler soigneusement la densité de courant et utiliser des additifs spécifiques tels que des agents de brillance pour obtenir une surface lisse et réfléchissante, comme on le voit avec le placage au chrome ou au nickel.
- Si votre objectif principal est la performance technique (par exemple, la résistance à l'usure) : Vous avez besoin d'un contrôle précis de l'épaisseur et de la dureté, souvent obtenu avec du chrome dur ou des revêtements en nickel chimique, où une forte adhérence est primordiale.
En contrôlant le flux d'ions et d'électrons, vous pouvez transformer la surface d'un matériau pour répondre à un besoin technique ou esthétique spécifique.

Tableau récapitulatif :
| Composant clé | Rôle dans l'électrodéposition |
|---|---|
| Électrolyte (Bain) | Solution contenant les ions métalliques dissous à déposer. |
| Cathode (Substrat) | L'objet à revêtir ; attire les ions métalliques positifs. |
| Anode (Source de métal) | Source d'ions métalliques (active) ou électrode inerte. |
| Alimentation (CC) | Fournit le courant pour entraîner la réaction non spontanée. |
| Densité de courant | Contrôle la vitesse de dépôt et la qualité du revêtement (lissage). |
| Additifs de bain | Influencent les propriétés finales du revêtement (par exemple, brillance, dureté). |
Prêt à obtenir des revêtements métalliques supérieurs dans votre laboratoire ?
Comprendre les principes de l'électrodéposition est la première étape. Sa mise en œuvre efficace nécessite l'équipement et les consommables appropriés. KINTEK est spécialisé dans les équipements de laboratoire de haute qualité pour l'électrodéposition et d'autres processus d'ingénierie des surfaces, vous aidant à obtenir des résultats précis, fiables et reproductibles.
Que vous vous concentriez sur la recherche, le contrôle qualité ou le développement de nouveaux revêtements, notre expertise peut soutenir les besoins de votre laboratoire.
Contactez nos experts dès aujourd'hui pour discuter de la manière dont nous pouvons vous aider à optimiser votre processus d'électrodéposition !
Guide Visuel
Produits associés
- Électrode électrochimique à disque métallique
- Creuset et bateau d'évaporation en cuivre sans oxygène pour revêtement par évaporation par faisceau d'électrons
- Feuille de métal expansé cuivre-nickel
- Feuilles de métaux or, platine, cuivre et fer de haute pureté
- Électrode Électrochimique en Feuille d'Or Électrode en Or
Les gens demandent aussi
- Quel est le rôle des électrodes métalliques dans la synthèse hydrothermale assistée par voie électrochimique ? Experts en revêtements à basse température
- Comment préparer une électrode à disque métallique et son électrolyte correspondant avant une expérience ? Un guide étape par étape
- Quelles sont les méthodes de protection de surface recommandées pour différents types d'électrodes à disque métallique ? Guide essentiel pour la longévité
- Quelles précautions faut-il prendre lors de l'utilisation d'électrodes à disque métallique ? Assurer la précision et la longévité
- Quelle est la durée de vie prévue d'une électrode à disque métallique ? Prolongez sa durée de vie grâce à un entretien approprié



















