Fondamentalement, une cellule électrolytique pour la corrosion sur plaque plate fonctionne en utilisant une source d'alimentation externe pour induire et contrôler délibérément la corrosion sur un échantillon métallique. Cette configuration force une réaction électrochimique non spontanée à se produire, permettant aux chercheurs d'accélérer, de mesurer et d'analyser les caractéristiques de dégradation du matériau dans un environnement hautement contrôlé.
Pour comprendre la science des matériaux, il faut souvent étudier comment les matériaux échouent. La cellule électrolytique à plaque plate est un outil spécialisé qui transforme le processus lent et imprévisible de la corrosion en une expérience quantifiable et reproductible en utilisant l'énergie électrique comme force motrice précise.

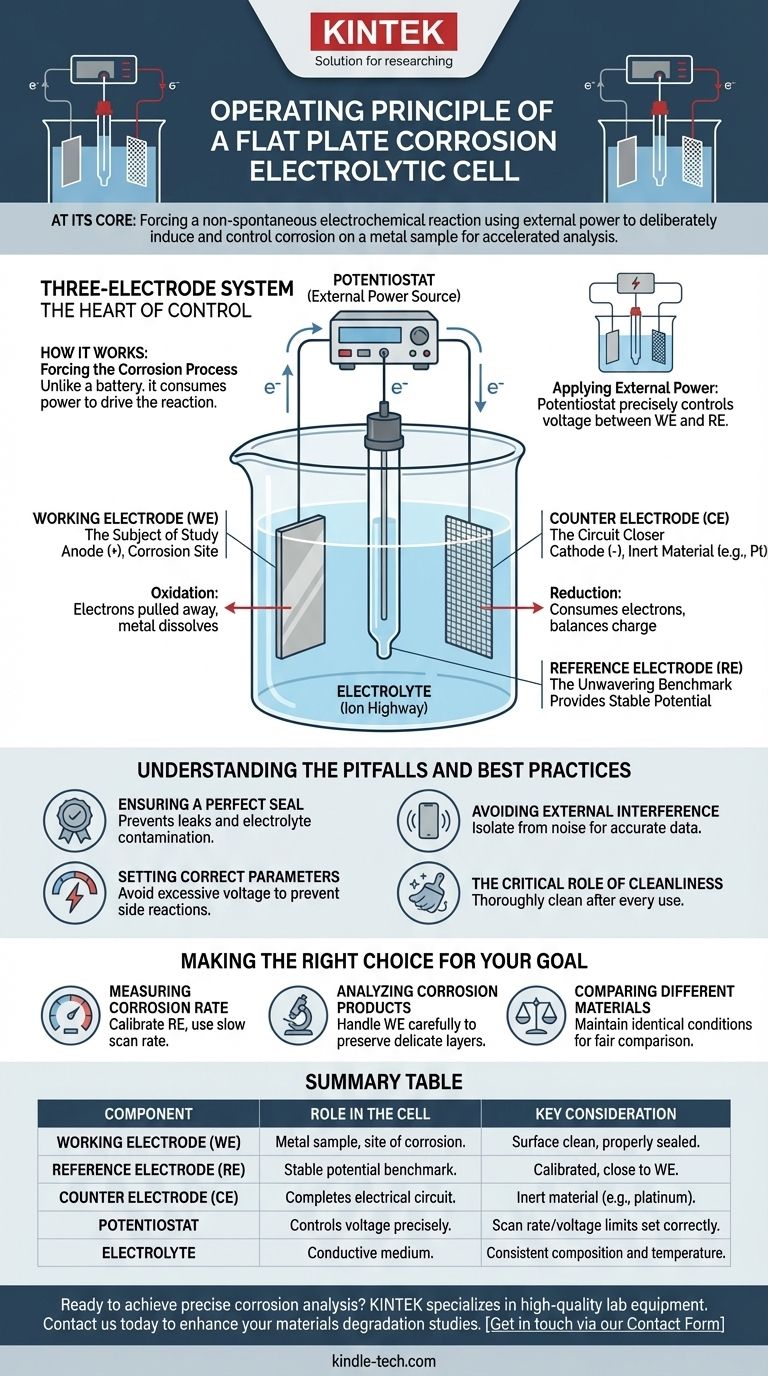
Le système à trois électrodes : le cœur du contrôle
La précision d'une cellule de corrosion provient de sa configuration à trois électrodes. Chaque composant a une fonction distincte et critique qui, ensemble, permet une mesure précise.
L'Électrode de Travail (ET) : Le Sujet de l'Étude
C'est l'échantillon métallique à plaque plate étudié. C'est la surface où la réaction de corrosion (oxydation) est intentionnellement initiée et mesurée. Son potentiel est la principale variable contrôlée et surveillée.
L'Électrode Auxiliaire (EA) : Le Complément du Circuit
Généralement fabriquée à partir d'un matériau inerte comme un treillis de platine, le seul rôle de l'électrode auxiliaire est de compléter le circuit électrique. Elle permet au courant de circuler à travers l'électrolyte vers et depuis l'électrode de travail, mais elle ne participe pas à la réaction étudiée.
L'Électrode de Référence (ER) : L'Étalon Inébranlable
L'électrode de référence, souvent une électrode argent/chlorure d'argent (Ag/AgCl), fournit un potentiel stable et constant qui ne change pas pendant l'expérience. Toutes les mesures de potentiel de l'électrode de travail sont effectuées par rapport à cet étalon inébranlable, garantissant que les données sont précises, reproductibles et comparables entre différentes expériences.
L'Électrolyte : L'Autoroute Ionique
C'est la solution corrosive (par exemple, eau salée, acide) qui remplit la cellule. Elle sert de milieu conducteur, contenant des ions qui migrent entre les électrodes pour transporter la charge et compléter la réaction électrochimique.
Comment cela fonctionne : Forcer le processus de corrosion
Contrairement à une batterie, qui génère de l'énergie à partir d'une réaction chimique spontanée, une cellule électrolytique consomme de l'énergie pour piloter une réaction qui ne se produirait pas d'elle-même.
Application d'une Alimentation Externe
Une source d'alimentation externe, généralement un appareil sophistiqué appelé potentiostat, est connectée aux trois électrodes. Cet instrument contrôle précisément la tension entre l'électrode de travail et l'électrode de référence.
Pilotage de l'Oxydation à l'Anode
Le potentiostat fait de l'électrode de travail l'anode (la borne positive). Ce potentiel électrique extrait activement les électrons des atomes métalliques à la surface de l'échantillon, les forçant à s'oxyder — c'est-à-dire à se corroder et à se dissoudre dans l'électrolyte sous forme d'ions positifs.
Équilibrage de la Réaction à la Cathode
Simultanément, l'électrode auxiliaire est faite cathode (la borne négative). Elle facilite une réaction de réduction (par exemple, la conversion des ions hydrogène dans l'électrolyte en gaz hydrogène) qui consomme les électrons circulant dans le circuit externe. Cela équilibre la charge globale.
Comprendre les pièges et les meilleures pratiques
Bien que puissante, la précision des résultats obtenus à partir d'une cellule électrolytique dépend entièrement d'une technique expérimentale méticuleuse.
Assurer une Étanchéité Parfaite
Le joint autour de l'échantillon à plaque plate est un point de défaillance courant. Toute fuite dans la cellule peut compromettre la concentration de l'électrolyte, endommager l'équipement et invalider les données expérimentales.
Éviter les Interférences Externes
Les mesures de corrosion impliquent souvent des courants électriques et des tensions très faibles. La configuration expérimentale doit être isolée des vibrations et des champs électromagnétiques externes (provenant, par exemple, d'autres équipements de laboratoire) qui peuvent introduire du bruit et corrompre les données.
Définir les Paramètres Corrects
L'application d'une tension excessive peut provoquer des réactions secondaires non désirées, telles que la décomposition rapide de l'électrolyte lui-même (électrolyse). Cela masque les données de corrosion souhaitées et peut même endommager les électrodes. Les paramètres doivent être choisis avec soin en fonction du matériau et de l'électrolyte.
Le Rôle Critique de la Propreté
La cellule doit être soigneusement nettoyée à l'eau désionisée après chaque utilisation. Tout résidu ou contamination d'une expérience précédente peut modifier radicalement l'environnement chimique et fausser les résultats du test suivant.
Faire le Bon Choix pour Votre Objectif
Pour obtenir des données significatives, votre procédure expérimentale doit s'aligner sur votre objectif de recherche.
- Si votre objectif principal est de mesurer le taux de corrosion (par exemple, courbes de polarisation) : Assurez-vous que votre électrode de référence est correctement calibrée et positionnée près de l'électrode de travail, et utilisez une vitesse de balayage de potentiel lente et régulière pour permettre au système de se stabiliser à chaque étape.
- Si votre objectif principal est d'analyser les produits de corrosion : Manipulez l'électrode de travail avec un soin extrême après l'expérience pour préserver la couche délicate de produits de corrosion à sa surface pour une analyse microscopique ou spectroscopique ultérieure.
- Si votre objectif principal est de comparer différents matériaux : Maintenez des conditions expérimentales identiques — température, composition de l'électrolyte et paramètres électriques — pour chaque échantillon afin de garantir que votre comparaison est équitable et précise.
En maîtrisant ces principes, vous pouvez transformer la cellule électrolytique d'un simple équipement de laboratoire en un instrument puissant pour l'analyse quantitative des matériaux.
Tableau Récapitulatif :
| Composant | Rôle dans la Cellule | Considération Clé |
|---|---|---|
| Électrode de Travail (ET) | L'échantillon métallique à l'étude ; site de corrosion. | La surface doit être propre et correctement scellée pour éviter les fuites. |
| Électrode de Référence (ER) | Fournit un étalon de potentiel stable pour des mesures précises. | Doit être calibrée et positionnée près de l'ET. |
| Électrode Auxiliaire (EA) | Complète le circuit électrique, permettant au courant de circuler. | Généralement fabriquée à partir d'un matériau inerte comme le platine. |
| Potentiostat | La source d'alimentation externe qui contrôle précisément la tension. | La vitesse de balayage et les limites de tension doivent être réglées correctement pour éviter les réactions secondaires. |
| Électrolyte | La solution corrosive qui sert de milieu conducteur. | La composition et la température doivent être cohérentes pour des résultats comparables. |
Prêt à obtenir une analyse de corrosion précise et reproductible dans votre laboratoire ?
KINTEK est spécialisée dans les équipements de laboratoire et les consommables de haute qualité pour la science des matériaux. Que vous installiez une nouvelle station d'essai de corrosion ou que vous ayez besoin d'optimiser votre flux de travail existant, notre gamme de cellules électrolytiques, d'électrodes et de potentiostats fiables est conçue pour fournir la précision et le contrôle dont votre recherche a besoin.
Contactez-nous dès aujourd'hui pour discuter de vos besoins spécifiques en laboratoire et laissez nos experts vous aider à choisir l'équipement parfait pour améliorer vos études de dégradation des matériaux.
Contactez-nous via notre formulaire de contact pour en savoir plus sur nos produits et services.
Guide Visuel
Produits associés
- Cellule électrochimique de corrosion plane
- Cellule électrolytique en PTFE Cellule électrochimique scellée et non scellée résistante à la corrosion
- Cellule électrochimique électrolytique pour l'évaluation des revêtements
- Cellule électrochimique à électrolyse spectrale en couche mince
- Cellules d'électrolyse PEM personnalisables pour diverses applications de recherche
Les gens demandent aussi
- Quels sont les avantages de conception d'une cellule électrochimique plane ? Améliorer la précision des tests de corrosion
- Pourquoi un système de contrôle de température constant est-il requis pour les tests de corrosion électrochimique dans le SBF ? Clé de la précision en laboratoire
- Quelles sont les précautions critiques de sécurité et d'utilisation pour l'utilisation d'une cellule électrolytique de corrosion à plaque plane ? Assurez des tests électrochimiques sûrs et précis
- Quelles sont les procédures et les observations nécessaires lors d'une expérience avec une cellule électrolytique à plaque plane pour la corrosion ? Maîtriser la méthode en 3 phases
- Quelle est la différence entre une cellule de corrosion électrolytique et une cellule de corrosion électrochimique ? Comprendre la force motrice derrière la corrosion















