L'illusion du bouton
Il y a une tentation dans le travail de laboratoire de considérer le contrôle comme un simple acte mécanique. Vous tournez un bouton, l'aiguille bouge, et la machine obéit.
En électrochimie, cette vision est dangereuse.
Une cellule électrolytique n'est pas simplement une machine ; c'est un environnement chaotique où vous tentez de forcer la nature à reculer. Vous utilisez de l'énergie pour piloter des réactions non spontanées. Pour ce faire avec succès, vous ne pouvez pas simplement "l'allumer".
Vous devez agir en tant qu'architecte de l'environnement atomique.
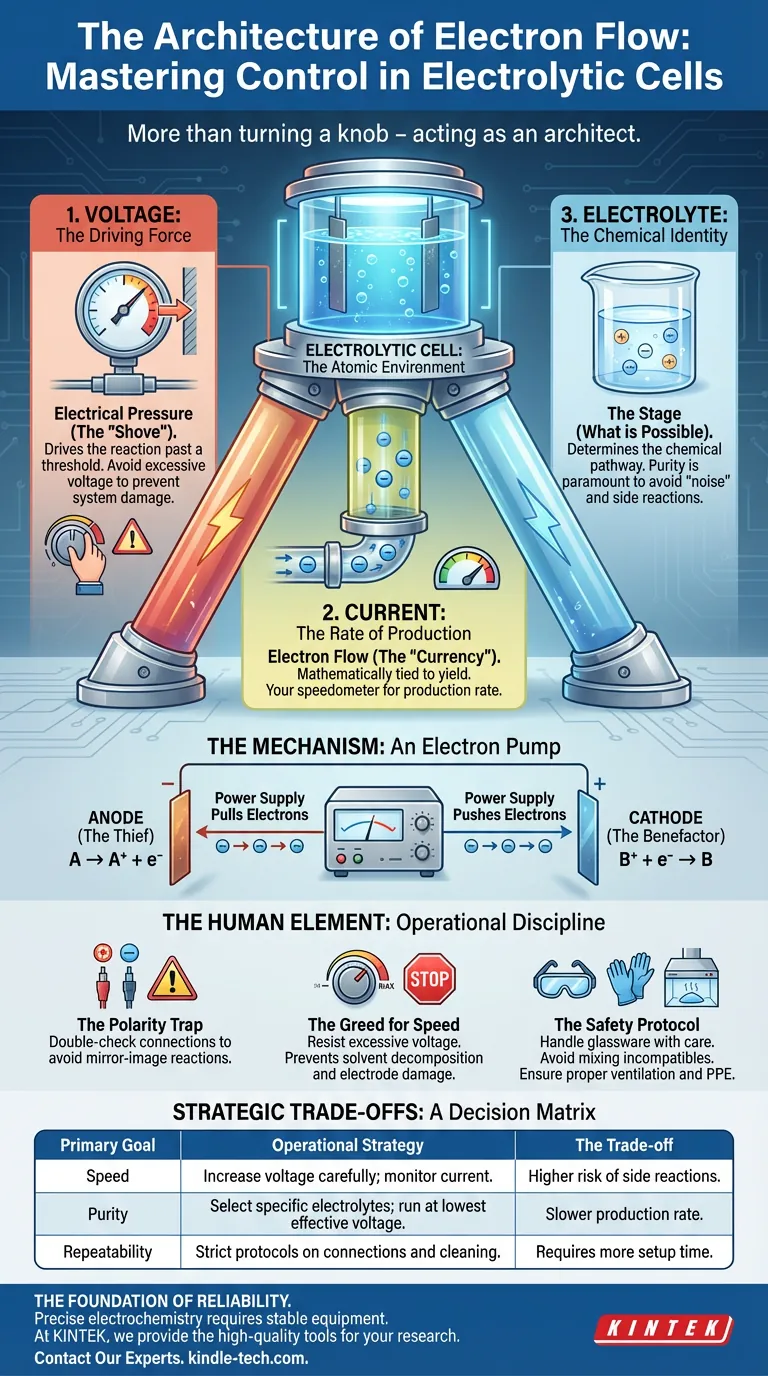
Le contrôle dans ce contexte est un trépied. Il repose sur trois piliers non négociables : la tension, le courant et la composition. Si vous en ignorez un, la structure s'effondre.
Les trois leviers d'influence
Pour maîtriser le rendement de votre cellule, vous devez comprendre le rôle distinct de chaque variable. Ils sont interconnectés, mais ils ne sont pas identiques.
1. La tension : la force motrice
Considérez la tension comme une pression électrique. C'est la poussée nécessaire pour que la réaction démarre.
Sans tension suffisante, rien ne se passe. La barrière à la réaction reste trop élevée. Cependant, plus n'est pas toujours mieux. Augmenter la tension augmente la vitesse, mais seulement jusqu'à un certain seuil. Au-delà de ce point, vous ne pilotez plus la réaction, vous endommagez le système.
2. Le courant : le taux de production
Le courant est le flux d'électrons. Dans l'économie de la cellule électrolytique, les électrons sont la monnaie.
La quantité de produit que vous créez est mathématiquement liée au courant. Si vous voulez un rendement plus élevé, vous avez besoin de plus de charge traversant le système au fil du temps. Le courant est votre compteur de vitesse.
3. L'électrolyte : l'identité chimique
L'électrolyte est la scène où se déroule la pièce. Il détermine quelle réaction est chimiquement possible.
Si la tension et le courant sont le moteur, l'électrolyte est la destination. La pureté est primordiale ici. Un électrolyte contaminé introduit du "bruit" dans le système, entraînant des réactions secondaires qui ruinent le produit final.
Le mécanisme : une pompe à électrons
Pour contrôler la cellule, vous devez visualiser ce qui se passe aux électrodes. L'alimentation externe agit comme une pompe, créant un déséquilibre que la nature cherche désespérément à corriger.
- À l'anode (le voleur) : L'alimentation retire les électrons. Cela force les espèces de l'électrolyte à perdre des électrons (oxydation).
- À la cathode (le bienfaiteur) : L'alimentation injecte des électrons. Cela force les espèces à gagner des électrons (réduction).
Votre travail consiste à réguler cette pompe afin que l'échange se produise exactement comme prévu, sans submerger la capacité chimique de la solution.
L'élément humain : la discipline opérationnelle
La plus grande variable dans toute expérience est l'opérateur. Les connaissances théoriques échouent face à la négligence pratique.
En chirurgie, une liste de contrôle sauve des vies. En laboratoire, un protocole sauve des expériences.
Le piège de la polarité
Inverser l'anode et la cathode est une erreur simple aux conséquences profondes. Elle crée une réaction miroir, produisant les mauvaises substances aux mauvais pôles. Vérifiez vos connexions deux fois.
L'avidité pour la vitesse
Il y a une envie psychologique de faire monter la tension pour finir plus vite. Résistez-y.
Une tension excessive conduit souvent à la décomposition du solvant (généralement de l'eau) ou à la dégradation de la surface de l'électrode. Vous sacrifiez la pureté pour la vitesse, et généralement, vous perdez les deux.
Le protocole de sécurité
La chimie est impitoyable face à la complaisance.
- Verrerie : Manipulez la cellule avec soin. Les rayures causées par les brosses métalliques affaiblissent l'intégrité structurelle.
- Mélanges : Ne mélangez jamais les acides et les bases lors du nettoyage. La réaction exothermique résultante peut faire éclater le récipient.
- Protection : Les électrolytes corrosifs et les gaz toxiques exigent une ventilation adéquate (hottes de laboratoire) et des EPI.
Compromis stratégiques
La perfection est impossible. L'optimisation est l'objectif. Votre stratégie de contrôle doit évoluer en fonction de votre objectif spécifique.
Utilisez cette matrice de décision pour guider votre configuration :
| Objectif principal | Stratégie opérationnelle | Le compromis |
|---|---|---|
| Vitesse | Augmentez la tension prudemment ; surveillez le courant. | Risque plus élevé de réactions secondaires. |
| Pureté | Sélectionnez des électrolytes spécifiques ; fonctionnez à la tension la plus basse efficace. | Taux de production plus lent. |
| Répétabilité | Protocoles stricts sur les connexions et le nettoyage. | Nécessite plus de temps d'installation. |
Les fondements de la fiabilité
Vous ne pouvez pas contrôler une réaction si vous ne pouvez pas faire confiance à vos outils.
Une électrochimie précise nécessite un équipement qui fournit une tension stable, un courant constant et des matériaux durables qui résistent aux environnements corrosifs sans contaminer vos résultats.
Chez KINTEK, nous comprenons la romance de l'ingénieur avec la précision. Nous sommes spécialisés dans la fourniture d'équipements de laboratoire et de consommables de haute qualité qui servent de partenaire silencieux dans vos recherches. Lorsque le matériel est fiable, vous êtes libre de vous concentrer sur la science.
Guide Visuel
Produits associés
- Cellule électrolytique en PTFE Cellule électrochimique scellée et non scellée résistante à la corrosion
- Cellule électrochimique électrolytique super scellée
- Cellule électrochimique électrolytique à cinq ports
- Cellule électrolytique de type H Triple Cellule électrochimique
- Cellule de diffusion de gaz électrolytique électrochimique à flux liquide
Articles associés
- L'ancre de la vérité : Pourquoi la stabilité physique définit le succès électrochimique
- L'art du non-spontané : la précision dans les circuits électrolytiques
- Le partenaire silencieux : pourquoi le choix des matériaux en électrochimie est une question de confiance
- L'architecture de l'invisibilité : déconstruction de la cellule "tout quartz"
- L'art de la résistance : Pourquoi votre cellule électrolytique a besoin d'espace pour respirer




















