L'Illusion de la Simplicité
En laboratoire, nous nous focalisons souvent sur la complexité de l'électrolyte. Nous mesurons les concentrations au microgramme. Nous sommes obsédés par les gradients de température. Nous traitons la solution chimique comme une recette délicate qui nécessite la touche d'un chef.
Pourtant, nous négligeons fréquemment la "plomberie" de l'expérience : les fils.
Connecter une cellule électrolytique semble trivial. Fil rouge ici, fil noir là. Cela ressemble à brancher un grille-pain – est-ce que ça a vraiment de l'importance dans quel sens ?
En électrolyse, cela importe plus que tout le reste.
La polarité des électrodes n'est pas simplement un détail de connexion. C'est le centre de commandement et de contrôle de votre expérience. C'est la différence entre créer un chef-d'œuvre et dissoudre votre équipement.
La Pompe à Électrons
Pour comprendre la polarité, vous devez cesser de considérer l'alimentation comme une batterie et commencer à la considérer comme une pompe.
Contrairement à une cellule galvanique, où la chimie crée de l'électricité, une cellule électrolytique utilise l'électricité pour forcer la chimie à se produire contre sa volonté. La réaction est non spontanée. Elle a besoin d'une impulsion.
L'alimentation fournit cette impulsion, mais strictement dans une seule direction :
- Elle tire les électrons d'un côté.
- Elle pousse les électrons de l'autre.
Ce flux dicte l'identité de vos électrodes. Les étiquettes "Anode" et "Cathode" ne sont pas des emplacements géographiques dans votre bécher ; ce sont des rôles fonctionnels définis entièrement par ce flux.
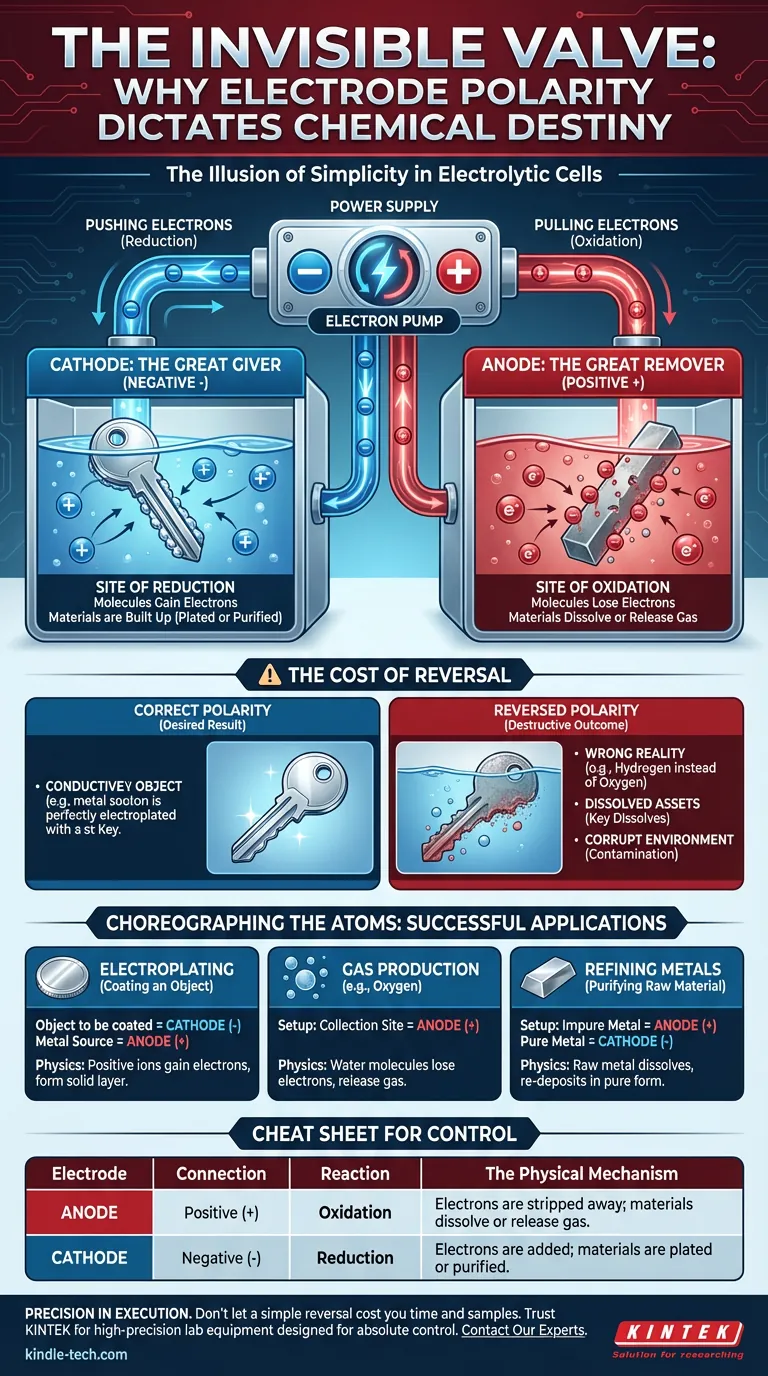
L'Anode : Le Grand Dissolveur
Connectée à la borne Positive (+), l'anode est l'endroit où l'alimentation arrache les électrons aux espèces chimiques.
C'est le site de l'Oxydation. Les molécules proches de cette surface perdent des électrons. Elles sont dépouillées.
La Cathode : Le Grand Donneur
Connectée à la borne Négative (-), la cathode est l'endroit où l'alimentation force un excès d'électrons sur la surface.
C'est le site de la Réduction. Les molécules proches de cette surface gagnent des électrons. Elles sont construites.
Le Coût de l'Inversion
Que se passe-t-il lorsque vous inversez les fils ?
Dans de nombreux domaines de la vie, une connexion inversée signifie simplement que l'appareil ne s'allume pas. En électrolyse, les conséquences sont beaucoup plus actives – et souvent destructrices.
Lorsque vous inversez la polarité, vous ne mettez pas la réaction en pause. Vous inversez l'univers de votre bécher.
1. Vous fabriquez la mauvaise réalité
Si vous aviez l'intention de produire de l'oxygène mais que vous avez inversé les bornes, vous pourriez produire de l'hydrogène à la place. La logique chimique est parfaitement inversée. Vous n'obtenez pas "aucun résultat" ; vous obtenez "l'anti-résultat".
2. Vous dissolvez vos biens
Imaginez que vous plaquiez une clé vintage avec du cuivre. Vous voulez que les ions de cuivre se déposent sur la clé.
Si vous inversez la polarité, la clé devient l'anode (le site d'oxydation). Au lieu de recevoir une couche brillante de cuivre, la clé elle-même commence à se dissoudre dans la solution. Vous ne conservez pas l'objet ; vous le détruisez activement.
3. Vous corrompez l'environnement
Forcer l'oxydation sur une électrode non conçue pour cela entraîne une corrosion rapide. Cela ne ruine pas seulement l'électrode ; cela inonde votre électrolyte soigneusement préparé de contaminants, invalidant toute l'expérience.
Chorégraphier les Atomes
Une électrolyse réussie exige que vous soyez un architecte du mouvement atomique. Vous devez décider où vont les électrons avant d'appuyer sur l'interrupteur.
Utilisez cette logique pour assigner votre polarité :
-
L'Objectif : Galvanoplastie
- La Configuration : L'objet à recouvrir doit être la Cathode (-).
- La Physique : Vous avez besoin que les ions métalliques positifs gagnent des électrons et se transforment en métal solide à la surface de l'objet.
-
L'Objectif : Production de Gaz (par ex. Oxygène)
- La Configuration : Le site de collecte doit être l'Anode (+).
- La Physique : Les molécules d'eau doivent perdre des électrons (s'oxyder) pour libérer du gaz oxygène.
-
L'Objectif : Raffinage des Métaux
- La Configuration : Le métal impur doit être l'Anode (+).
- La Physique : Le métal brut doit se dissoudre (s'oxyder) dans la solution pour pouvoir être redéposé sous forme pure ailleurs.
Le Résumé du Contrôle
Voici la feuille de triche pour contrôler votre destin chimique :
| Électrode | Connexion | Réaction | Le Mécanisme Physique |
|---|---|---|---|
| Anode | Positive (+) | Oxydation | Les électrons sont arrachés ; les matériaux se dissolvent ou libèrent du gaz. |
| Cathode | Négative (-) | Réduction | Les électrons sont ajoutés ; les matériaux sont plaqués ou purifiés. |
La Précision dans l'Exécution
Il y a une certaine romance dans l'électrolyse. Vous pénétrez dans le monde moléculaire et forcez les atomes à marcher dans la direction que vous choisissez.
Mais ce contrôle repose sur l'intégrité de votre installation. Même la meilleure compréhension théorique échoue si l'équipement est peu fiable ou si les connexions sont mauvaises.
Chez KINTEK, nous comprenons que la frontière entre une percée et une expérience ratée est souvent aussi mince qu'une connexion de fil. Nous sommes spécialisés dans les équipements de laboratoire et les consommables de haute précision conçus pour vous donner un contrôle absolu sur vos processus électrochimiques.
Que vous raffiniez des métaux précieux ou que vous meniez des recherches sensibles, nos outils garantissent que lorsque vous commandez aux électrons de circuler, ils vont exactement là où ils sont censés aller.
Ne laissez pas une simple inversion vous coûter du temps et des échantillons. Contactez Nos Experts
Guide Visuel
Produits associés
- Cellule électrolytique en PTFE Cellule électrochimique scellée et non scellée résistante à la corrosion
- Cellule électrochimique électrolytique super scellée
- Cellule électrochimique électrolytique à cinq ports
- Cellule électrolytique de type H Triple Cellule électrochimique
- Cellule de diffusion de gaz électrolytique électrochimique à flux liquide
Articles associés
- Le partenaire silencieux : pourquoi le choix des matériaux en électrochimie est une question de confiance
- Conception et normes des cellules électrolytiques
- L'Architecture de la Certitude : Maîtriser le Contrôle dans les Cellules Électrolytiques Multifonctionnelles
- L'art du non-spontané : la précision dans les circuits électrolytiques
- L'art de la résistance : Pourquoi votre cellule électrolytique a besoin d'espace pour respirer




















