À la base, une électrode argent/chlorure d'argent (Ag/AgCl) conçue pour les solutions neutres est une électrode de référence qui fournit un potentiel stable et constant. Sa caractéristique clé est l'utilisation d'un fil d'argent recouvert de chlorure d'argent, qui est immergé dans une solution saturée de chlorure de potassium (KCl) pour maintenir une concentration fixe d'ions chlorure.
Le but d'une électrode Ag/AgCl n'est pas de réagir avec votre échantillon, mais de fournir un point de référence de tension inébranlable et connu. Sa conception, centrée sur une solution saturée de KCl, assure cette stabilité, qui est le fondement de toute mesure électrochimique précise.

Les composants fondamentaux et leur rôle
Pour comprendre les performances de l'électrode, vous devez d'abord comprendre sa construction. Chaque partie a une fonction précise pour garantir un potentiel stable.
L'élément argent/chlorure d'argent
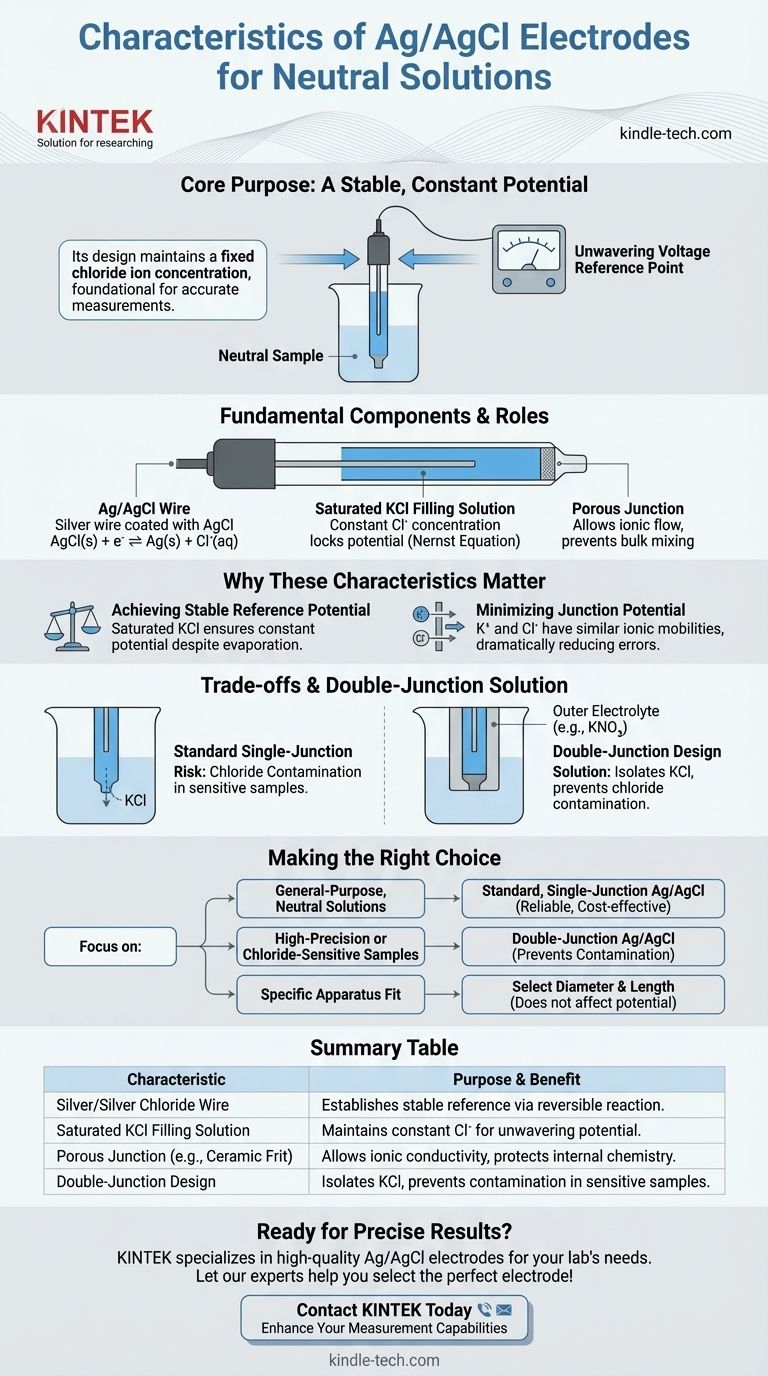
Le cœur de l'électrode est un fil d'argent pur recouvert d'une couche de chlorure d'argent (AgCl). C'est là que se produit la réaction électrochimique fondamentale.
Le potentiel est établi par l'équilibre entre l'argent/chlorure d'argent solide et les ions chlorure (Cl⁻) dans la solution de remplissage : AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq).
La solution de remplissage de KCl saturé
Pour une utilisation dans des solutions neutres, l'électrode est remplie d'une solution saturée de chlorure de potassium (KCl). C'est la caractéristique la plus critique pour la stabilité.
Parce que la solution est saturée, la concentration d'ions chlorure est maintenue constante à un niveau connu et élevé. Selon l'équation de Nernst, cette concentration constante de chlorure fixe le potentiel de l'électrode, ce qui en fait une référence fiable.
La jonction poreuse
Une fritte poreuse, généralement en céramique ou en quartz, sépare la solution de remplissage interne de la solution d'échantillon externe.
Cette jonction permet aux ions de circuler entre l'électrode et l'échantillon, complétant le circuit électrique. Cependant, elle empêche le mélange en vrac des deux solutions, protégeant la chimie interne de l'électrode de référence.
Pourquoi ces caractéristiques sont importantes pour votre mesure
Les composants spécifiques d'une électrode Ag/AgCl sont délibérément choisis pour résoudre les problèmes courants en électrochimie, garantissant que vos résultats sont précis et reproductibles.
Obtenir un potentiel de référence stable
Le but entier d'une électrode de référence est d'avoir un potentiel qui ne change pas pendant votre expérience.
En utilisant une solution saturée de KCl, la concentration de chlorure reste constante même si une petite quantité d'eau s'évapore ou diffuse. Cette concentration constante assure un potentiel de référence solide comme un roc par rapport auquel vous pouvez mesurer votre électrode de travail.
Minimiser le potentiel de jonction
Une source majeure d'erreur dans les mesures électrochimiques est le potentiel de jonction liquide. Il s'agit d'une petite tension qui se développe à l'interface entre la solution de remplissage et votre solution d'échantillon en raison des différences de vitesses de diffusion ionique.
Le chlorure de potassium (KCl) est utilisé spécifiquement parce que les mobilités ioniques de l'ion potassium (K⁺) et de l'ion chlorure (Cl⁻) sont presque identiques. Cette similitude les fait diffuser à travers la jonction à peu près à la même vitesse, ce qui minimise considérablement le potentiel de jonction et améliore la précision des mesures.
Comprendre les compromis et les variations
Bien que l'électrode Ag/AgCl standard soit un outil de travail, elle n'est pas universellement parfaite. Comprendre ses limites est essentiel pour éviter les erreurs de mesure.
Le risque de contamination par le chlorure
Le principal compromis est qu'une petite quantité de la solution de remplissage de KCl s'échappera inévitablement de la jonction poreuse dans votre échantillon.
Pour la plupart des solutions neutres, ce n'est pas un problème. Cependant, si votre expérience est sensible aux ions chlorure — par exemple, si vous mesurez de faibles concentrations de chlorure ou travaillez avec des échantillons qui précipitent avec le chlorure (comme le nitrate d'argent) — cette fuite introduira des erreurs significatives.
Le rôle de l'électrode à double jonction
Pour résoudre le problème de la contamination par le chlorure, une électrode à double jonction est utilisée. Cette conception comprend une deuxième chambre externe qui isole la solution de KCl de l'échantillon.
Cette chambre externe peut être remplie d'un électrolyte non interférant, tel que le nitrate de potassium (KNO₃) ou le sulfate de sodium (Na₂SO₄). Elle fournit le pont ionique à l'échantillon sans introduire d'ions chlorure, préservant l'intégrité de votre échantillon.
Considérations de conception physique
Les électrodes sont disponibles en différents diamètres (par exemple, 4 mm, 6 mm, 10 mm) et longueurs. Ces caractéristiques physiques n'affectent pas le potentiel de l'électrode mais sont choisies en fonction des contraintes de votre cellule électrochimique, du volume de votre échantillon et de la durabilité requise.
Faire le bon choix pour votre objectif
Le choix de l'électrode correcte est une étape critique pour l'acquisition de données fiables. Votre choix dépend directement de la nature chimique de votre échantillon.
- Si votre objectif principal est des mesures à usage général dans des solutions neutres : Une électrode Ag/AgCl standard à jonction simple avec KCl saturé est le choix fiable et économique.
- Si votre objectif principal est des mesures de haute précision ou des échantillons sensibles au chlorure : Vous devez utiliser une électrode Ag/AgCl à double jonction pour éviter la contamination de l'échantillon et garantir la précision des données.
- Si votre objectif principal est de s'adapter à un appareil spécifique : Sélectionnez le diamètre et la longueur de l'électrode qui correspondent physiquement à la conception de votre cellule électrochimique.
Comprendre comment ces composants créent une référence stable est la clé pour générer des résultats électrochimiques fiables et reproductibles.
Tableau récapitulatif :
| Caractéristique | Objectif et avantage |
|---|---|
| Fil argent/chlorure d'argent | Élément central ; établit un potentiel de référence stable via une réaction réversible. |
| Solution de remplissage de KCl saturé | Maintient une concentration constante d'ions chlorure pour un potentiel inébranlable, même avec une évaporation mineure. |
| Jonction poreuse (par exemple, fritte céramique) | Permet la conductivité ionique tout en empêchant le mélange en vrac des solutions, protégeant la chimie interne. |
| Conception à double jonction (variation) | Isole le KCl de l'échantillon en utilisant un électrolyte intermédiaire pour prévenir la contamination par le chlorure dans les échantillons sensibles. |
Prêt à obtenir des résultats électrochimiques précis et fiables ?
La bonne électrode de référence est fondamentale pour le succès de votre laboratoire. KINTEK est spécialisé dans les équipements de laboratoire de haute qualité, y compris une gamme d'électrodes Ag/AgCl conçues pour la précision et la durabilité dans les solutions neutres. Que vous ayez besoin d'un modèle standard à jonction simple pour un usage général ou d'une électrode à double jonction pour des applications sensibles au chlorure, nous avons la solution pour répondre à vos besoins spécifiques en laboratoire.
Laissez nos experts vous aider à choisir l'électrode parfaite pour vos expériences. Contactez KINTEK dès aujourd'hui pour discuter de vos exigences et améliorer vos capacités de mesure !
Guide Visuel
Produits associés
- Électrode de référence au calomel, chlorure d'argent, sulfate de mercure pour usage en laboratoire
- Électrode de référence au sulfate de cuivre pour usage en laboratoire
- Électrode à disque d'or
- Électrode Électrochimique en Feuille d'Or Électrode en Or
- Électrode électrochimique en graphite, tige et plaque de graphite
Les gens demandent aussi
- Quelle électrode est utilisée comme électrode de référence pour la mesure des potentiels de demi-pile ? Comprendre l'étalon universel
- Comment la sélection des électrodes de référence, telles que Ag/AgCl ou Hg/HgO, est-elle corrélée au pH de l'électrolyte dans les essais de réaction d'évolution d'hydrogène (HER) ?
- Qu'est-ce que l'électrode de référence en potentiométrie ? La clé de mesures stables et précises
- Pourquoi la sélection d'une électrode de référence de haute qualité est-elle essentielle en synthèse électrochimique ? | KINTEK
- Quelle électrode est utilisée comme référence de masse ? Maîtrisez la clé des mesures électrochimiques précises










