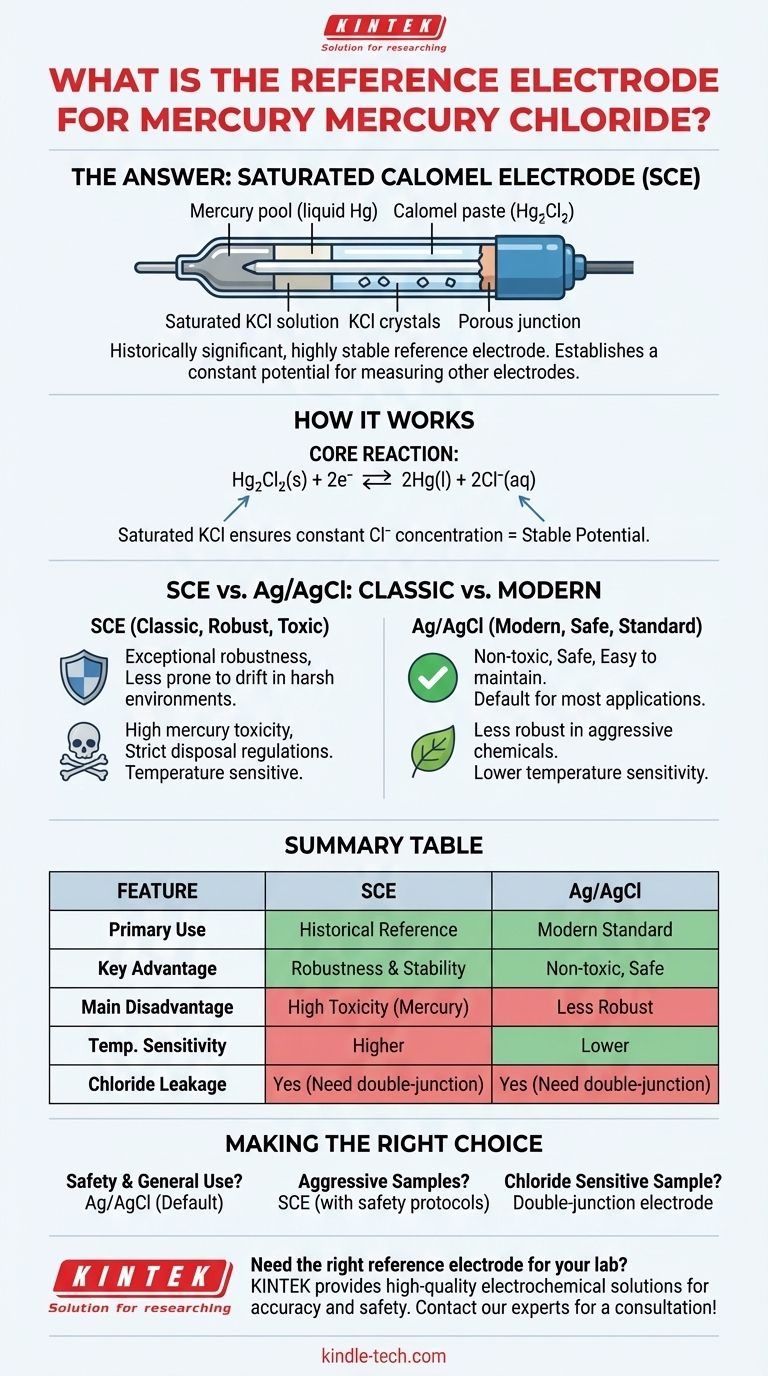
L'électrode de référence basée sur le mercure et le chlorure de mercure(I) est l'électrode au calomel saturé (ECS). C'est une électrode historiquement significative et très stable qui établit un potentiel constant, par rapport auquel le potentiel d'autres électrodes peut être mesuré dans une cellule électrochimique. Sa construction implique une pâte de mercure élémentaire et de chlorure de mercure(I) (calomel) en contact avec une solution aqueuse saturée de chlorure de potassium (KCl).
L'électrode au calomel saturé (ECS) est une électrode de référence robuste et très stable, mais son utilisation a été largement supplantée par l'électrode Argent/Chlorure d'Argent (Ag/AgCl) en raison de la toxicité importante et des problèmes d'élimination associés à ses composants à base de mercure.

Comment l'électrode au calomel établit-elle un potentiel stable ?
Le seul but d'une électrode de référence est de fournir un potentiel stable et connu qui ne change pas pendant une expérience. L'ECS y parvient grâce à un équilibre chimique soigneusement équilibré.
La réaction électrochimique centrale
Le potentiel de l'ECS est régi par une demi-réaction réversible impliquant le mercure et son sel de chlorure.
Hg₂Cl₂(s) + 2e⁻ ⇌ 2Hg(l) + 2Cl⁻(aq)
Le potentiel de cette réaction dépend de la concentration (plus précisément, de l'activité) des ions chlorure (Cl⁻) dans la solution.
Le rôle du KCl saturé
Pour garantir que le potentiel est constant, la concentration en ions chlorure ne doit pas changer. L'ECS y parvient en utilisant une solution saturée de chlorure de potassium (KCl) comme électrolyte interne.
Tant qu'il y a des cristaux de KCl non dissous présents, la solution reste saturée, fixant la concentration en ions chlorure à une valeur constante. Cela rend le potentiel de l'électrode stable et reproductible.
ECS vs Ag/AgCl : Le classique et le moderne
Bien que l'ECS ait été un cheval de bataille pendant des décennies, l'électrode Argent/Chlorure d'Argent (Ag/AgCl) est maintenant la référence la plus courante dans les laboratoires modernes.
L'essor de l'électrode Argent/Chlorure d'Argent
Le principal moteur de l'abandon de l'ECS est la sécurité. Le mercure est une neurotoxine puissante soumise à des réglementations strictes en matière de manipulation et d'élimination.
L'électrode Ag/AgCl est non toxique, moins chère, et plus facile à fabriquer et à entretenir, ce qui en fait le choix préféré pour la plupart des applications à usage général.
Performance et stabilité
Les deux électrodes offrent une excellente stabilité de potentiel. L'ECS a la réputation d'être exceptionnellement robuste et moins sujette à la dérive dans certains environnements chimiques industriels ou complexes.
Cependant, le potentiel d'une ECS est plus sensible aux changements de température que celui d'une électrode Ag/AgCl. Cela est dû au fait que la solubilité du KCl, qui dicte la concentration en chlorure, varie considérablement avec la température.
Comprendre les compromis
Le choix d'une électrode de référence implique de trouver un équilibre entre les exigences de performance et les considérations pratiques et de sécurité.
Avantage : Robustesse inégalée
L'ECS est réputée pour sa durabilité. Elle peut fonctionner de manière fiable dans des solutions qui pourraient « empoisonner » ou endommager une électrode Ag/AgCl, telles que celles contenant des sulfures, des bromures ou des protéines qui réagissent avec l'argent.
Inconvénient : Le problème du mercure
C'est le plus grand inconvénient de l'ECS. La toxicité du mercure en fait une responsabilité importante en matière de santé et d'environnement. La rupture accidentelle et l'élimination en fin de vie nécessitent des procédures spécialisées et coûteuses.
Inconvénient : Fuite de chlorure
Comme la plupart des électrodes de référence, l'ECS se connecte à la solution d'échantillon via une fritte poreuse ou une jonction. Cette jonction peut lentement laisser s'échapper du KCl de la solution interne de l'électrode dans votre échantillon.
Cela peut poser problème si votre expérience est sensible aux ions chlorure. Dans de tels cas, une électrode à « double jonction » est nécessaire pour isoler l'échantillon du KCl.
Faire le bon choix pour votre objectif
La meilleure électrode de référence est celle qui répond aux exigences spécifiques de votre mesure tout en respectant les normes de sécurité modernes.
- Si votre objectif principal est la sécurité et l'utilisation générale en laboratoire : L'électrode Argent/Chlorure d'Argent (Ag/AgCl) est le choix par défaut et correct pour presque toutes les applications standard.
- Si votre objectif principal est la robustesse dans des échantillons agressifs : L'électrode au calomel saturé (ECS) peut être envisagée, mais seulement lorsque sa stabilité unique est essentielle et que des protocoles de sécurité stricts concernant le mercure sont en place.
- Si votre échantillon ne doit pas être contaminé par du chlorure : Vous devez utiliser une électrode de référence à double jonction, qui place un deuxième électrolyte non interférant entre l'élément de référence et l'échantillon.
Comprendre ces compromis fondamentaux vous permet de choisir le bon outil pour une analyse électrochimique fiable et sûre.
Tableau récapitulatif :
| Caractéristique | Électrode au calomel saturé (ECS) | Argent/Chlorure d'Argent (Ag/AgCl) |
|---|---|---|
| Utilisation principale | Électrode de référence historique | Électrode de référence moderne et standard |
| Avantage clé | Robustesse et stabilité exceptionnelles | Non toxique, sûre et facile à entretenir |
| Inconvénient majeur | Toxicité élevée du mercure | Moins robuste dans certains produits chimiques agressifs |
| Sensibilité à la température | Sensibilité plus élevée | Sensibilité plus faible |
| Fuite de chlorure | Oui (double jonction nécessaire si problématique) | Oui (double jonction nécessaire si problématique) |
Besoin de l'électrode de référence adaptée à votre application de laboratoire spécifique ?
Le choix entre une ECS traditionnelle et une électrode Ag/AgCl moderne dépend de vos exigences en matière de sécurité, de robustesse et de compatibilité avec l'échantillon. KINTEK se spécialise dans la fourniture d'équipements et de consommables de laboratoire de haute qualité, y compris une gamme complète de cellules électrochimiques et d'électrodes de référence, pour garantir que vos expériences sont à la fois précises et sûres.
Laissez nos experts vous aider à sélectionner l'équipement parfait pour vos besoins. Contactez KINTEK dès aujourd'hui pour une consultation !
Guide Visuel
Produits associés
- Électrode de référence au calomel, chlorure d'argent, sulfate de mercure pour usage en laboratoire
- Électrode de référence au sulfate de cuivre pour usage en laboratoire
- Électrode à disque d'or
- Électrode en feuille de platine pour applications de laboratoire et industrielles
- Électrode auxiliaire en platine pour usage en laboratoire
Les gens demandent aussi
- Quelle est la fonction d'une électrode de référence ? Maîtriser la précision dans la reconstruction de réacteurs à trois électrodes
- Quel type d'électrode peut être utilisé comme point de référence ? Sélectionnez la bonne pour des mesures précises
- Pourquoi la sélection d'une électrode de référence de haute qualité est-elle essentielle en synthèse électrochimique ? | KINTEK
- Qu'est-ce que l'électrode de référence en potentiométrie ? La clé de mesures stables et précises
- Comment la sélection des électrodes de référence, telles que Ag/AgCl ou Hg/HgO, est-elle corrélée au pH de l'électrolyte dans les essais de réaction d'évolution d'hydrogène (HER) ?






