À la base, l'électrolyse pour le traitement de l'eau est une méthode électrochimique avancée qui utilise un courant électrique continu pour initier des réactions chimiques et purifier l'eau. Ce processus implique le passage de l'électricité à travers des électrodes immergées dans l'eau, ce qui force les composés et les contaminants à se décomposer et à se séparer au niveau moléculaire. C'est une technique puissante pour gérer les défis complexes des eaux usées.
Le principe fondamental de l'électrolyse ne consiste pas à filtrer physiquement l'eau, mais à en modifier fondamentalement la composition chimique. En introduisant un courant électrique, vous forcez des réactions chimiques non spontanées à se produire, démantelant efficacement les polluants que d'autres méthodes ne peuvent pas facilement éliminer.

Comment fonctionne le processus électrochimique
Pour comprendre comment l'électrolyse traite l'eau, vous devez d'abord comprendre les composants et les réactions de base impliqués. Le système est alimenté par une source d'énergie externe qui crée un environnement puissant pour le changement chimique.
Le rôle de l'électricité et des électrodes
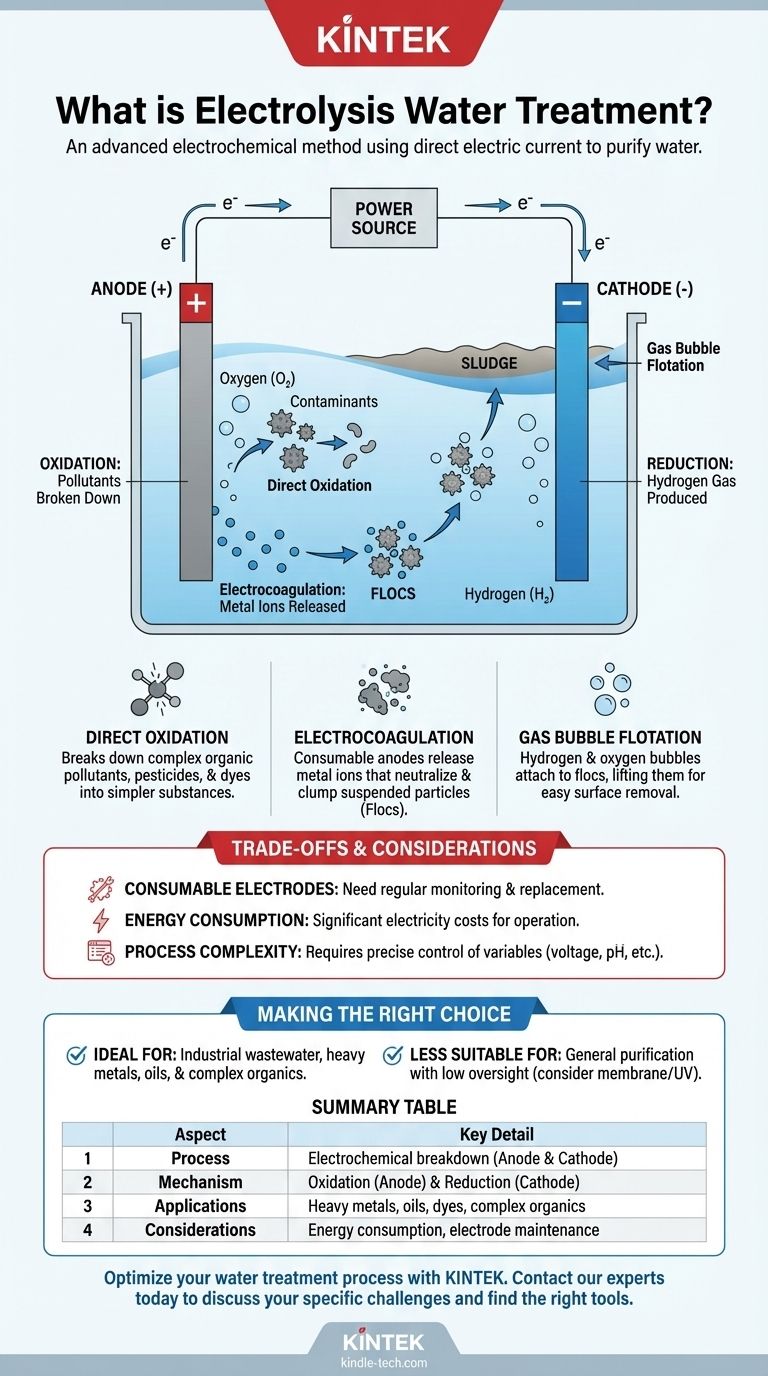
Le processus commence lorsqu'une tension externe est appliquée à deux électrodes — une anode chargée positivement et une cathode chargée négativement — qui sont placées dans l'eau. Ces électrodes sont souvent fabriquées à partir de matériaux "consommables" comme le fer ou l'aluminium, qui participent activement au processus de traitement en fournissant des ions dans l'eau.
La réaction à la cathode (réduction)
La cathode chargée négativement attire les ions chargés positivement (cations) de l'eau, tels que les ions hydrogène (H+). À la surface de la cathode, ces ions gagnent des électrons dans un processus appelé réduction. Cette réaction produit du gaz d'hydrogène pur (H₂), qui remonte à la surface sous forme de bulles.
La réaction à l'anode (oxydation)
Simultanément, l'anode chargée positivement attire les ions chargés négativement (anions), tels que les ions hydroxyde (OH-). Ici, les ions cèdent leurs électrons dans un processus appelé oxydation. Cette réaction produit principalement de l'oxygène gazeux (O₂) et c'est également là que de nombreux polluants sont décomposés.
L'objectif principal : l'élimination des contaminants
Alors que l'électrolyse de l'eau pure produit simplement de l'hydrogène et de l'oxygène, son application dans le traitement des eaux usées est bien plus sophistiquée. Les réactions sont conçues pour attaquer et éliminer un large éventail de contaminants.
Oxydation directe des polluants
L'environnement oxydant puissant créé à l'anode peut directement décomposer les polluants organiques complexes, les pesticides et les colorants. Ce processus brise efficacement leur structure moléculaire, les convertissant en substances plus simples et moins nocives comme le dioxyde de carbone et l'eau.
Électrocoagulation
Lorsque des électrodes consommables (comme le fer ou l'aluminium) sont utilisées, l'anode libère des ions métalliques dans l'eau. Ces ions agissent comme de puissants coagulants, neutralisant la charge des particules en suspension et les faisant s'agglomérer en masses plus grandes appelées "flocs", qui sont beaucoup plus faciles à éliminer.
Flottation par bulles de gaz
Les bulles de gaz d'hydrogène et d'oxygène produites aux électrodes s'attachent aux flocs nouvellement formés. Cela augmente leur flottabilité, les faisant remonter à la surface où ils peuvent être facilement écrémés sous forme de boues.
Comprendre les compromis et les considérations
L'électrolyse est une technologie puissante, mais ce n'est pas une solution universelle. Comprendre ses exigences opérationnelles est essentiel pour une mise en œuvre réussie.
Électrodes consommables
Comme leur nom l'indique, les électrodes consommables sont sacrifiées pendant le processus. Elles se corrodent et se dissolvent avec le temps, ce qui signifie qu'elles doivent être surveillées et remplacées périodiquement. Cela introduit une exigence de maintenance récurrente et un coût matériel.
Consommation d'énergie
L'ensemble du processus est alimenté par l'électricité. La "tension externe" requise se traduit directement par des coûts énergétiques, qui peuvent être importants, en particulier pour les opérations de traitement à grande échelle. L'efficacité du système est un facteur clé de sa viabilité économique.
Complexité du processus
Une électrolyse efficace nécessite un contrôle précis de multiples variables. Des facteurs tels que la tension, la densité de courant, le niveau de pH de l'eau et le matériau des électrodes doivent être gérés avec soin pour optimiser l'élimination des contaminants et prévenir les sous-produits indésirables. C'est un processus techniquement exigeant, et non un système simple "plug-and-play".
Faire le bon choix pour votre objectif
Le choix de la bonne méthode de traitement de l'eau dépend entièrement des contaminants spécifiques et de vos priorités opérationnelles.
- Si votre objectif principal est de traiter les eaux usées industrielles contenant des métaux lourds, des huiles ou des composés organiques complexes : L'électrolyse est une solution particulièrement puissante qui peut décomposer les contaminants que d'autres systèmes ne peuvent pas gérer.
- Si votre objectif principal est la purification générale de l'eau avec une faible surveillance opérationnelle : Les besoins en énergie et la nécessité de remplacer les électrodes peuvent rendre des méthodes plus simples comme la filtration membranaire ou le traitement UV plus appropriées.
- Si votre objectif principal est un résultat de haute pureté avec un minimum d'additifs chimiques : L'électrolyse offre un avantage en utilisant l'électricité et les électrodes elles-mêmes comme principaux agents de traitement, réduisant ainsi le besoin d'ajouter des produits chimiques en vrac.
En fin de compte, comprendre les principes électrochimiques derrière l'électrolyse vous permet de déterminer si sa nature puissante, mais exigeante, convient à votre défi spécifique de traitement de l'eau.
Tableau récapitulatif :
| Aspect | Détail clé |
|---|---|
| Processus | Décomposition électrochimique à l'aide d'une anode et d'une cathode. |
| Mécanisme primaire | Oxydation à l'anode et réduction à la cathode. |
| Applications clés | Élimination des métaux lourds, des huiles, des colorants et des composés organiques complexes. |
| Principales considérations | Consommation d'énergie et maintenance des électrodes consommables. |
Optimisez votre processus de traitement de l'eau avec KINTEK.
L'électrolyse est une solution puissante mais techniquement exigeante. KINTEK est spécialisé dans la fourniture d'équipements de laboratoire et de consommables de haute qualité nécessaires pour un contrôle précis et une mise en œuvre efficace des méthodes de traitement électrochimique de l'eau.
Que vous recherchiez des matériaux d'électrodes ou que vous mettiez à l'échelle un système de traitement, notre expertise vous assure de disposer des bons outils pour réussir.
Contactez nos experts dès aujourd'hui pour discuter de vos défis spécifiques en matière de purification de l'eau et découvrir comment KINTEK peut vous aider à atteindre vos objectifs.
Guide Visuel
Produits associés
- Cellules d'électrolyse PEM personnalisables pour diverses applications de recherche
- Bain-marie électrolytique à cinq ports à double couche
- Cellule électrolytique électrochimique à bain-marie double couche
- Bain-marie électrochimique multifonctionnel pour cellule électrolytique, simple ou double couche
- Cellule électrochimique électrolytique à bain-marie optique
Les gens demandent aussi
- Qu'est-ce qu'une cellule électrolytique ? Un guide pour piloter les réactions chimiques avec l'électricité
- Quelle est la procédure appropriée pour arrêter l'expérience après électrolyse ? Un guide de sécurité étape par étape
- Quelle est la procédure de nettoyage immédiat après utilisation d'une cellule d'électrolyse ? Prévenir l'accumulation de résidus pour des résultats précis
- Quelles sont les configurations d'ouverture pour les versions non scellée et scellée de la cellule d'électrolyse ? Optimisez votre montage électrochimique
- Quelles sont les précautions à prendre lors du chauffage ou de la stérilisation d'une cellule d'électrolyse ? Éviter d'endommager les composants sensibles



















