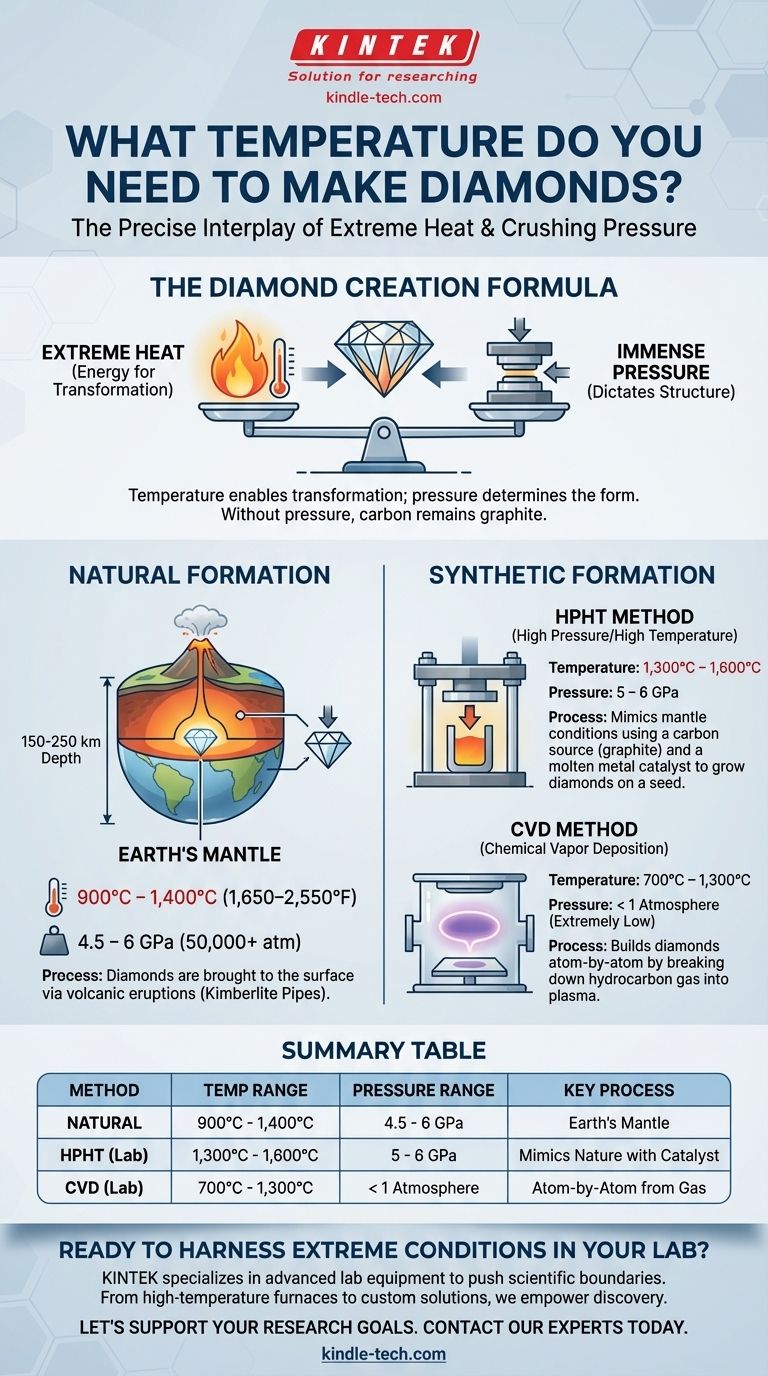
Pour créer un diamant, il faut des températures extrêmement élevées, mais le chiffre exact dépend entièrement de la pression que vous pouvez appliquer. Dans la nature, les diamants se forment à des températures comprises entre 900°C et 1 400°C (1 650–2 550°F), tandis que la méthode la plus courante de culture en laboratoire, HPHT, utilise des températures similaires d'environ 1 300–1 600°C. Cependant, la température n'est que la moitié de l'équation ; sans une pression immense, vous ne ferez que du graphite.
La création d'un diamant n'est pas seulement fonction de la température, mais d'une interaction précise entre une chaleur extrême et une pression écrasante. Comprendre cette relation est la clé pour comprendre comment le carbone peut se transformer de sa forme commune, le graphite, en l'un des matériaux les plus durs et les plus précieux sur Terre.

Les deux voies de la création de diamants
Les diamants sont simplement des atomes de carbone arrangés dans une structure cristalline spécifique et très dense. Pour forcer ces atomes à adopter cette formation, la nature et la science utilisent deux méthodes principales, chacune avec une recette distincte de chaleur et de pression.
Formation naturelle : Le manteau terrestre
Les diamants naturels se forment profondément dans le manteau supérieur de la Terre, à environ 150 à 250 kilomètres sous la surface.
À ces profondeurs, les conditions nécessaires sont réunies :
- Température : Environ 900°C à 1 400°C (1 650–2 550°F).
- Pression : Une immense 4,5 à 6 gigapascals (GPa). C'est plus de 50 000 fois la pression atmosphérique au niveau de la mer.
Ces diamants sont ensuite transportés à la surface sur des millions d'années par des éruptions volcaniques profondes, qui créent les cheminées de kimberlite où la plupart des diamants sont extraits aujourd'hui.
Formation synthétique : Le laboratoire
Les scientifiques ont développé deux techniques principales pour reproduire et même innover le processus de la nature.
La méthode HPHT (Haute Pression/Haute Température)
Cette méthode imite le plus fidèlement les conditions du manteau terrestre. Une source de carbone, comme le graphite, est placée dans une grande presse mécanique.
- Température : Un creuset chauffe le carbone à 1 300°C–1 600°C.
- Pression : La presse applique des pressions de 5 à 6 GPa.
Un catalyseur de métal en fusion est utilisé pour dissoudre le carbone, qui cristallise ensuite autour d'une minuscule "graine" de diamant pour former un diamant plus grand, de qualité gemme.
La méthode CVD (Dépôt Chimique en Phase Vapeur)
La CVD adopte une approche complètement différente, construisant un diamant atome par atome. Il s'agit moins de force brute que de contrôle chimique précis.
- Température : Un gaz hydrocarboné (comme le méthane) est chauffé dans une chambre à vide à 700°C–1 300°C.
- Pression : La pression est extrêmement basse, souvent inférieure à une atmosphère.
La chaleur décompose le gaz en un plasma d'ions carbone, qui se déposent ensuite sur une plaque de semence de diamant plate, faisant croître une couche de diamant atome par atome.
Comprendre les compromis : Pourquoi la pression est le facteur décisif
Beaucoup de gens se demandent pourquoi on ne peut pas simplement chauffer du carbone pour fabriquer un diamant. La réponse réside dans le diagramme de phase du carbone, qui représente la forme stable du carbone à différentes températures et pressions.
Graphite : L'état par défaut
Aux pressions que nous subissons dans la vie quotidienne (une atmosphère), la forme la plus stable du carbone est le graphite.
Même si vous chauffez du graphite à 3 000°C, il restera du graphite ou se sublimera en gaz. Il n'a tout simplement pas la force externe nécessaire pour contraindre ses atomes à adopter la structure de diamant étroitement tassée.
Diamant : L'état de haute pression
L'application d'une pression immense change les règles. La pression force physiquement les atomes de carbone à se rapprocher, rendant la structure de diamant plus dense plus stable que la structure de graphite moins dense.
Le rôle de la température est de fournir de l'énergie. Elle donne aux atomes de carbone la mobilité dont ils ont besoin pour rompre leurs liaisons existantes et se réorganiser en un nouveau réseau de diamant stable une fois la pression appliquée. Sans chaleur suffisante, le processus prendrait un temps impossibly long, même à la bonne pression.
Faire le bon choix pour votre objectif
Votre intérêt pour la température requise pour fabriquer des diamants provient probablement d'une curiosité plus profonde sur le processus lui-même. Comprendre votre objectif clarifiera quel processus est le plus pertinent pour vous.
- Si votre objectif principal est la géologie et les merveilles naturelles : Vous devriez vous concentrer sur les conditions du manteau terrestre — des températures autour de 1 000°C combinées à des pressions dépassant 5 GPa.
- Si votre objectif principal est la fabrication industrielle et la technologie : La méthode HPHT est la reproduction la plus directe de la nature, tandis que la méthode CVD représente une approche plus avancée et contrôlée qui permet différentes applications.
- Si votre objectif principal est le principe scientifique fondamental : La clé est que la température permet la transformation, mais la pression dicte ce que sera cette transformation.
En fin de compte, transformer du simple carbone en diamant est une puissante démonstration de la façon dont les conditions physiques définissent la structure de la matière.
Tableau récapitulatif :
| Méthode | Plage de température | Plage de pression | Processus clé |
|---|---|---|---|
| Formation naturelle | 900°C - 1 400°C | 4,5 - 6 GPa | Se forme dans le manteau terrestre |
| HPHT (Cultivé en laboratoire) | 1 300°C - 1 600°C | 5 - 6 GPa | Imite les conditions naturelles avec un catalyseur |
| CVD (Cultivé en laboratoire) | 700°C - 1 300°C | < 1 atmosphère | Construit le diamant atome par atome à partir de gaz |
Prêt à exploiter des conditions extrêmes dans votre laboratoire ?
Comprendre l'interaction précise de la chaleur et de la pression est fondamental pour la science des matériaux. Que votre recherche implique la synthèse à haute température, les tests de matériaux ou le développement de nouveaux matériaux à base de carbone, disposer du bon équipement est essentiel.
KINTEK est spécialisé dans l'équipement de laboratoire de pointe dont vous avez besoin pour repousser les limites de la science. Des fours à haute température capables d'atteindre plus de 1 600°C aux solutions personnalisées pour les environnements contrôlés, nous fournissons les outils qui favorisent la découverte et l'innovation dans les laboratoires du monde entier.
Discutons de la manière dont nous pouvons soutenir vos objectifs de recherche spécifiques. Contactez nos experts dès aujourd'hui pour trouver la solution parfaite pour les besoins de votre laboratoire.
Guide Visuel
Produits associés
- Réacteurs de laboratoire personnalisables à haute température et haute pression pour diverses applications scientifiques
- Réacteurs haute pression personnalisables pour des applications scientifiques et industrielles avancées
- Système de réacteur de dépôt chimique en phase vapeur par plasma micro-ondes MPCVD pour laboratoire et croissance de diamants
- Réacteur Autoclave Haute Pression en Acier Inoxydable pour Laboratoire
- Mini autoclave à réacteur haute pression en acier inoxydable pour laboratoire
Les gens demandent aussi
- Quel rôle joue un réacteur à haute température et haute pression dans la synthèse de CoFe2O4/Fe ? Débloquez la précision cœur-enveloppe
- Quel rôle jouent les réacteurs à haute température et haute pression (HTHP) dans la simulation de la corrosion des puits de pétrole et de gaz ?
- Pourquoi un réacteur de réaction de haute précision et haute température est-il essentiel à la synthèse des points quantiques ? Assurez des performances optimales
- Quel équipement est requis pour les réactions à haute pression et haute température ? Maîtrisez la chimie extrême en toute sécurité
- Comment la pression initiale d'oxygène affecte-t-elle l'oxydation humide des boues pharmaceutiques ? Maîtrisez votre profondeur d'oxydation



















