Le partenaire silencieux du laboratoire
En science, nous sommes obsédés par les variables que nous pouvons voir. Nous calibrons méticuleusement le potentiostat. Nous polissons l'électrode de travail jusqu'à ce qu'elle reflète notre propre épuisement. Nous purifions l'électrolyte au niveau des parties par milliard.
Mais souvent, nous ignorons la pièce où se déroule la réaction.
La cellule électrolytique est fréquemment traitée comme un seau passif, un simple récipient pour la "vraie" science. C'est une erreur. En électrochimie, le récipient est une condition limite. Il définit la couche de diffusion, dicte la distribution du courant et contrôle le rapport signal/bruit.
Choisir le bon volume et la bonne dimension de cellule n'est pas seulement une décision d'achat ; c'est la première étape de la conception expérimentale.
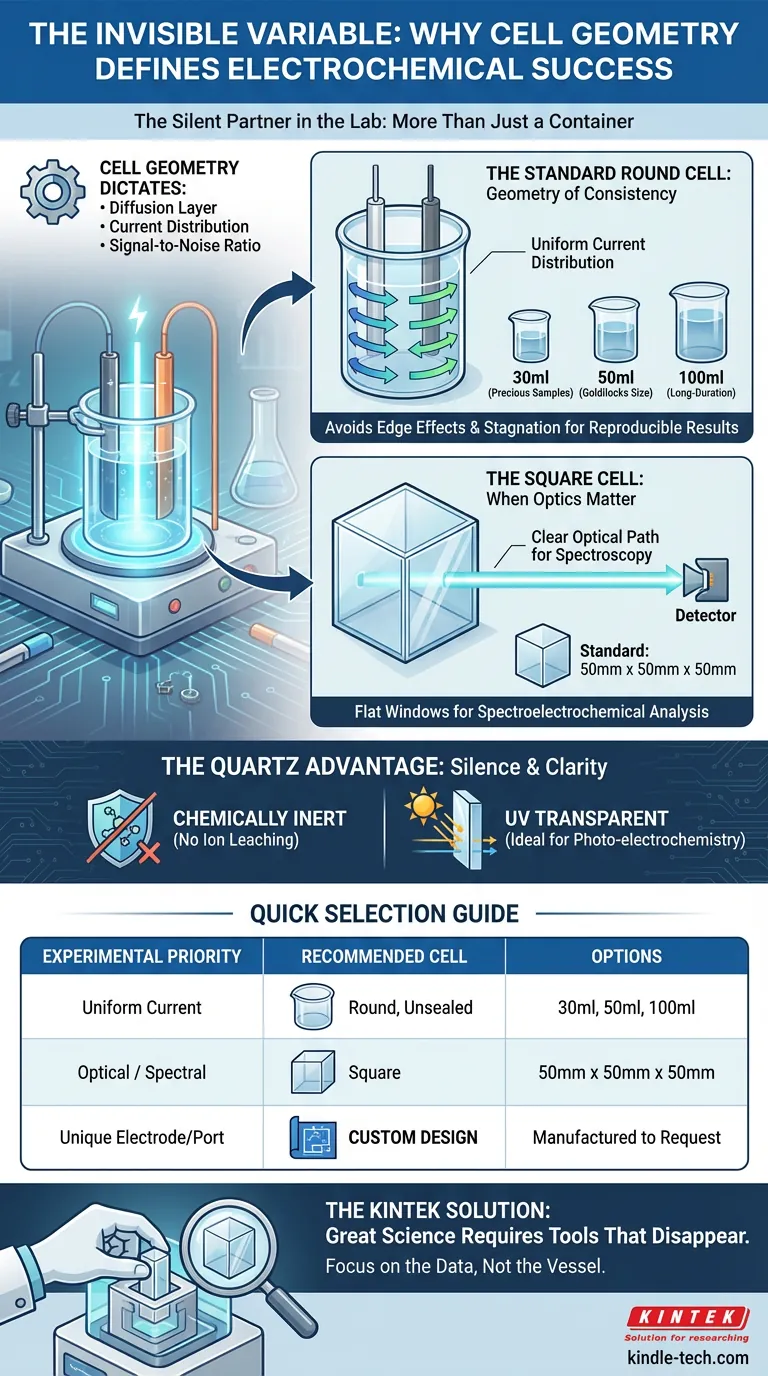
La cellule ronde standard : la géométrie de la cohérence
Pour la plupart des électrochimies à usage général, l'ennemi, ce sont les effets de bord.
Les coins aigus créent des zones de densité de courant inégale. Ils provoquent des points de stagnation dans l'électrolyte. C'est pourquoi l'outil standard de l'industrie est la cellule en quartz ronde non scellée.
La géométrie circulaire favorise une distribution uniforme du courant entre les électrodes de travail et auxiliaire. C'est le chemin de moindre résistance pour une voltammétrie cyclique reproductible.
Les volumes standard sont conçus en fonction de l'économie des réactifs et de la taille des électrodes :
- 30 ml : Idéal pour les échantillons précieux où la conservation de l'électrolyte est essentielle.
- 50 ml : La taille "juste ce qu'il faut" pour les configurations standard, équilibrant le volume et l'espace pour les électrodes.
- 100 ml : Nécessaire pour les électrodes plus grandes ou les expériences de longue durée où les changements de concentration doivent être minimisés.
La cellule carrée : quand l'optique compte
Parfois, la priorité passe de la cinétique électrochimique pure à l'observation.
Si vous effectuez des expériences spectroélectrochimiques, une cellule ronde devient un cauchemar de réfraction et de distorsion optique. Vous ne pouvez pas mesurer ce que vous ne pouvez pas voir clairement.
Pour résoudre ce problème, le standard passe à une cellule carrée en quartz.
- Dimension standard : 50 mm x 50 mm x 50 mm.
Cette géométrie offre les fenêtres optiques plates et parallèles requises pour l'analyse spectroscopique. Bien qu'elle introduise des coins (et donc une inhomogénéité potentielle du courant), elle offre la transparence nécessaire pour corréler le flux de courant avec les changements spectraux.
L'avantage du quartz
Pourquoi ces cellules standard sont-elles fabriquées exclusivement en quartz ?
Cela se résume à deux facteurs : le silence et la clarté.
Le verre est une soupe complexe d'oxydes qui peut relarguer des ions dans des conditions de pH extrêmes, introduisant du bruit dans vos données. Le quartz est chimiquement inerte. Il reste silencieux, garantissant que le courant que vous mesurez provient de votre analyte, pas de votre récipient.
De plus, le verre standard bloque la lumière UV. Le quartz la laisse passer. Pour toute expérience impliquant la photoélectrochimie, le quartz n'est pas un luxe ; c'est une nécessité.
Le piège du "taille unique"
Il y a un confort psychologique à acheter sur étagère. Cela semble sûr. Cela semble standard.
Mais la recherche opère à la limite du connu. Souvent, une cellule standard de 50 ml est trop grande pour un catalyseur synthétisé, ou une cellule carrée de 50 mm ne convient pas à un spectromètre spécialisé.
Forcer une expérience dans le mauvais récipient introduit des erreurs. Une cellule trop grande gaspille des réactifs coûteux. Une cellule trop petite encombre les électrodes, provoquant des courts-circuits ou un flux turbulent.
C'est là que la personnalisation devient le choix scientifique le plus rigoureux.
La plupart des fournisseurs, y compris KINTEK, peuvent fabriquer des cellules sur la base de dessins spécifiques. Si votre protocole nécessite une longueur de trajet unique, des emplacements de ports spécifiques ou des volumes non standard, le matériel doit s'adapter à la science, et non l'inverse.
Guide de sélection rapide
Pour simplifier le processus de décision, associez votre contrainte expérimentale principale au type de cellule :
| Priorité expérimentale | Type de cellule recommandé | Options standard |
|---|---|---|
| Distribution de courant uniforme | Ronde, non scellée | 30 ml, 50 ml, 100 ml |
| Analyse optique/spectrale | Carrée | 50 mm x 50 mm x 50 mm |
| Besoins uniques en électrodes/ports | Conception personnalisée | Fabriqué sur demande |
La solution
La grande science nécessite des outils qui disparaissent.
Lorsque votre équipement s'adapte parfaitement, vous arrêtez d'y penser. Vous arrêtez de vous soucier des fuites, de la distorsion optique ou du gaspillage de réactifs. Vous vous concentrez entièrement sur les données.
Chez KINTEK, nous fournissons l'équipement fondamental qui permet cette concentration. Que vous ayez besoin de la fiabilité de nos cellules en quartz standard ou d'une conception sur mesure pour une percée novatrice, nous veillons à ce que le récipient corresponde à la vision.
Contactez nos experts pour discuter si un volume standard ou une dimension personnalisée convient à votre prochaine expérience.
Guide Visuel
Produits associés
- Cellule électrochimique électrolytique en quartz pour expériences électrochimiques
- Cellule électrochimique électrolytique à cinq ports
- Cellule électrolytique en PTFE Cellule électrochimique scellée et non scellée résistante à la corrosion
- Cellule électrochimique électrolytique pour l'évaluation des revêtements
- Cellule électrochimique de corrosion plane
Articles associés
- L'Architecture de la Transparence : Maîtriser la Sécurité et la Précision en Électrolyse de Quartz
- Avantages des cellules électrochimiques pour le stockage d'énergie
- La géométrie du contrôle : pourquoi les millimètres comptent en électrochimie
- Cellules électrochimiques : Produire de l'électricité et piloter des réactions
- Le paradoxe de la transparence : maîtriser la précision fragile des cellules tout quartz




















