À la base, une atmosphère inerte est un environnement contrôlé où l'air normal et réactif a été intentionnellement remplacé par un gaz non réactif (ou "inerte"). Ceci est fait pour prévenir les réactions chimiques indésirables, telles que l'oxydation ou la combustion, qui se produiraient autrement en présence d'oxygène.
Le but fondamental d'une atmosphère inerte n'est pas le gaz lui-même, mais ce qu'il élimine : l'oxygène et l'humidité de l'air qui provoquent la dégradation, la détérioration, la rouille ou l'inflammation des matériaux.

Le problème : l'air réactif
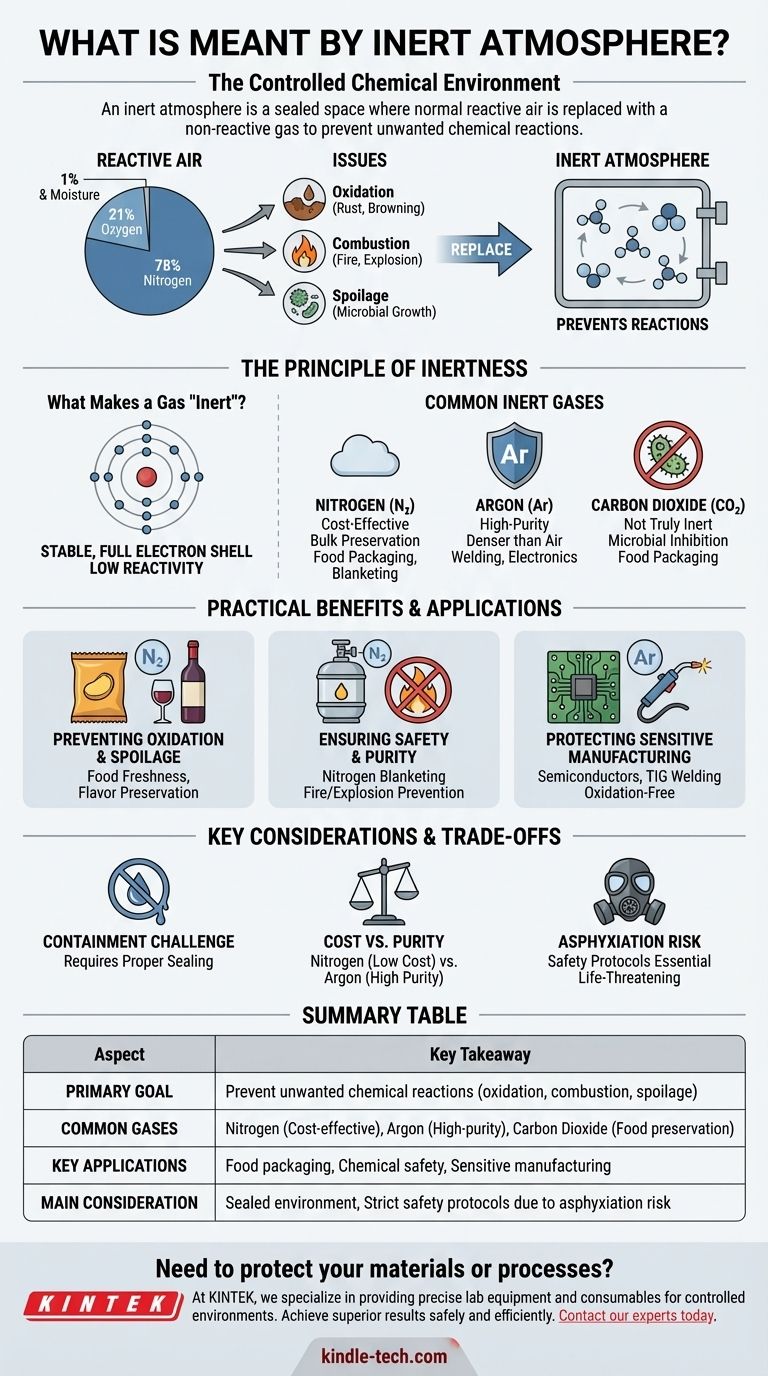
L'air que nous respirons est composé d'environ 78 % d'azote, 21 % d'oxygène et de petites quantités d'autres gaz, y compris la vapeur d'eau. Pour de nombreux processus industriels, scientifiques et commerciaux, cette composition est un inconvénient majeur.
Pourquoi l'oxygène est souvent un problème
L'oxygène est un élément très réactif. Sa tendance à se combiner avec d'autres substances est responsable de processus courants comme la rouille (oxydation du fer) et le brunissement d'une pomme coupée. Dans des situations plus volatiles, c'est un composant clé du feu et des explosions.
Le rôle de l'humidité
La vapeur d'eau présente dans l'air peut également accélérer la corrosion et fournir un environnement propice à la croissance microbienne, entraînant la détérioration des aliments ou la contamination des matériaux sensibles.
Le principe d'inertie
La création d'une atmosphère inerte implique de purger un espace scellé de l'air ambiant et de le remplir avec un gaz qui n'interférera pas avec le produit ou le processus protégé.
Qu'est-ce qui rend un gaz "inerte" ?
Les gaz inertes sont chimiquement stables car leur couche électronique externe est pleine, ce qui signifie qu'ils ont très peu tendance à réagir avec d'autres éléments. Bien que les vrais gaz nobles comme l'argon soient les plus inertes, d'autres gaz comme l'azote sont suffisamment non réactifs pour la plupart des applications.
Gaz couramment utilisés
Le choix du gaz dépend du niveau d'inertie requis et du budget.
- Azote (N₂) : De loin le plus courant, car il est peu coûteux et constitue la majeure partie de notre atmosphère, ce qui le rend facile à se procurer.
- Argon (Ar) : Plus inerte que l'azote et plus dense que l'air. Il est utilisé pour des applications plus sensibles comme le soudage haut de gamme et la fabrication d'électronique où même la légère réactivité de l'azote est inacceptable.
- Dioxyde de carbone (CO₂) : Bien que n'étant pas vraiment inerte, il est souvent utilisé dans l'emballage alimentaire car il déplace l'oxygène et peut inhiber la croissance de certaines bactéries et moisissures.
Avantages pratiques et applications
La valeur d'une atmosphère inerte est démontrée dans un large éventail de domaines où le contrôle de l'environnement chimique est essentiel.
Prévention de l'oxydation et de la détérioration
C'est l'une des utilisations les plus courantes. L'air à l'intérieur d'un sac de chips est remplacé par de l'azote pour empêcher les huiles de rancir et pour amortir le produit. De même, les vignerons utilisent des gaz inertes pour protéger le vin de l'oxygène pendant l'embouteillage.
Assurer la sécurité et la pureté
Dans les usines de traitement chimique, l'air des cuves contenant des liquides ou des poudres inflammables est souvent remplacé par de l'azote. Ce processus, connu sous le nom de "blanketing à l'azote", élimine l'oxygène nécessaire à un incendie ou à une explosion, améliorant considérablement la sécurité.
Protection de la fabrication sensible
Lors de la fabrication de semi-conducteurs et d'électronique, même des niveaux microscopiques d'oxydation peuvent ruiner un composant. Ces processus sont souvent menés dans des chambres remplies d'un gaz inerte de haute pureté comme l'argon. Les soudeurs utilisent également un bouclier de gaz inerte pour protéger le bain de fusion de l'oxygène, ce qui affaiblirait le joint final.
Considérations clés et compromis
Bien que puissante, la mise en œuvre d'une atmosphère inerte nécessite une planification minutieuse et une compréhension de ses limites.
Le défi du confinement
Une atmosphère inerte n'est efficace que si le conteneur ou la pièce est correctement scellé. Toute fuite permettra à l'oxygène et à l'humidité de rentrer, annulant le but du système.
Coût vs pureté
Il existe un compromis direct entre le coût du gaz et son niveau d'inertie. L'azote est suffisant pour la plupart des applications en vrac, mais les processus nécessitant une pureté chimique absolue exigent des gaz plus coûteux comme l'argon.
Risque critique d'asphyxie
Une atmosphère conçue pour prévenir la combustion est aussi une atmosphère qui ne peut pas soutenir la vie. Toute zone inondée d'un gaz inerte présente un risque d'asphyxie extrême, car elle contient peu ou pas d'oxygène. Des protocoles de sécurité stricts sont essentiels pour tout personnel travaillant dans ou à proximité de ces environnements.
Faire le bon choix pour votre objectif
La sélection et l'application d'une atmosphère inerte sont entièrement dictées par le résultat souhaité.
- Si votre objectif principal est une conservation rentable : L'azote est le choix standard pour les applications à grande échelle comme l'emballage alimentaire, les silos à grains et l'inertage des réservoirs chimiques.
- Si votre objectif principal est un traitement de haute pureté : L'argon est l'option supérieure pour les travaux sensibles comme le soudage TIG, la recherche scientifique et la fabrication de plaquettes de silicium où une non-réactivité absolue est vitale.
- Si votre objectif principal est l'inhibition microbienne active : Une atmosphère modifiée incluant du dioxyde de carbone est souvent utilisée dans l'emballage de la viande et des produits frais pour prolonger la durée de conservation au-delà de la simple prévention de l'oxydation.
En fin de compte, une atmosphère inerte est un outil puissant pour prendre le contrôle de l'environnement chimique afin de protéger et de préserver les matériaux et les processus sensibles.
Tableau récapitulatif :
| Aspect | Point clé à retenir |
|---|---|
| Objectif principal | Prévenir les réactions chimiques indésirables (oxydation, combustion, détérioration). |
| Gaz courants | Azote (rentable), Argon (haute pureté), Dioxyde de carbone (conservation alimentaire). |
| Applications clés | Emballage alimentaire, sécurité chimique (inertage), fabrication sensible (soudage, électronique). |
| Considération principale | Nécessite un environnement scellé et des protocoles de sécurité stricts en raison du risque d'asphyxie. |
Besoin de protéger vos matériaux ou processus de l'oxygène et de l'humidité ?
Chez KINTEK, nous sommes spécialisés dans la fourniture de l'équipement de laboratoire et des consommables précis nécessaires pour créer et maintenir des environnements contrôlés pour votre laboratoire. Que votre objectif soit une conservation rentable ou un traitement de haute pureté, nos solutions peuvent vous aider à obtenir des résultats supérieurs en toute sécurité et efficacité.
Contactez nos experts dès aujourd'hui pour discuter de la façon dont nous pouvons soutenir votre application spécifique avec des solutions fiables d'atmosphère inerte.
Guide Visuel
Produits associés
- Four à atmosphère contrôlée 1200℃, four à atmosphère inerte à l’azote
- Four à atmosphère contrôlée 1700℃ Four à atmosphère inerte d'azote
- Four à atmosphère contrôlée de 1400℃ avec atmosphère d'azote et inerte
- Four à atmosphère d'hydrogène contrôlée à l'azote
- Four à atmosphère contrôlée à bande transporteuse
Les gens demandent aussi
- Quelle est la nécessité d'un four à atmosphère contrôlée pour la recherche sur la corrosion ? Répliquer les risques industriels réalistes
- Qu'est-ce qu'un four à atmosphère contrôlée pour le traitement thermique ? Maîtriser la chimie des surfaces et la métallurgie
- Qu'est-ce qu'un four à atmosphère contrôlée ? Atteignez la pureté et la précision dans le traitement à haute température
- Quelle est la fonction d'un four à atmosphère contrôlée ? Maîtriser la nitruration pour les aciers AISI 52100 et 1010
- Quel est le rôle de l'atmosphère du four ? Maîtrisez le contrôle métallurgique précis pour votre traitement thermique




