L'unité SI principale pour la capacité thermique est le joule par kelvin (J/K). Cette unité décrit la quantité d'énergie (en joules) nécessaire pour élever la température d'un objet ou d'un système entier d'un degré Kelvin. Cependant, les unités spécifiques que vous rencontrez changeront selon que vous mesurez un objet entier, une masse spécifique d'une substance ou une quantité molaire.
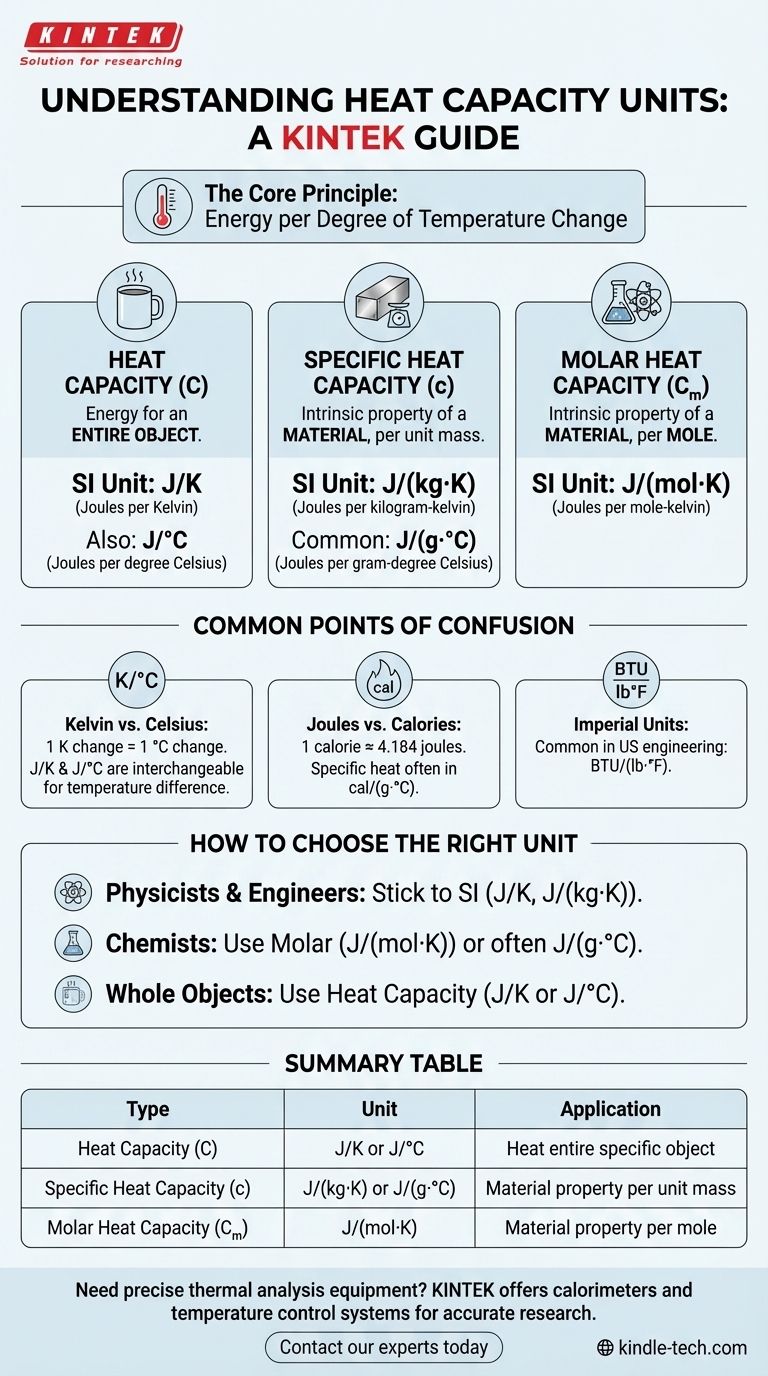
Les unités de capacité thermique représentent toujours l'énergie par degré de changement de température. Comprendre la différence entre la capacité thermique, la capacité thermique spécifique et la capacité thermique molaire est la clé pour identifier et utiliser l'unité correcte pour votre calcul.

Ce que signifient réellement les unités
Capacité Thermique (C)
La capacité thermique fait référence à l'énergie nécessaire pour élever la température d'un objet entier d'un degré. Comme elle concerne un objet spécifique et entier (comme une tasse à café ou un bloc moteur), sa masse est déjà prise en compte.
L'unité est simplement l'énergie divisée par la température : joules par kelvin (J/K). Vous pouvez également la voir exprimée sous forme de joules par degré Celsius (J/°C).
Capacité Thermique Spécifique (c)
C'est la mesure la plus courante que vous rencontrerez. La chaleur spécifique est une propriété intrinsèque d'un matériau, et non d'un objet. C'est l'énergie requise pour élever la température d'une unité de masse d'une substance d'un degré.
L'unité SI standard est le joule par kilogramme-kelvin (J/(kg·K)).
En chimie et dans d'autres contextes de laboratoire, il est très courant de voir des unités basées sur les grammes et les Celsius, telles que joules par gramme-degré Celsius (J/(g·°C)).
Capacité Thermique Molaire (Cₘ)
La capacité thermique molaire est également une propriété intrinsèque d'un matériau, mais elle est définie par mole au lieu de par masse. Ceci est particulièrement utile en chimie, où les réactions sont décrites en termes de moles.
L'unité SI standard est le joule par mole-kelvin (J/(mol·K)).
Points de confusion courants
Kelvin contre Celsius
Pour les calculs de capacité thermique, un changement d'un degré Kelvin (1 K) est exactement le même qu'un changement d'un degré Celsius (1 °C).
Par conséquent, les unités J/K et J/°C sont fonctionnellement interchangeables lorsque vous calculez une différence de température. Il en va de même pour J/(kg·K) et J/(kg·°C).
Joules contre Calories
La calorie (cal) est une unité d'énergie plus ancienne, non SI. Elle est encore utilisée dans certains contextes, notamment en chimie et en nutrition.
La conversion est d'environ 1 calorie = 4,184 joules. Vous pouvez voir la chaleur spécifique exprimée en cal/(g·°C). Par exemple, la chaleur spécifique de l'eau est très proche de 1,0 cal/(g·°C).
Unités Impériales et Coutumières Américaines
Dans certains domaines de l'ingénierie, en particulier aux États-Unis, vous pouvez rencontrer des unités impériales.
L'unité la plus courante pour la chaleur spécifique dans ce système est l'Unité Thermique Britannique par livre par degré Fahrenheit (BTU/(lb·°F)).
Comment choisir la bonne unité pour votre application
-
Si vous êtes physicien ou ingénieur : Tenez-vous-en aux unités SI standard. Utilisez J/K pour les systèmes entiers et J/(kg·K) pour les propriétés des matériaux.
-
Si vous êtes chimiste : La capacité thermique molaire (J/(mol·K)) est souvent la plus utile pour les calculs de réaction, bien que vous utilisiez fréquemment J/(g·°C) pour le travail en laboratoire.
-
Si vous travaillez avec un objet entier et spécifique : Utilisez l'unité de capacité thermique générale, J/K ou J/°C, car la masse de l'objet est déjà prise en compte.
Comprendre quelle quantité est mesurée — un objet entier, une unité de masse ou une mole — est le guide définitif pour choisir l'unité correcte.
Tableau Récapitulatif :
| Type de Capacité Thermique | Unité | Application |
|---|---|---|
| Capacité Thermique (C) | J/K ou J/°C | Énergie pour chauffer un objet spécifique et entier |
| Capacité Thermique Spécifique (c) | J/(kg·K) ou J/(g·°C) | Propriété intrinsèque d'un matériau (par unité de masse) |
| Capacité Thermique Molaire (Cₘ) | J/(mol·K) | Propriété intrinsèque d'un matériau (par mole) |
Besoin d'un équipement d'analyse thermique précis pour votre laboratoire ? Comprendre la capacité thermique est crucial pour les expériences en chimie, en science des matériaux et en ingénierie. KINTEK se spécialise dans les équipements de laboratoire de haute qualité, y compris les calorimètres et les systèmes de contrôle de température, pour garantir que vos mesures sont précises et fiables. Contactez nos experts dès aujourd'hui pour trouver la solution parfaite pour les besoins d'analyse thermique de votre laboratoire.
Guide Visuel