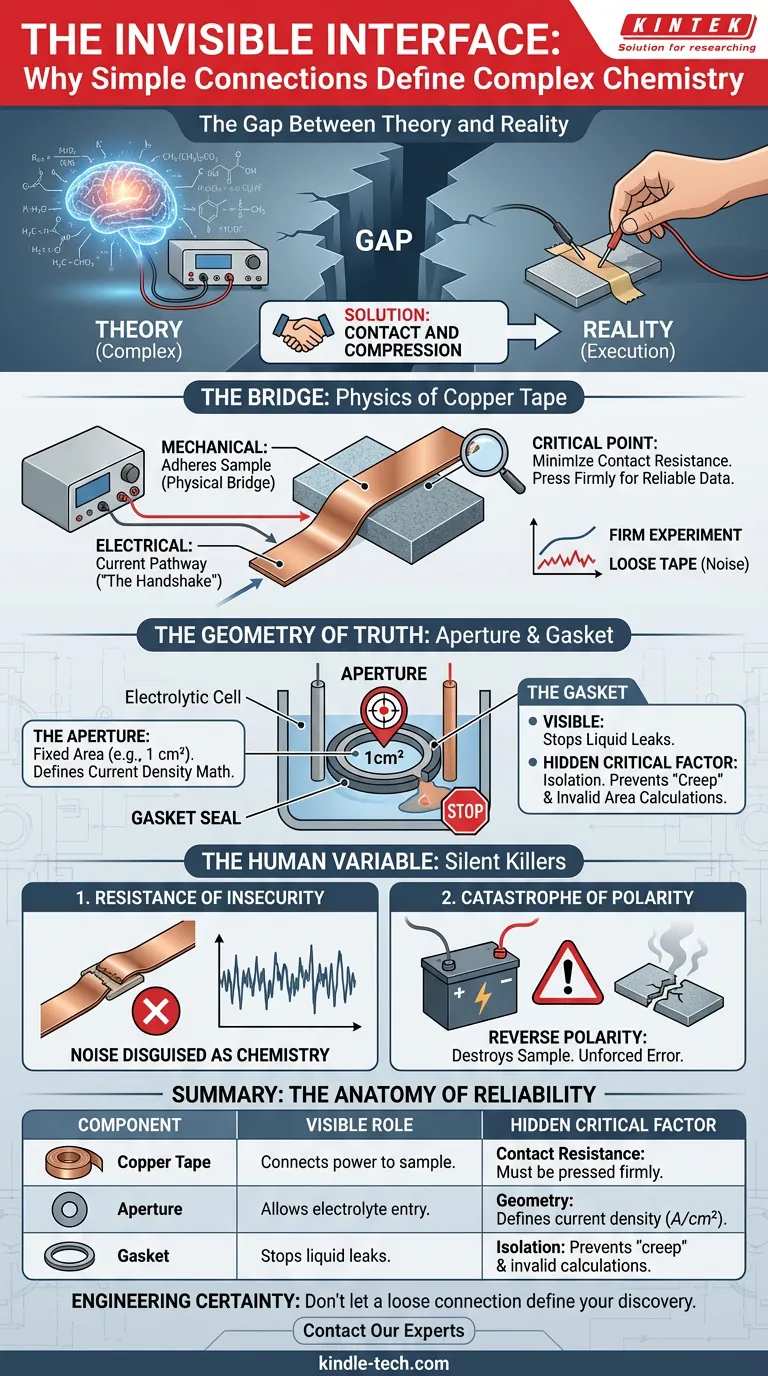
L'écart entre la théorie et la réalité
Nous avons tendance à romantiser les aspects complexes de la science. En électrochimie, nous nous obsédons sur l'équation de Nernst, le potentiostat sophistiqué ou la structure moléculaire de l'électrolyte.
Nous supposons que si la théorie est solide, le résultat est inévitable.
Mais le point de défaillance le plus courant dans un laboratoire n'est généralement pas une faille dans la théorie chimique. C'est une faille dans l'exécution physique. C'est l'écart entre le monde macroscopique (le fil) et le monde microscopique (l'échantillon).
Combler cet écart nécessite une solution qui semble presque trop simple pour être scientifique : le contact et la compression.
Le pont : la physique du ruban de cuivre
Pour rendre un échantillon d'électrode de travail conducteur, vous n'avez pas besoin d'une soudure laser complexe. Vous avez besoin d'un pont physique fiable. Dans cette conception de cellule électrolytique, ce pont est le ruban de cuivre.
Il remplit une double fonction qui plaît au désir d'efficacité de l'ingénieur :
- Mécanique : Il adhère physiquement l'échantillon au contact de la cellule.
- Électrique : Il crée le chemin pour que le courant circule de l'alimentation électrique au matériau.
C'est la "poignée de main" de l'expérience. Si le ruban de cuivre est lâche, la poignée de main est faible. La résistance augmente. La chute de tension devient imprévisible.
Les données que vous voyez à l'écran ne sont aussi honnêtes que le morceau de ruban qui maintient votre échantillon.
La géométrie de la vérité
Une fois la connexion établie, l'expérience a besoin de limites. En science, les variables indéfinies sont l'ennemi de la reproductibilité.
La cellule utilise une conception physique stricte pour imposer l'ordre au comportement chaotique des ions :
- L'ouverture : Un trou circulaire fixe, généralement de 1 cm².
- Le joint : Un joint d'étanchéité qui isole la réaction.
Pourquoi le joint est important
Le joint fait plus que prévenir les fuites. Il définit la "vérité" de vos données.
La densité de courant est calculée en fonction de la surface. Si l'électrolyte fuit sous le joint, votre surface réactive augmente, ce qui vous est effectivement inconnu. Vos calculs de densité de courant seront erronés, non pas parce que la chimie a échoué, mais parce que la géométrie a échoué.
Le joint garantit que seule la partie exposée participe à la réaction. Il force l'univers de votre expérience à exister dans ce cercle défini de 1 cm².
La variable humaine
Atul Gawande écrit souvent que le volume de connaissances en médecine a dépassé notre capacité à le gérer en toute sécurité sans listes de contrôle. Il en va de même pour le paillasse de laboratoire.
La machinerie est parfaite ; l'opérateur est humain. Il existe deux "tueurs silencieux" des données électrochimiques :
1. La résistance de l'insécurité
Une connexion physique peu sûre — où le ruban de cuivre n'est pas fermement pressé — introduit une résistance de contact. Ce bruit se déguise en comportement chimique. Vous pourriez passer des semaines à analyser un "pic" dans vos données qui n'est en fait qu'un morceau de ruban lâche.
2. La catastrophe de la polarité
L'erreur la plus dangereuse est la plus simple : l'inversion de polarité.
Connecter incorrectement le positif au négatif n'est pas seulement une erreur de données. Cela peut déclencher des réactions indésirables qui détruisent l'échantillon ou endommagent l'électrode. C'est une erreur non provoquée qui se produit lorsque nous sommes pressés.
Résumé : L'anatomie de la fiabilité
Comprendre le système vous permet de dépanner le résultat.
| Composant | Le rôle visible | Le facteur critique "caché" |
|---|---|---|
| Ruban de cuivre | Connecte l'alimentation à l'échantillon | Résistance de contact : Doit être fermement pressé pour minimiser le bruit. |
| Ouverture | Permet l'entrée de l'électrolyte | Géométrie : Définit les mathématiques derrière la densité de courant ($A/cm^2$). |
| Joint | Arrête les fuites de liquide | Isolation : Empêche le "glissement" qui invalide les calculs de surface. |
Ingénierie de la certitude
La grande science consiste à contrôler les variables. Vous ne pouvez pas contrôler l'électron, mais vous pouvez contrôler la connexion.
Chez KINTEK, nous comprenons que la fiabilité de vos données tient à un fil — ou dans ce cas, à un morceau de ruban de cuivre et à un joint. Nous concevons nos équipements de laboratoire et nos consommables pour éliminer les conjectures de ces interfaces physiques, vous permettant de vous concentrer sur la chimie plutôt que sur la mécanique.
Ne laissez pas une connexion lâche définir votre découverte.
Guide Visuel
Produits associés
- Fabricant personnalisé de pièces en PTFE Téflon pour joints et plus
- Joint d'étanchéité pour boîtier de pile bouton pour applications de laboratoire de piles
- Mousse de cuivre
- Joint isolant en céramique de zircone Ingénierie avancée céramiques fines
Articles associés
- Performance et application du polytétrafluoroéthylène (PTFE) dans un environnement à haute température
- Le rôle clé du PTFE dans la fabrication des semi-conducteurs : des gazoducs à l'isolation électrique
- Analyse approfondie des principales caractéristiques et des avantages du polytétrafluoroéthylène
- Le polytétrafluoroéthylène (PTFE) :Comment un faible coefficient de frottement favorise le progrès industriel
- Joint PTFE : une solution polyvalente pour l'étanchéité des brides




