D'un point de vue technique, la lyophilisation améliore la qualité pharmaceutique en transformant fondamentalement un produit liquide instable en un solide poreux stable. Ceci est réalisé en éliminant l'eau par sublimation, ce qui réduit considérablement la dégradation chimique, prolonge la durée de conservation souvent à plusieurs années à température ambiante, et crée un produit qui peut être rapidement reconstitué pour utilisation tout en préservant ses propriétés thérapeutiques originales.
Le défi principal de nombreux médicaments modernes, en particulier les produits biologiques et les vaccins, est leur instabilité inhérente sous forme liquide. La lyophilisation résout ce problème non pas en séchant simplement le produit, mais en fixant sa structure moléculaire délicate à basse température, garantissant ainsi que sa sécurité et son efficacité sont préservées de la fabrication à l'administration au patient.

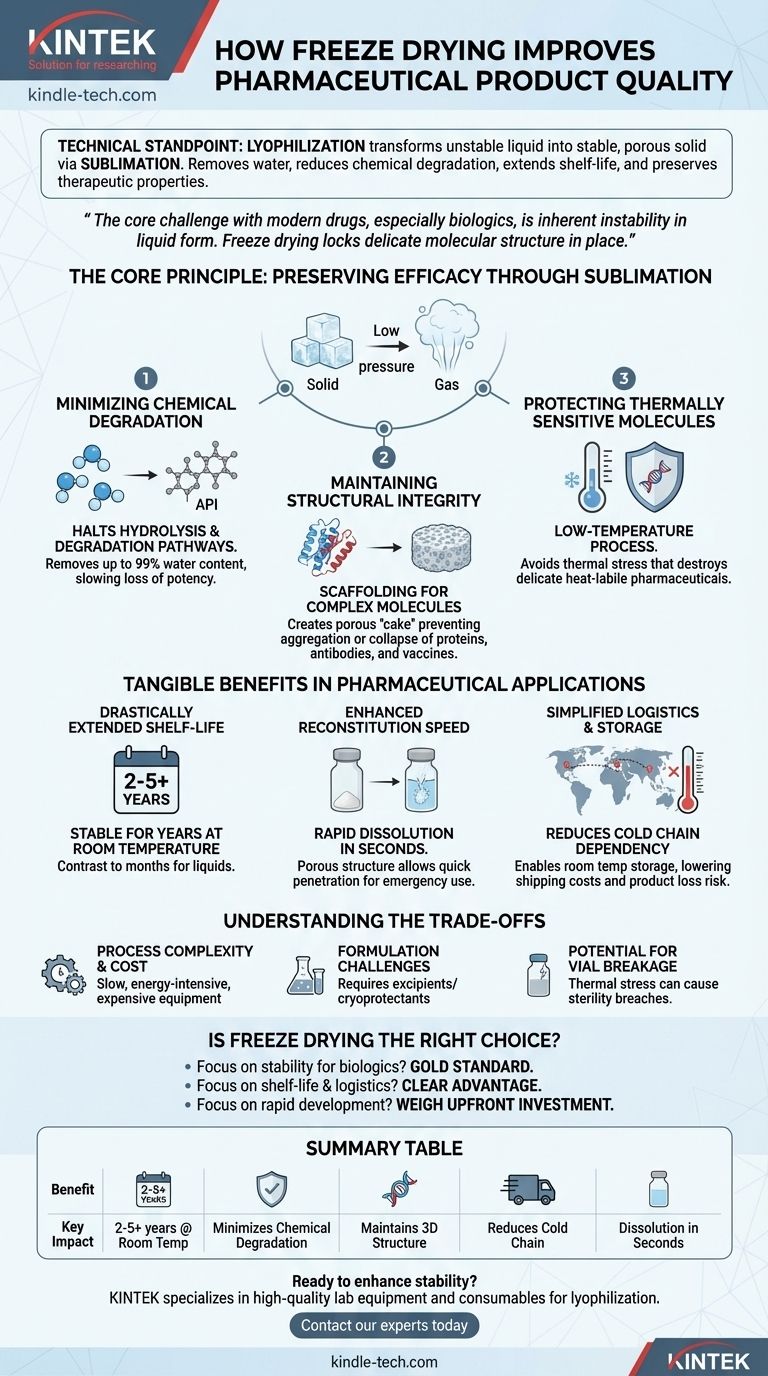
Le principe fondamental : Préserver l'efficacité par sublimation
La lyophilisation est un processus de déshydratation à basse température qui consiste à congeler le produit, à abaisser la pression, puis à éliminer la glace par sublimation – la transition directe d'un solide à un gaz. Ce mécanisme unique est la clé de ses avantages en matière d'amélioration de la qualité.
Minimiser la dégradation chimique
L'eau est un milieu principal pour les réactions chimiques, en particulier l'hydrolyse, qui peut décomposer et inactiver les principes actifs pharmaceutiques (API). En éliminant jusqu'à 99 % de la teneur en eau, la lyophilisation arrête efficacement ces voies de dégradation.
Cela ralentit considérablement la perte de puissance au fil du temps, garantissant que le médicament délivre son effet thérapeutique prévu même après des années de stockage.
Maintenir l'intégrité structurelle
Pour les molécules complexes comme les protéines, les anticorps et les vaccins, leur structure tridimensionnelle est essentielle à leur fonction. Les méthodes de séchage thermique conventionnelles peuvent provoquer la dénaturation et l'effondrement de cette structure, rendant le médicament inutile.
La lyophilisation, cependant, élimine l'eau d'un état congelé. Ce processus agit comme un échafaudage, créant un « gâteau » poreux et spongieux qui maintient la dispersion moléculaire originale du médicament et empêche l'agrégation ou l'effondrement structurel.
Protéger les molécules thermosensibles
De nombreux produits biologiques avancés sont extrêmement sensibles à la chaleur. L'ensemble du processus de lyophilisation est effectué à des températures basses ou sub-zéro, ce qui évite le stress thermique qui détruirait autrement ces produits délicats. Cela en fait la méthode privilégiée pour la conservation des produits pharmaceutiques thermolabiles.
Avantages tangibles dans les applications pharmaceutiques
Les principes scientifiques de la lyophilisation se traduisent directement par des avantages critiques et concrets pour le développement, la fabrication et la distribution de médicaments.
Durée de conservation considérablement prolongée
Le principal avantage de la création d'un état sec et stable est une prolongation massive de la durée de conservation du produit. De nombreux produits pharmaceutiques lyophilisés sont stables pendant deux à cinq ans ou plus à température ambiante, un contraste frappant avec les formulations liquides qui ne peuvent durer que quelques mois même avec réfrigération.
Vitesse de reconstitution améliorée
La structure de gâteau poreuse créée pendant la sublimation a une très grande surface. Lorsqu'un solvant (comme de l'eau stérile) est ajouté, il peut pénétrer rapidement cette structure, permettant au produit de se dissoudre et d'être reconstitué en quelques secondes. C'est un avantage essentiel pour la médecine d'urgence et la commodité clinique.
Logistique et stockage simplifiés
En permettant le stockage à température ambiante, la lyophilisation peut éliminer le besoin d'une « chaîne du froid » continue et coûteuse – le réseau réfrigéré nécessaire pour stocker et transporter de nombreux produits biologiques liquides. Cela simplifie la distribution mondiale, réduit les coûts d'expédition et diminue le risque de perte de produit due aux excursions de température.
Comprendre les compromis
Bien que puissante, la lyophilisation n'est pas une solution universelle. L'objectivité exige de reconnaître ses défis importants.
Complexité et coût du processus
La lyophilisation est un processus lent, de plusieurs jours, et très énergivore. L'équipement spécialisé est coûteux à acheter, à exploiter et à entretenir, ce qui en fait l'une des opérations unitaires les plus coûteuses dans la fabrication pharmaceutique.
Défis de formulation
Vous ne pouvez pas simplement mettre n'importe quel médicament liquide dans un lyophilisateur. Une lyophilisation réussie nécessite souvent un développement de formulation approfondi, y compris l'ajout d'excipients (comme des sucres ou des acides aminés) qui agissent comme cryoprotecteurs et lyoprotecteurs pour protéger l'API pendant les contraintes de congélation et de séchage.
Potentiel de rupture de flacon
L'étape de congélation induit un stress thermique important sur le récipient primaire du produit (généralement un flacon en verre). Sans une optimisation minutieuse du processus, cela peut entraîner la rupture du récipient, ce qui se traduit par des ruptures de stérilité et une perte de produit.
La lyophilisation est-elle le bon choix pour votre produit ?
La décision d'utiliser la lyophilisation est un équilibre stratégique entre les exigences de qualité, les besoins logistiques et les coûts.
- Si votre objectif principal est la stabilité d'un produit biologique ou d'un vaccin : La lyophilisation est souvent la norme d'or pour préserver la structure et la fonction des molécules complexes et thermosensibles.
- Si votre objectif principal est de prolonger la durée de conservation et de simplifier la logistique : La lyophilisation offre un avantage évident en permettant le stockage à température ambiante et en réduisant ou en éliminant la dépendance à la chaîne du froid.
- Si votre objectif principal est un développement rapide et un faible coût : Vous devez peser la qualité supérieure de la lyophilisation par rapport à son investissement significatif en développement de processus, en temps de cycle et en équipement capital.
En fin de compte, la lyophilisation est un investissement stratégique dans la qualité des produits, échangeant une complexité initiale contre une stabilité et une fiabilité à long terme.
Tableau récapitulatif :
| Avantage | Impact clé |
|---|---|
| Durée de conservation prolongée | Stable pendant 2 à 5 ans et plus à température ambiante contre quelques mois pour les liquides |
| Potence préservée | Minimise la dégradation chimique (par exemple, hydrolyse) des API |
| Intégrité structurelle | Maintient la structure 3D des protéines, anticorps et vaccins |
| Logistique simplifiée | Réduit ou élimine le besoin de stockage coûteux en chaîne du froid |
| Reconstitution rapide | La structure de gâteau poreuse permet une dissolution en quelques secondes |
Prêt à améliorer la stabilité et la durée de conservation de vos produits pharmaceutiques ? Le processus de lyophilisation est une science précise qui nécessite un équipement fiable. KINTEK est spécialisé dans les équipements de laboratoire et les consommables de haute qualité pour le développement et la fabrication pharmaceutiques. Notre expertise peut vous aider à naviguer dans les complexités de la lyophilisation pour atteindre une qualité de produit supérieure. Contactez nos experts dès aujourd'hui pour discuter de la manière dont nos solutions peuvent répondre à vos besoins spécifiques en laboratoire.
Guide Visuel
Produits associés
- Lyophilisateur de laboratoire haute performance
- Lyophilisateur de laboratoire haute performance pour la recherche et le développement
- Lyophilisateur de laboratoire de paillasse pour usage en laboratoire
- Lyophilisateur de laboratoire de paillasse
- Congélateur Ultra Basse Température Vertical 108L
Les gens demandent aussi
- Quels types d'échantillons liquides peuvent être traités à l'aide d'un lyophilisateur de laboratoire ? Préservez vos matériaux sensibles
- Quelles précautions prendre lors de l'utilisation d'un lyophilisateur de laboratoire ? Étapes essentielles pour une lyophilisation fiable
- Quels sont les principaux avantages de la lyophilisation en laboratoire ? Préservez les matériaux sensibles grâce à une lyophilisation douce
- Quels sont les principaux composants d'un lyophilisateur de laboratoire ? Un guide des 5 systèmes essentiels
- Comment les lyophilisateurs de laboratoire soutiennent-ils la recherche scientifique ? Préserver l'intégrité de l'échantillon pour des résultats reproductibles















