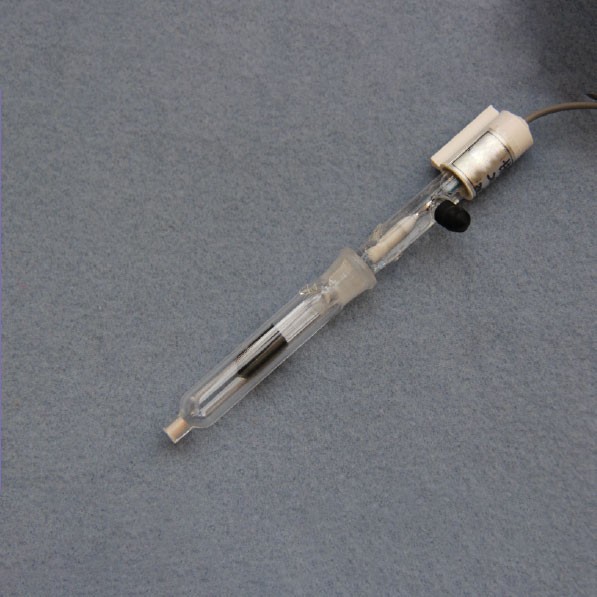
Introduction aux électrodes de référence
Les électrodes de référence jouent un rôle crucial dans les mesures électrochimiques, en garantissant des potentiels stables et reproductibles. Dans le domaine de la recherche scientifique et des applications de laboratoire, la précision et la fiabilité de ces électrodes sont primordiales. Cet article traite des spécificités des électrodes de référence en calomel saturéélectrodes de référence au calomel saturé (SCE), en explorant leur composition, leurs principes de fonctionnement, leurs avantages et leurs limites. Idéal pour les chercheurs et les techniciens de laboratoire, ce guide complet vise à améliorer la compréhension et l'application pratique des SCE dans divers contextes scientifiques.
Qu'est-ce qu'une électrode de calomel saturée (ECS) ?
L'électrode de Calomel saturée (SCE) est une électrode de référence largement utilisée dans les mesures électrochimiques, connue pour sa stabilité et sa facilité d'utilisation. Elle se compose d'une électrode de mercure (Hg) recouverte d'une couche de chlorure de mercure(I), également appelée calomel (Hg2Cl2), qui est en contact avec une solution saturée de chlorure de potassium (KCl). Cette configuration permet d'obtenir un potentiel de référence cohérent et fiable pour diverses applications électrochimiques.
Structure et composants
Le SCE est constitué de plusieurs composants clés :
- Mercure (Hg): Le mercure métallique sert de surface d'électrode.
- Chlorure de mercure(I) (Hg2Cl2): Cette couche de calomel forme une pâte avec le mercure, assurant l'équilibre chimique nécessaire au fonctionnement de l'électrode.
- Solution saturée de chlorure de potassium (KCl): La solution d'électrolyte est maintenue saturée pour maintenir une activité ionique constante, ce qui stabilise le potentiel de l'électrode. La saturation est cruciale car elle fixe l'activité des ions chlorure, assurant ainsi un potentiel stable.
- Fil de platine: Ce composant facilite le contact électrique entre l'électrode et le circuit externe.

Avantages et inconvénients
Avantages :
- Facilité de mise en place et reproductibilité: La SCE est simple à préparer et peut être facilement reproduite, ce qui garantit des résultats cohérents.
- Compact et portable: Sa petite taille et sa portabilité lui permettent de s'adapter à diverses configurations expérimentales.
- Aucun pont salin séparé n'est nécessaire: La solution de KCl saturée à l'intérieur de l'électrode agit comme son propre pont salin, ce qui simplifie l'installation.
- Potentiel stable: Le potentiel de l'électrode reste stable dans le temps et en cas de fluctuations mineures de la température.
Inconvénients :
- Gamme de température limitée: L'utilisation de la SCE est généralement limitée à une température inférieure à 50°C en raison de l'instabilité potentielle à des températures plus élevées.
- Interférence avec certains ions: La présence d'ions K+ et Cl- dans l'échantillon peut interférer avec les réactions électrochimiques, ce qui limite son applicabilité dans certains scénarios.
- Compensation de potentiel nécessaire: Lors de la mesure des potentiels de demi-cellule, des ajustements peuvent être nécessaires pour tenir compte du potentiel inhérent du SCE.
Applications
Le SCE est largement utilisé dans divers domaines, notamment la chimie analytique, la surveillance de l'environnement et les processus industriels. Il sert de point de référence fiable pour mesurer les potentiels d'autres électrodes, ce qui permet d'obtenir des données précises et cohérentes lors de différentes expériences.
En résumé, l'électrode au calomel saturé est une électrode de référence robuste et polyvalente qui offre un potentiel stable, une facilité d'utilisation et une reproductibilité. Malgré certaines limites, ses avantages en font un choix privilégié pour de nombreuses applications électrochimiques.
Avantages de l'utilisation d'électrodes de calomel saturées (SCE)
Les électrodes de calomel saturées (SCE) sont largement utilisées dans les expériences et les applications électrochimiques en raison de leurs nombreux avantages. Ces électrodes sont composées de chlorure mercureux (calomel) en contact avec du mercure métallique, généralement en couche sous une solution saturée de chlorure de potassium (KCl). La SCE fournit un potentiel de référence stable et reproductible, ce qui en fait un outil essentiel dans divers contextes d'analyse et de recherche. Nous examinons ici les principaux avantages de l'utilisation du SCE, notamment la facilité d'installation, la reproductibilité, la compacité et la stabilité du potentiel au fil du temps et des variations de température.
Facilité d'installation
L'un des principaux avantages de l'utilisation d'une SCE est sa simplicité d'installation. L'électrode est composée d'éléments simples : calomel, mercure et une solution de KCl saturée. Cette simplicité réduit la complexité de l'assemblage et minimise le risque d'erreurs lors de l'installation. De plus, la SCE ne nécessite pas de pont salin séparé, car elle comprend déjà un tube latéral contenant la solution de KCl. Cette caractéristique simplifie le montage expérimental et garantit que l'électrode est prête à l'emploi avec une préparation minimale.
Reproductibilité
La reproductibilité est un facteur essentiel dans la recherche scientifique et les mesures analytiques. Les SCE offrent une grande reproductibilité, ce qui signifie que le potentiel généré par l'électrode reste constant au cours de différentes expériences et configurations. Cette constance est cruciale pour la collecte de données précises et fiables. La composition et la structure normalisées des SCE contribuent à leur reproductibilité, ce qui en fait un choix privilégié pour les chercheurs et les analystes qui exigent des résultats précis et reproductibles.
Compacité
Les SCE sont connues pour leur conception compacte, ce qui les rend pratiques à utiliser dans divers montages expérimentaux. La petite taille de l'électrode nécessite un minimum d'espace, ce qui permet une utilisation plus efficace de l'espace de la paillasse du laboratoire. En outre, la conception compacte facilite le transport, ce qui rend les SCE adaptées au travail sur le terrain et aux mesures sur place. Cette portabilité est particulièrement bénéfique pour les applications où la mobilité et la flexibilité sont essentielles.
Stabilité du potentiel
La stabilité du potentiel généré par un SCE est un autre avantage important. Le potentiel du SCE reste relativement constant dans le temps et est peu affecté par de légères variations de température. Cette stabilité garantit que le potentiel de référence fourni par l'électrode reste précis et fiable, même dans des conditions expérimentales variables. Le potentiel constant des SCE est essentiel pour maintenir l'intégrité des mesures électrochimiques et garantir la validité et la fiabilité des résultats.
Variations de température
Les SCE présentent un degré élevé de stabilité en réponse aux variations de température. Bien que l'électrode soit généralement utilisée dans une plage de température limitée (jusqu'à 50 °C), son potentiel reste relativement insensible aux petites fluctuations de température. Cette stabilité de température est essentielle pour les expériences et les mesures qui peuvent être effectuées dans des conditions environnementales variables. La capacité des SCE à maintenir un potentiel stable à différentes températures renforce leur polyvalence et leur applicabilité dans divers contextes de recherche et d'analyse.
En conclusion, les avantages de l'utilisation d'électrodes de calomel saturées (SCE) sont nombreux et significatifs. Leur facilité d'installation, leur reproductibilité, leur compacité et la stabilité du potentiel au fil du temps et des variations de température en font un outil inestimable pour la recherche et l'analyse électrochimiques. Ces avantages garantissent que les SCE restent un choix privilégié pour les scientifiques et les analystes qui ont besoin d'électrodes de référence précises, fiables et efficaces dans leur travail.
Inconvénients et limites
L'électrode au calomel saturé (SCE) est une électrode de référence largement utilisée dans diverses applications électrochimiques en raison de son potentiel stable et de sa facilité de préparation. Cependant, elle n'est pas dépourvue d'inconvénients et de limites. Les comprendre peut aider à sélectionner l'électrode de référence appropriée pour des applications spécifiques.
Interférence potentielle avec certains ions
L'une des principales limites de l'ECS est son interférence potentielle avec certains ions présents dans l'échantillon. La SCE contient une solution saturée de chlorure de potassium (KCl), qui peut interférer avec la mesure si l'échantillon contient également des ions chlorure. Cette interférence peut conduire à des lectures inexactes, en particulier dans les échantillons à forte concentration de chlorure. Par exemple, dans le cadre de la surveillance environnementale de l'eau de mer, la forte teneur en chlorure peut affecter de manière significative la précision de la SCE.
Nécessité d'une compensation potentielle
Une autre limite de la SCE est la nécessité d'une compensation de potentiel. Le potentiel du SCE est relativement stable, mais il peut varier en fonction des changements de température. Cela nécessite l'utilisation de circuits ou de logiciels de compensation de la température dans de nombreuses applications afin de garantir des mesures précises. Sans une compensation appropriée, le potentiel peut dériver, entraînant des résultats erronés. Ceci est particulièrement important dans les applications où des mesures précises et exactes sont essentielles, comme dans la recherche pharmaceutique et biomédicale.
Problèmes d'environnement et de sécurité liés à la teneur en mercure
La limitation la plus importante de la SCE concerne les problèmes d'environnement et de sécurité liés à sa teneur en mercure. Le mercure est un métal toxique qui présente de graves risques pour la santé en cas d'inhalation ou d'ingestion. L'utilisation des SCE dans les laboratoires et les environnements industriels nécessite des procédures de manipulation strictes afin d'éviter l'exposition au mercure. En outre, l'élimination des SCE et de leurs composants doit être conforme aux réglementations environnementales afin d'éviter la contamination de l'eau et du sol par le mercure.

Limites de température
Le SCE est également limité par sa plage de température de fonctionnement. Le SCE standard est généralement utilisé à des températures allant jusqu'à 50°C. Au-delà de cette température, la stabilité de l'électrode peut être compromise, ce qui peut entraîner des imprécisions dans les mesures. Pour les applications nécessitant des températures plus élevées, d'autres électrodes de référence, telles que l'électrode de chlorure d'argent-argent (Ag/AgCl), sont souvent préférées.
Compatibilité chimique
La composition chimique de l'échantillon mesuré est une autre considération essentielle. Certains produits chimiques peuvent dégrader les matériaux utilisés dans la construction de la SCE, tels que le corps en verre ou en époxy. Cela peut entraîner une réduction de la durée de vie de l'électrode et une contamination potentielle de l'échantillon. Il est essentiel de sélectionner le matériau approprié pour l'électrode en fonction de l'application spécifique afin de garantir la compatibilité et la longévité.
Conclusion
En conclusion, bien que l'électrode au calomel saturé (SCE) soit une électrode de référence fiable et largement utilisée, elle n'est pas sans limites. L'interférence potentielle avec certains ions, la nécessité d'une compensation de potentiel, les problèmes d'environnement et de sécurité liés à la teneur en mercure, les limites de température et la compatibilité chimique sont autant de facteurs à prendre en compte lors de la sélection d'une électrode de référence pour une application spécifique. En comprenant ces limitations, les chercheurs et les techniciens peuvent prendre des décisions éclairées pour garantir des mesures précises et fiables dans leurs expériences électrochimiques.
Applications des électrodes de calomel saturées
L'électrode de calomel saturée (SCE) est une électrode de référence largement utilisée dans diverses applications scientifiques et industrielles en raison de son potentiel stable et de sa facilité d'utilisation. Cette section explore les diverses applications de l'ECS dans différents domaines, y compris les laboratoires, les études environnementales et les processus industriels, tout en notant les conditions spécifiques dans lesquelles son utilisation n'est pas recommandée.
Applications en laboratoire
En laboratoire, la SCE est fréquemment utilisée dans les mesures électrochimiques telles que la détermination du pH, les mesures du potentiel d'oxydoréduction et les études de corrosion. La stabilité du potentiel SCE permet d'obtenir des résultats précis et reproductibles, ce qui en fait un choix privilégié pour de nombreux chercheurs. Par exemple, dans les mesures de pH, la SCE est associée à une électrode de verre pour déterminer avec précision le pH des solutions. Le potentiel de la SCE reste constant, fournissant un point de référence fiable auquel le potentiel de l'électrode de verre peut être comparé.

Études environnementales
La SCE est largement utilisée dans les études environnementales pour mesurer le potentiel redox des masses d'eau, ce qui est crucial pour évaluer la qualité de l'eau et la santé des écosystèmes aquatiques. Le potentiel redox indique les conditions oxydantes ou réductrices de l'eau, qui peuvent influencer la survie et l'activité de divers micro-organismes et la transformation des polluants. Par exemple, en surveillant l'impact des effluents industriels sur l'eau des rivières, le SCE aide à déterminer l'ampleur du stress oxydatif causé par les polluants.
Procédés industriels
Dans les processus industriels, la SCE est utilisée pour la surveillance et le contrôle de la corrosion. Il est particulièrement utile dans l'industrie du pétrole et du gaz, où il permet d'évaluer les taux de corrosion des métaux en contact avec des environnements agressifs. En surveillant la différence de potentiel entre la SCE et l'électrode de travail, les industries peuvent prévoir et prévenir la corrosion, prolongeant ainsi la durée de vie des équipements et réduisant les coûts de maintenance.
Limites et alternatives
Malgré son utilisation répandue, il existe des conditions spécifiques dans lesquelles l'utilisation de la SCE n'est pas recommandée. L'une des principales limites est sa plage de température, qui est limitée à 50°C. Au-delà de cette température, le potentiel du SCE devient instable, ce qui entraîne des mesures imprécises. En outre, la présence de certains ions, tels que K+ et Cl-, peut interférer avec les réactions électrochimiques, ce qui rend la SCE inadaptée à ces applications.
Dans ce cas, d'autres électrodes de référence, telles que l'électrode argent/chlorure d'argent (Ag/AgCl), sont utilisées. L'électrode Ag/AgCl est stable à des températures plus élevées et est moins sensible aux interférences de certains ions, ce qui en fait un choix approprié pour les applications où la SCE n'est pas réalisable.
Conclusion
L'électrode au calomel saturé reste un outil essentiel dans diverses applications scientifiques et industrielles en raison de sa stabilité et de sa facilité d'utilisation. Ses applications vont des mesures en laboratoire à la surveillance de l'environnement et au contrôle des processus industriels. Toutefois, il est essentiel de comprendre ses limites et de savoir quand utiliser d'autres électrodes de référence pour obtenir des résultats précis et fiables. Au fur et à mesure que la technologie progresse, le développement de nouvelles électrodes de référence aux performances améliorées continuera d'élargir le champ des applications dans lesquelles ces outils essentiels peuvent être utilisés.
Comparaison avec d'autres électrodes de référence
Lors d'expériences électrochimiques, le choix de l'électrode de référence est crucial car elle fournit un potentiel stable et défini par rapport auquel les potentiels des autres électrodes peuvent être mesurés. Les électrodes de référence courantes comprennent l'électrode au calomel saturée (SCE), l'électrode argent/chlorure d'argent (Ag/AgCl), l'électrode cuivre/sulfate de cuivre (Cu/CuSO4) et l'électrode standard à hydrogène (SHE). Chacune de ces électrodes présente ses propres avantages et inconvénients, ce qui les rend adaptées à différents contextes.
Électrode au calomel saturé (SCE)
La SCE est largement utilisée en raison de sa stabilité et de sa facilité de préparation. Elle se compose de mercure en contact avec une solution saturée de chlorure de potassium (KCl) et de calomel (Hg2Cl2). Le potentiel du SCE est de +0,241 V par rapport au SHE, ce qui est une valeur connue et constante. Cela en fait une référence fiable dans de nombreux systèmes aqueux. Cependant, son utilisation est limitée aux températures inférieures à 50°C en raison de la solubilité du calomel, et il n'est pas adapté aux systèmes non aqueux en raison de l'introduction de potentiels de jonction non définis.
Argent/Chlorure d'argent (Ag/AgCl)
L'électrode Ag/AgCl est un autre choix populaire, en particulier dans les applications non aqueuses et à haute température. Elle consiste en un fil d'argent recouvert de chlorure d'argent et immergé dans une solution de KCl. Le potentiel de l'électrode Ag/AgCl varie légèrement en fonction de la concentration de KCl, mais il est généralement compris entre +0,197 V et +0,222 V par rapport au SHE. L'un des principaux avantages de l'électrode Ag/AgCl est sa stabilité dans une large gamme de températures et de solvants, ce qui la rend polyvalente pour diverses applications. Cependant, elle peut être sensible à la contamination par les ions chlorure, ce qui affecte son potentiel.
Sulfate de cuivre/cuivre (Cu/CuSO4)
L'électrode Cu/CuSO4 est souvent utilisée dans les applications de terrain en raison de sa simplicité et de sa robustesse. Elle consiste en une tige de cuivre immergée dans une solution saturée de sulfate de cuivre. Le potentiel de l'électrode Cu/CuSO4 est de +0,314 V par rapport au SHE, ce qui est relativement stable. Cette électrode est particulièrement utile dans les études sur le sol et l'eau où une référence durable et facile à entretenir est nécessaire. Cependant, son potentiel peut être affecté par la pureté du cuivre et la concentration de la solution de sulfate de cuivre.

Électrode standard à hydrogène (SHE)
L'électrode SHE est le principal étalon de mesure des potentiels d'électrode, avec un potentiel défini de 0,000 V. Elle se compose d'une électrode de platine dans une solution avec une concentration de 1 M d'ions hydrogène, en contact avec de l'hydrogène gazeux à une pression de 1 atmosphère. Bien que la SHE soit l'électrode de référence idéale, elle n'est pas pratique pour une utilisation courante en raison de sa complexité, de la nécessité d'utiliser de l'hydrogène gazeux pur et d'un contrôle précis des conditions. Elle est plus couramment utilisée comme référence théorique dans les tables de potentiel de réduction standard.
Comparaison et adaptation au contexte
Chaque électrode de référence possède son propre ensemble d'avantages et de limites, ce qui la rend adaptée à différentes applications. L'électrode SCE est fiable et facile à préparer, ce qui en fait un choix populaire dans de nombreux laboratoires. L'électrode Ag/AgCl offre une polyvalence en termes de température et de solvant, ce qui est bénéfique pour les applications non aqueuses et à haute température. L'électrode Cu/CuSO4 est robuste et simple, idéale pour le travail sur le terrain et les études environnementales. L'électrode SHE, bien qu'étant l'étalon principal, n'est pas pratique pour une utilisation de routine mais reste essentielle à des fins théoriques et d'étalonnage.
En résumé, le choix de l'électrode de référence doit être basé sur les exigences spécifiques de l'expérience, y compris la plage de température, le type de solvant et le besoin de stabilité et de facilité d'utilisation. En comprenant les avantages et les inconvénients relatifs de chaque électrode de référence, les chercheurs peuvent prendre des décisions éclairées pour garantir des mesures électrochimiques précises et fiables.
Sélection et considérations
Lors de la sélection d'une électrode de référence pour des mesures électrochimiques, plusieurs facteurs doivent être pris en compte pour garantir des résultats précis et fiables. Le choix de l'électrode de référence a un impact significatif sur la qualité des données obtenues, et la compréhension des nuances de chaque type peut aider à prendre une décision éclairée.
Types d'électrodes de référence

Les électrodes de référence sont des composants essentiels des mesures électrochimiques, car elles fournissent un potentiel stable et reproductible par rapport auquel d'autres potentiels peuvent être mesurés. Les types d'électrodes les plus courants sont les suivants
- Argent/chlorure d'argent (Ag/AgCl) : Largement utilisé en raison de sa stabilité et de son coût relativement faible. Elle convient à un large éventail d'applications, y compris les mesures de pH et l'analyse électrochimique générale.
- Électrode de calomel saturée (SCE) : Connue pour sa stabilité et sa facilité de préparation, elle est cependant moins utilisée aujourd'hui en raison des préoccupations environnementales liées au mercure.
- Oxyde de mercure/mercure(I) (Hg/Hg2O) : Offre une bonne stabilité mais est moins utilisé en raison de préoccupations environnementales similaires à celles du SCE.
- Sulfate de mercure (Hg/Hg2SO4) : Convient aux applications à haute température mais doit être manipulé avec précaution en raison de sa teneur en mercure.
- Cuivre/sulfate de cuivre (Cu/CuSO4) : Souvent utilisé pour la surveillance des sols et des eaux souterraines en raison de sa stabilité dans les environnements aqueux.
Principales considérations
Compatibilité de l'échantillon
L'électrode de référence doit être chimiquement compatible avec l'échantillon afin d'éviter toute interaction susceptible de modifier le potentiel ou de réagir avec le matériau de l'électrode. Par exemple, certains solvants organiques peuvent dissoudre certains matériaux d'électrode, tandis que des ions agressifs comme le fluorure peuvent attaquer le verre ou d'autres composants sensibles.
Stabilité requise du potentiel
La stabilité est essentielle pour obtenir des mesures précises. Une électrode de référence stable garantit que le potentiel reste constant dans le temps et dans des conditions variables. Les électrodes Ag/AgCl, par exemple, sont connues pour leur excellente stabilité de potentiel, ce qui en fait un choix populaire dans de nombreuses applications.
Temps de réponse
Le temps de réponse d'une électrode de référence correspond à la rapidité avec laquelle elle atteint un potentiel stable après avoir été immergée dans l'échantillon. Des temps de réponse plus rapides sont généralement préférés car ils améliorent l'efficacité du processus analytique. Certaines électrodes, en particulier celles qui ont des jonctions poreuses, peuvent avoir des temps de réponse plus lents en raison de limitations de la diffusion.
Considérations relatives à la température
La température peut affecter de manière significative le potentiel d'une électrode de référence. La plupart des électrodes de référence sont conçues pour être utilisées dans des plages de température spécifiques. Par exemple, la SCE est généralement limitée à 50°C. Les applications exigeant des températures plus élevées peuvent nécessiter l'utilisation d'électrodes alternatives, telles que Hg/Hg2SO4, qui peuvent fonctionner à des températures plus élevées.
Composition chimique de l'échantillon
La composition chimique de l'échantillon doit être prise en compte pour sélectionner une électrode qui ne se dégradera pas ou ne réagira pas avec les composants de l'échantillon. Par exemple, certains produits chimiques peuvent corroder le corps de l'électrode, ce qui nécessite l'utilisation de matériaux tels que le verre, l'époxy ou d'autres matériaux résistants.
Considérations pratiques
Lors du changement de la solution de remplissage de référence, il est important de noter que le nouveau potentiel peut être moins stable et plus sensible aux changements de température. Laisser l'électrode reposer pendant une nuit avec la nouvelle solution de remplissage peut aider à établir un potentiel stable. Dans la pratique, de nombreux utilisateurs choisissent d'acheter des électrodes de référence séparées dédiées à des solutions de remplissage spécifiques plutôt que de changer fréquemment de solution de remplissage.
Conclusion
Le choix de l'électrode de référence appropriée implique un examen minutieux de la compatibilité de l'échantillon, de la stabilité du potentiel requise, du temps de réponse et des considérations relatives à la température. En comprenant les forces et les faiblesses des différents types d'électrodes de référence et leur compatibilité avec divers types d'échantillons, les utilisateurs peuvent garantir des mesures électrochimiques précises et fiables.
Produits associés
- Électrode de référence au calomel, chlorure d'argent, sulfate de mercure pour usage en laboratoire
- Électrode de référence au sulfate de cuivre pour usage en laboratoire
- Électrode en feuille de platine pour applications de laboratoire et industrielles
Articles associés
- Notions d'électrochimie : Conditions et précautions d'utilisation des différentes électrodes de référence
- Comment choisir la bonne électrode de référence pour votre application
- Électrodes de référence : Calomel, chlorure d'argent et sulfate de mercure - Un guide complet
- Utilisation et entretien des électrodes de référence
- Électrodes de référence communes dans les études électrochimiques