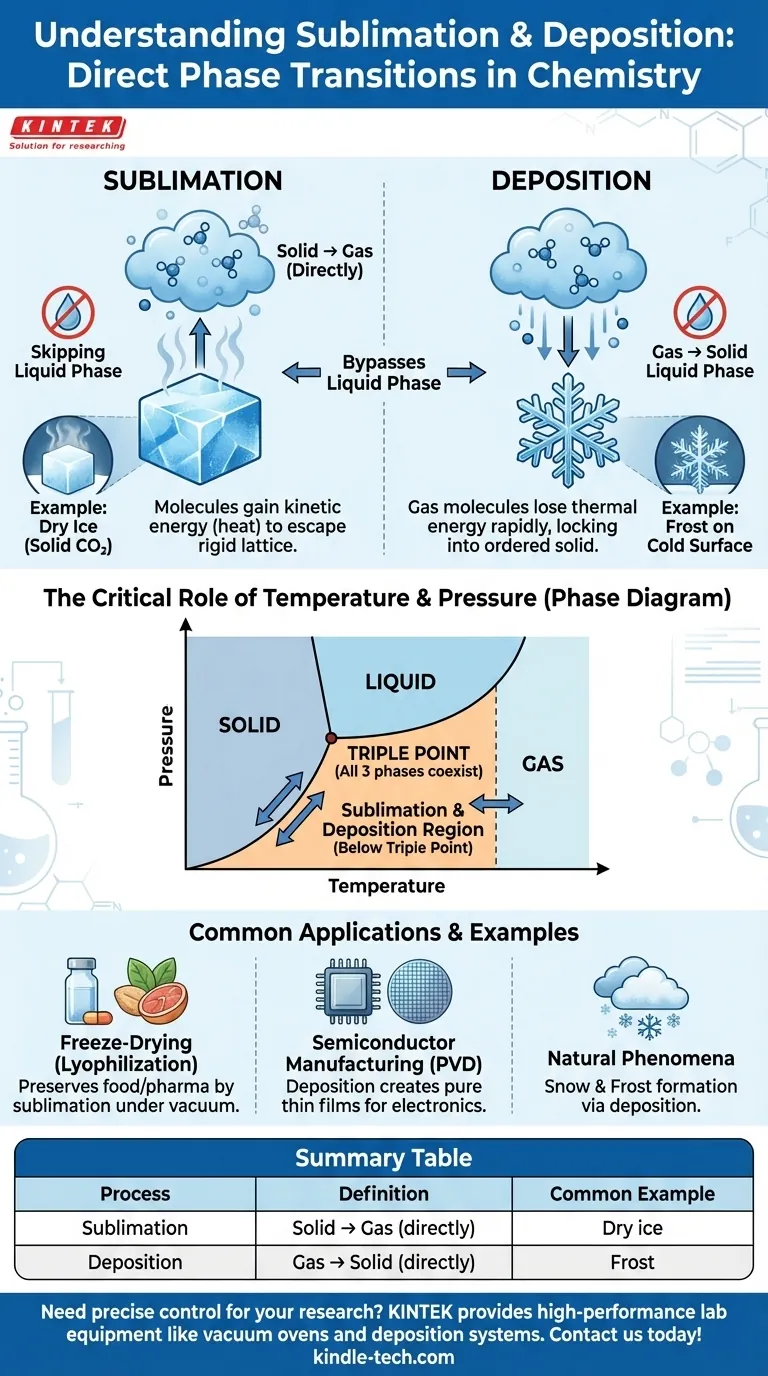
Dans l'étude de la matière, la sublimation et le dépôt sont des transitions de phase où une substance passe directement de son état solide à son état gazeux, en contournant complètement la phase liquide. La sublimation est la conversion directe d'un solide en gaz. Le dépôt est le processus inverse, où un gaz se transforme directement en solide.
Le principe fondamental à comprendre est que la sublimation et le dépôt sont les deux faces d'une même pièce. Ils représentent le chemin direct et bidirectionnel entre les phases solide et gazeuse qui se produit dans des conditions spécifiques de température et de pression, en sautant entièrement l'état liquide intermédiaire.

La mécanique des transitions de phase
Pour comprendre pourquoi une substance sauterait la phase liquide, nous devons examiner l'énergie et l'arrangement de ses molécules. Les transitions de phase concernent fondamentalement les changements d'énergie moléculaire et de liberté de mouvement.
Sublimation : la transition solide-gaz
Dans un solide, les molécules sont enfermées dans une structure fixe, souvent cristalline, bien qu'elles vibrent toujours sur place.
Lorsque de l'énergie (généralement sous forme de chaleur) est ajoutée, ces vibrations augmentent. En sublimation, les molécules acquièrent suffisamment d'énergie cinétique pour surmonter les forces intermoléculaires qui les maintiennent dans leur réseau rigide et s'échapper directement sous forme de gaz.
Un exemple classique est la glace sèche, qui est du dioxyde de carbone solide. À température ambiante et pression standard, elle se transforme directement en dioxyde de carbone gazeux sans jamais devenir une flaque liquide.
Dépôt : la transition gaz-solide
Le dépôt est l'opposé de la sublimation. Il se produit lorsque les molécules en phase gazeuse perdent rapidement de l'énergie thermique.
Cette perte rapide d'énergie fait ralentir si considérablement les molécules de gaz en mouvement rapide qu'elles se bloquent directement dans une structure solide ordonnée. Elles n'ont pas la possibilité de se condenser d'abord en liquide.
La formation de givre sur une vitre froide en est un exemple parfait. La vapeur d'eau dans l'air entre en contact avec une surface sous le point de congélation et se transforme directement en cristaux de glace.
Le rôle critique de la température et de la pression
Qu'une substance sublime, fonde ou bouille n'est pas une propriété intrinsèque de la substance seule. Cela est déterminé par les conditions externes de température et de pression, qui sont mieux visualisées sur un diagramme de phase.
Présentation du point triple
Pour chaque substance, il existe une combinaison spécifique de température et de pression appelée le point triple. C'est le point unique où les phases solide, liquide et gazeuse peuvent coexister en équilibre thermodynamique.
Pourquoi le saut de la phase liquide se produit
La sublimation et le dépôt se produisent à des combinaisons de température et de pression inférieures au point triple.
À ces basses pressions, la phase liquide n'est pas stable. L'ajout d'énergie à un solide le poussera directement au-delà de la limite dans la phase gazeuse (sublimation), et le retrait d'énergie d'un gaz le fera passer directement dans la phase solide (dépôt).
Applications et exemples courants
Ces processus ne sont pas seulement des concepts théoriques ; ils sont au cœur des phénomènes naturels et des technologies industrielles critiques.
La sublimation en action : la lyophilisation
La lyophilisation est une méthode clé pour conserver les aliments et les produits pharmaceutiques. Le matériau est d'abord congelé, puis la pression ambiante est considérablement réduite, ce qui provoque la sublimation de l'eau congelée (glace) directement en vapeur d'eau, laissant l'article sec sans dommage thermique.
Le dépôt en technologie : la fabrication de semi-conducteurs
Dans l'industrie technologique, un processus appelé dépôt physique en phase vapeur (PVD) est utilisé pour créer des films minces. Un matériau solide est vaporisé sous vide, et le gaz résultant se dépose ensuite sous forme de film solide pur sur un substrat, tel qu'une tranche de silicium utilisée pour fabriquer des puces informatiques.
Phénomènes naturels : neige et givre
La formation de neige dans les nuages est un exemple naturel de dépôt. La vapeur d'eau dans l'atmosphère se refroidit et se dépose directement en cristaux de glace complexes, formant des flocons de neige qui n'ont jamais existé sous forme de gouttes de pluie liquides.
Faire le bon choix pour votre objectif
Comprendre ces concepts vous permet d'interpréter les processus naturels et industriels avec une plus grande clarté.
- Si votre objectif principal est de visualiser les phénomènes quotidiens : Rappelez-vous que la "fumée" de la glace sèche est de la sublimation, et le givre sur votre pelouse par un matin froid est du dépôt.
- Si votre objectif principal est de comprendre les processus industriels : Reconnaissez que la lyophilisation utilise la sublimation pour éliminer l'eau en douceur, tandis que la création d'électronique avancée repose souvent sur le dépôt pour construire des composants couche par couche.
- Si votre objectif principal est de saisir la chimie physique fondamentale : Ancrez votre compréhension au diagramme de phase, où tout comportement en dessous du point triple implique des transitions directes solide-gaz.
En fin de compte, la sublimation et le dépôt démontrent comment l'état de la matière est une condition dynamique régie par l'interaction de l'énergie et de la pression.
Tableau récapitulatif :
| Processus | Définition | Exemple courant |
|---|---|---|
| Sublimation | Solide → Gaz (directement) | Glace sèche (CO₂ solide) se transformant en gaz |
| Dépôt | Gaz → Solide (directement) | Formation de givre sur une fenêtre froide |
| Condition clé | Se produit à des températures et pressions inférieures au point triple de la substance | - |
Besoin d'un contrôle précis de la température et de la pression pour vos recherches sur les transitions de phase ou vos processus industriels ? KINTEK est spécialisé dans les équipements de laboratoire haute performance, y compris les fours sous vide et les systèmes de dépôt, pour atteindre de manière fiable les conditions nécessaires à la sublimation et au dépôt. Laissez nos experts vous aider à choisir les bons outils pour les défis uniques de votre laboratoire. Contactez-nous dès aujourd'hui pour discuter de votre application !
Guide Visuel