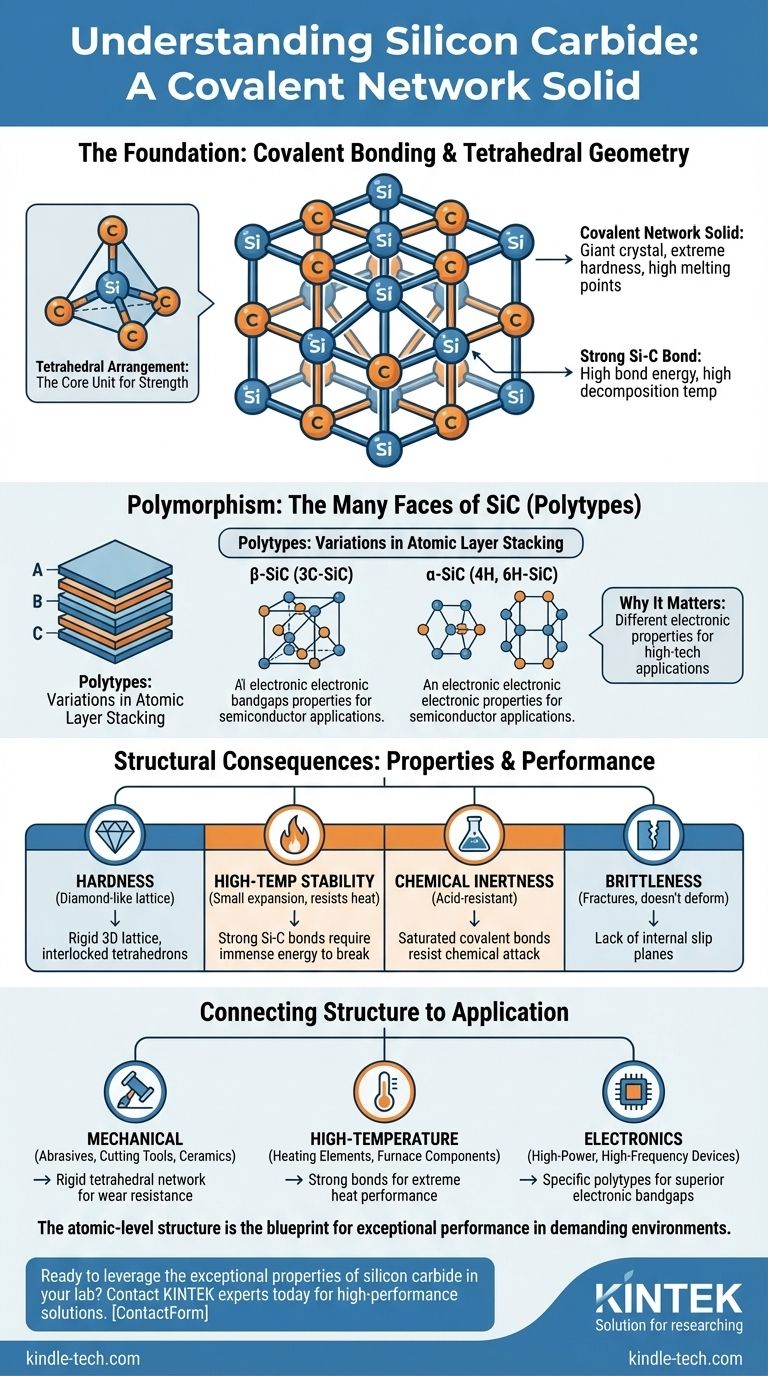
À la base, le carbure de silicium (SiC) est un solide à réseau covalent. Cela signifie que sa structure fondamentale est un vaste réseau cristallin tridimensionnel construit à partir d'atomes de silicium (Si) et de carbone (C). Chaque atome est fermement verrouillé en place par de fortes liaisons covalentes selon un motif tétraédrique répétitif, tout comme la structure du diamant. Cet arrangement peut se former selon de nombreuses variations d'empilement, connues sous le nom de polytypes.
La question de la structure du carbure de silicium est centrale pour comprendre ses propriétés remarquables. Son réseau covalent rigide, semblable à celui du diamant, est la cause directe de sa dureté exceptionnelle, de sa stabilité chimique et de sa capacité à résister à des températures extrêmes.

Le fondement : la liaison covalente et la géométrie tétraédrique
Comprendre le SiC commence par son arrangement atomique. Contrairement aux métaux avec des électrons libres ou aux sels maintenus par attraction ionique, la force du SiC provient de liaisons électroniques fortes et partagées qui créent une seule molécule massive.
Qu'est-ce qu'un solide à réseau covalent ?
Un solide à réseau covalent est une substance où les atomes sont liés par des liaisons covalentes dans un réseau continu s'étendant à travers le matériau. Il n'y a pas de molécules individuelles.
Le cristal entier est essentiellement une seule molécule géante. Cette structure est responsable de la dureté extrême et des points de fusion élevés de matériaux comme le diamant et le carbure de silicium.
L'arrangement tétraédrique
Dans le réseau du SiC, chaque atome de silicium est chimiquement lié à quatre atomes de carbone voisins. De même, chaque atome de carbone est lié à quatre atomes de silicium voisins.
Cet arrangement forme un tétraèdre, une forme géométrique très stable et symétrique. Ce motif répétitif de tétraèdres entrelacés crée une armature incroyablement solide et rigide.
La force de la liaison Si-C
La liaison entre le silicium et le carbone est très forte et relativement courte. Une quantité importante d'énergie est nécessaire pour la rompre.
Cette énergie de liaison élevée est la source directe de la température de décomposition élevée du SiC (il se sublime plutôt que de fondre) et de sa dureté exceptionnelle, qui n'est surpassée que par très peu de matériaux.
Polymorphisme : les multiples facettes du carbure de silicium
Le carbure de silicium n'est pas une structure unique. Il présente un phénomène appelé polymorphisme, ce qui signifie qu'il peut exister sous de nombreuses structures cristallines différentes tout en conservant la même formule chimique (SiC). Ces différentes formes sont appelées polytypes.
Comprendre les polytypes
Les polytypes sont des variations dans la séquence d'empilement des couches atomiques dans le cristal. Imaginez empiler des couches d'atomes représentées par A, B et C. Différents motifs répétitifs (comme ABCABC... ou ABAB...) donnent des structures cristallines différentes.
Bien que chimiquement identiques, ces polytypes peuvent avoir des propriétés physiques et, surtout, électroniques distinctes.
Catégories clés : α-SiC et β-SiC
Les centaines de polytypes de SiC connus sont largement regroupés en deux catégories principales.
Le Bêta-SiC (β-SiC) fait référence au polytype cubique (3C-SiC), qui a une structure similaire à celle de la blende. L'Alpha-SiC (α-SiC) englobe tous les autres polytypes, qui sont principalement hexagonaux (comme 4H-SiC et 6H-SiC) ou rhomboédriques.
Pourquoi les polytypes sont importants pour les applications
L'existence des polytypes n'est pas seulement un détail académique ; elle est essentielle pour les applications de haute technologie. Différents polytypes ont des bandes interdites électroniques différentes, ce qui détermine leurs propriétés semi-conductrices.
Par exemple, le polytype 4H-SiC est privilégié pour les dispositifs électroniques de puissance et de haute fréquence, car ses propriétés électroniques sont supérieures à cette fin spécifique, ce qui soutient son utilisation dans le domaine des semi-conducteurs avancés.
Comprendre les conséquences structurelles
Les propriétés énumérées pour le carbure de silicium — dureté, stabilité et résistance à la température — sont toutes des conséquences directes de sa structure atomique sous-jacente.
Dureté extrême, mais grande fragilité
La référence indique que le SiC est « dur et cassant ». Le réseau covalent rigide qui lui confère sa dureté extrême signifie également qu'il manque des plans de glissement internes trouvés dans les métaux.
Lorsqu'il est soumis à une contrainte dépassant ce que les liaisons peuvent supporter, le cristal ne peut pas se déformer en permettant aux atomes de glisser les uns par rapport aux autres. Au lieu de cela, il se fracture de manière catastrophique, ce qui est la définition de la fragilité.
Stabilité à haute température
Les puissantes liaisons Si-C nécessitent une énergie thermique immense pour vibrer et se briser. C'est pourquoi le SiC est décrit comme ayant un « faible coefficient de dilatation » et une « bonne résistance au refroidissement rapide et à la chaleur ».
Cette stabilité thermique en fait un matériau idéal pour les éléments chauffants électriques à haute température et les composants de four, car il conserve son intégrité structurelle à des températures où la plupart des métaux fondraient ou se déformeraient.
Inertie chimique
La référence souligne la « bonne stabilité chimique » du SiC et note qu'il est « extrêmement résistant aux acides ». Les liaisons covalentes saturées et stables ne sont pas facilement attaquées ou rompues par les réactifs chimiques.
Les électrons sont étroitement verrouillés entre les atomes de silicium et de carbone, laissant peu de possibilités aux acides ou autres produits chimiques de réagir, ce qui donne un matériau très durable et non réactif.
Relier la structure à l'application
Comprendre la structure atomique du carbure de silicium vous permet de le sélectionner avec confiance pour le bon usage. Les propriétés ne sont pas arbitraires ; elles sont le résultat direct de son réseau covalent.
- Si votre objectif principal est la résistance mécanique et à l'usure : Le réseau tétraédrique rigide et interconnecté fait du SiC un choix idéal pour les abrasifs, les outils de coupe et les céramiques structurelles durables.
- Si votre objectif principal est la performance à haute température : L'énergie élevée requise pour rompre ses liaisons Si-C le rend parfait pour les éléments chauffants, les composants de four et les matériaux réfractaires.
- Si votre objectif principal est l'électronique avancée : Les propriétés électroniques distinctes de certains polytypes, comme le 4H-SiC, sont essentielles pour créer la prochaine génération de dispositifs semi-conducteurs de puissance et à haute fréquence.
En fin de compte, la structure au niveau atomique du carbure de silicium est le plan direct de ses performances exceptionnelles dans les environnements les plus exigeants du monde.
Tableau récapitulatif :
| Propriété | Conséquence de la structure |
|---|---|
| Dureté | Réseau covalent rigide en 3D de tétraèdres entrelacés |
| Stabilité à haute température | Les liaisons Si-C fortes nécessitent une énergie immense pour se rompre |
| Inertie chimique | Les liaisons covalentes saturées résistent à l'attaque chimique |
| Fragilité | L'absence de plans de glissement dans le réseau rigide entraîne une fracture |
| Polytypes (ex. 4H-SiC) | Les différentes séquences d'empilement des couches atomiques permettent des applications semi-conductrices avancées |
Prêt à tirer parti des propriétés exceptionnelles du carbure de silicium dans votre laboratoire ?
Chez KINTEK, nous sommes spécialisés dans les équipements de laboratoire et les consommables haute performance conçus pour prospérer dans des environnements exigeants. Que votre application nécessite une résistance extrême à l'usure, une stabilité à haute température ou des capacités semi-conductrices avancées, notre expertise en science des matériaux peut vous aider à obtenir des résultats supérieurs.
Contactez nos experts dès aujourd'hui pour discuter de la manière dont nos solutions en carbure de silicium peuvent améliorer l'efficacité et les capacités de votre laboratoire.
Guide Visuel