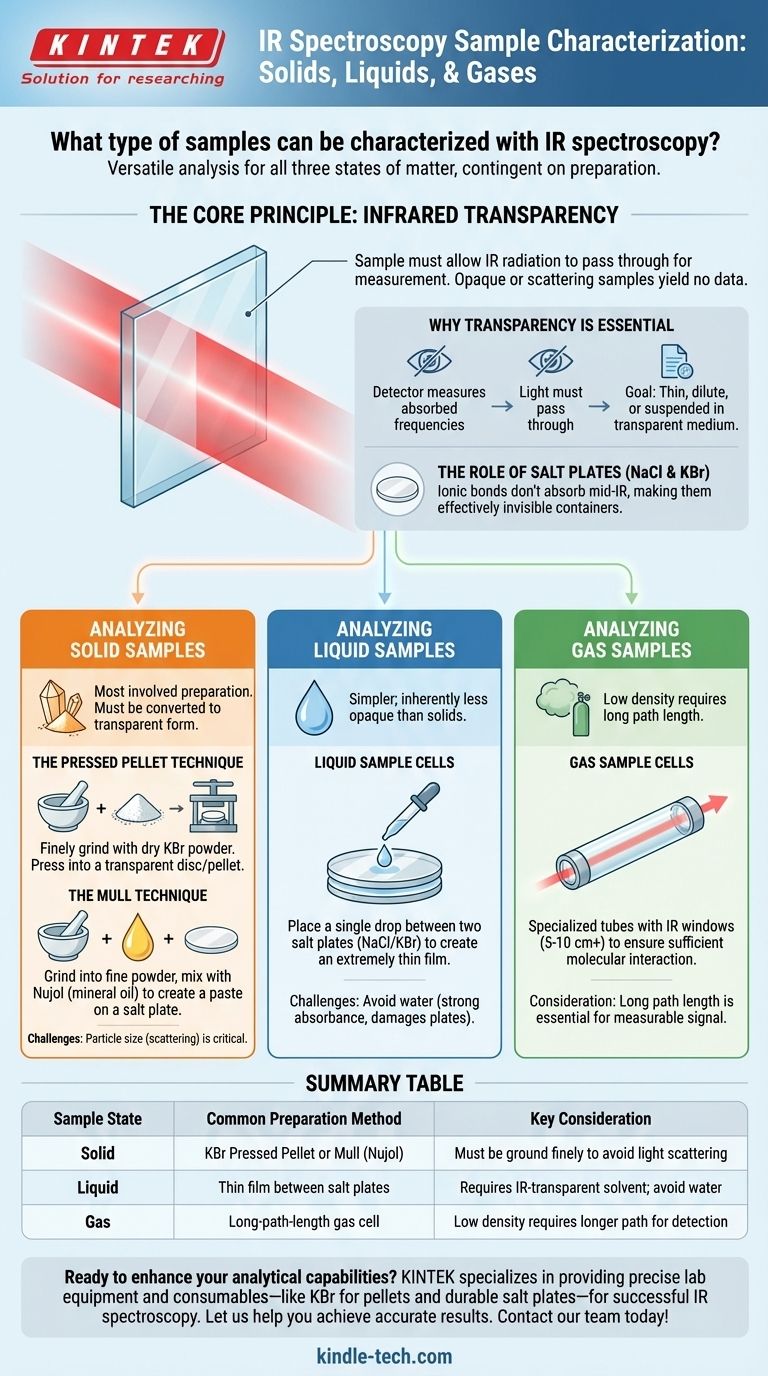
En bref, la spectroscopie IR est une technique remarquablement polyvalente capable d'analyser des échantillons dans les trois états de la matière principaux : solide, liquide et gaz. La clé n'est pas l'état physique de l'échantillon lui-même, mais la manière dont il est préparé pour l'analyse.
L'exigence la plus importante pour tout échantillon destiné à la spectroscopie IR est la transparence aux infrarouges. L'échantillon, ainsi que tout matériau utilisé pour le maintenir ou le contenir, doit permettre au rayonnement IR de le traverser pour une mesure réussie.

Le principe fondamental : la transparence aux infrarouges
Pour comprendre quels échantillons peuvent être utilisés, nous devons d'abord comprendre comment fonctionne la technique. La spectroscopie IR mesure les fréquences spécifiques de la lumière infrarouge qui sont absorbées par les liaisons chimiques d'un échantillon.
Pourquoi la transparence est essentielle
Pour que le détecteur de l'instrument puisse mesurer quelles fréquences ont été absorbées, la lumière doit d'abord pouvoir traverser l'échantillon. Si l'échantillon est opaque ou diffuse trop la lumière, aucune donnée significative ne peut être collectée.
Ce principe dicte chaque aspect de la préparation de l'échantillon. L'objectif est toujours de créer un échantillon suffisamment mince, suffisamment dilué ou suspendu dans un milieu transparent au faisceau IR.
Le rôle des plaques de sel (NaCl et KBr)
Vous verrez souvent des matériaux comme le chlorure de sodium (NaCl) et le bromure de potassium (KBr) utilisés pour fabriquer des supports d'échantillons, des fenêtres et des pastilles. C'est parce que leurs liaisons ioniques n'absorbent pas la lumière dans la région de l'infrarouge moyen, ce qui les rend effectivement invisibles pour le spectromètre.
Analyse des échantillons solides
La préparation des échantillons solides est souvent le processus le plus complexe car ils doivent être convertis en une forme transparente au rayonnement IR.
La technique de la pastille pressée
La méthode la plus courante consiste à broyer finement une petite quantité de l'échantillon solide avec une poudre de sel sèche et transparente aux IR, généralement du bromure de potassium (KBr). Ce mélange est ensuite soumis à une pression immense pour former un petit disque ou une « pastille » transparente qui peut être placée directement dans le faisceau du spectromètre.
La technique du mull
Une méthode alternative consiste à broyer le solide en une poudre très fine, puis à le mélanger avec une goutte ou deux d'huile lourde, comme le Nujol (une huile minérale). Cela crée une pâte épaisse, ou « mull », qui est ensuite étalée sur une plaque de sel. Le spectre de l'huile lui-même doit être soustrait du résultat final.
Autres techniques pour les solides
Pour certains polymères, un échantillon peut être préparé en dissolvant le matériau dans un solvant approprié et en l'évaporant sur une plaque de sel, laissant un mince film coulé.
Analyse des échantillons liquides et gazeux
Les liquides et les gaz sont souvent plus simples à préparer car ils sont intrinsèquement moins opaques que les solides en vrac.
Cellules pour échantillons liquides
La méthode la plus simple pour les liquides consiste à placer une seule goutte entre deux plaques de sel polies (comme NaCl ou KBr). Les plaques sont pressées l'une contre l'autre pour créer un film extrêmement mince du liquide, ce qui est suffisant pour l'analyse.
Cellules pour échantillons gazeux
Les échantillons gazeux sont analysés à l'aide d'une cellule à gaz spécialisée. Ce sont des tubes dotés de fenêtres transparentes aux IR aux deux extrémités. Parce que les gaz ont une très faible densité et absorbent donc très peu de lumière IR, ces cellules doivent avoir une longueur de trajet très longue (souvent 5 à 10 cm ou plus) pour garantir qu'un nombre suffisant de molécules interagissent avec le faisceau pour produire un signal mesurable.
Comprendre les limites pratiques
Bien que polyvalente, la spectroscopie IR n'est pas sans défis, dont la plupart sont liés à la préparation de l'échantillon.
Le défi de l'eau
Les échantillons aqueux (à base d'eau) sont extrêmement difficiles à analyser. L'eau elle-même présente des bandes d'absorbance IR très fortes et larges qui peuvent masquer les signaux de l'échantillon. De plus, les plaques de sel les plus courantes (NaCl et KBr) sont solubles dans l'eau et seraient rapidement endommagées.
La préparation de l'échantillon est essentielle
Une mauvaise préparation est la source la plus fréquente de données erronées. Pour les solides, si les particules ne sont pas suffisamment broyées, elles diffuseront le faisceau IR au lieu de l'absorber, ce qui entraînera un spectre déformé et inutilisable.
Concentration et longueur de trajet
L'intensité d'un signal IR est proportionnelle à la concentration de l'échantillon et à la distance parcourue par la lumière à travers celui-ci. C'est pourquoi les liquides purs sont analysés dans des films très minces, tandis que les gaz à faible concentration nécessitent des longueurs de trajet très longues.
Faire le bon choix pour votre échantillon
Votre approche sera entièrement dictée par l'état physique et les propriétés du matériau que vous devez analyser.
- Si votre objectif principal est un solide pur : Les techniques de pastille de KBr et de mull sont des méthodes standard pour produire des données quantitatives de haute qualité.
- Si votre objectif principal est un liquide pur : Un film mince entre deux plaques de sel est la méthode d'analyse la plus rapide et la plus directe.
- Si votre objectif principal est un gaz : Vous aurez besoin d'une cellule à gaz à longue distance de trajet spécialisée pour obtenir un signal mesurable.
- Si votre échantillon est dissous dans un solvant : Vous devez vous assurer que le solvant lui-même est transparent dans la région IR d'intérêt et utiliser une cellule liquide résistante à ce solvant.
En fin de compte, la réussite de l'analyse IR dépend moins de l'état de l'échantillon que de sa préparation correcte pour être transparent à la lumière infrarouge.
Tableau récapitulatif :
| État de l'échantillon | Méthode de préparation courante | Considération clé |
|---|---|---|
| Solide | Pastille pressée de KBr ou Mull (Nujol) | Doit être finement broyé pour éviter la diffusion de la lumière |
| Liquide | Film mince entre plaques de sel (NaCl/KBr) | Nécessite un solvant transparent aux IR ; éviter l'eau |
| Gaz | Cellule à gaz à longue distance de trajet | La faible densité nécessite une plus longue distance pour la détection |
Prêt à améliorer vos capacités analytiques ? KINTEK se spécialise dans la fourniture des équipements de laboratoire et des consommables précis — comme le KBr pour la préparation des pastilles et des plaques de sel durables — dont vous avez besoin pour une spectroscopie IR réussie. Nos experts comprennent le rôle critique d'une préparation d'échantillon adéquate. Laissez-nous vous aider à obtenir des résultats précis et fiables. Contactez notre équipe dès aujourd'hui pour discuter de vos besoins de laboratoire !
Guide Visuel