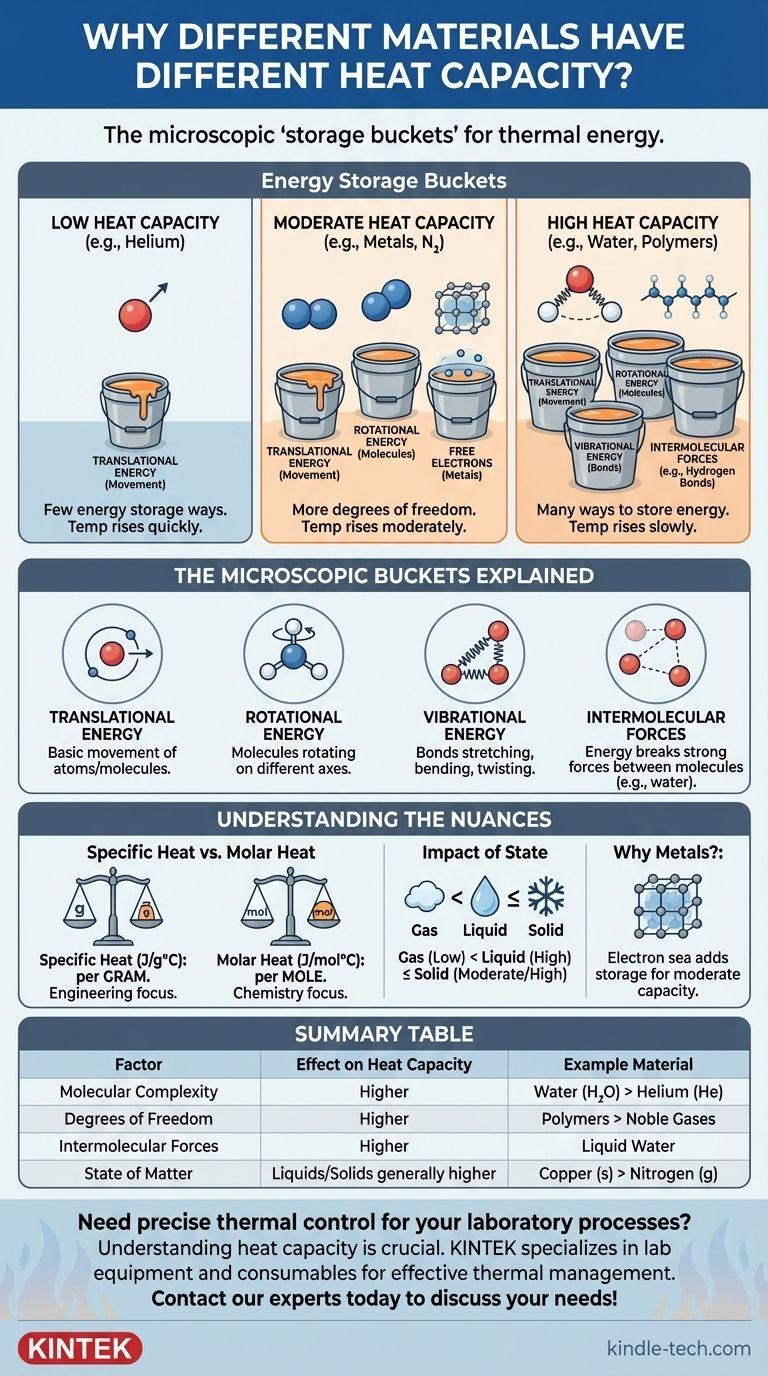
Au fond, la capacité thermique d'un matériau est déterminée par le nombre de façons dont il peut stocker de l'énergie thermique au niveau microscopique. Lorsque vous ajoutez de la chaleur, cette énergie ne fait pas seulement bouger les atomes plus vite ; elle est distribuée dans diverses "zones de stockage", telles que les rotations et les vibrations moléculaires. Les matériaux ayant des structures plus complexes ont plus de ces zones de stockage, ils nécessitent donc plus d'énergie pour atteindre la même augmentation de température.
Le point clé à retenir est le suivant : la capacité thermique est une mesure de la complexité et de la liberté moléculaires. Les matériaux avec des atomes simples (comme les gaz nobles) ont une faible capacité thermique, tandis que les matériaux avec des molécules complexes et de fortes forces intermoléculaires (comme l'eau) ont une capacité thermique élevée car ils ont beaucoup plus de façons d'absorber l'énergie au-delà du simple mouvement.

Qu'est-ce que la capacité thermique, vraiment ?
Pour comprendre les différences entre les matériaux, nous devons d'abord séparer les concepts de chaleur et de température.
Température vs. Chaleur
La température est une mesure de l'énergie cinétique moyenne des particules dans une substance. Considérez-la comme la vitesse moyenne des atomes ou des molécules lorsqu'ils se déplacent, s'agitent et vibrent.
La chaleur, d'autre part, est l'énergie thermique totale transférée vers ou depuis une substance. Lorsque vous ajoutez de la chaleur, vous ajoutez de l'énergie. Le rôle de cette énergie est d'augmenter l'énergie interne totale de la substance.
L'analogie du "stockage d'énergie"
Imaginez que vous avez plusieurs seaux vides. Ajouter de la chaleur, c'est comme y verser de l'eau. La température est comme le niveau d'eau dans un seul de ces seaux, celui étiqueté "Mouvement" (énergie cinétique).
La capacité thermique d'un matériau est déterminée par le nombre total de seaux qu'il possède. Si un matériau n'a qu'un seul seau ("Mouvement"), toute l'eau que vous y versez y va, et le niveau monte rapidement. Si un matériau a de nombreux seaux, vous devez verser beaucoup plus d'eau pour augmenter le niveau dans ce seau spécifique de "Mouvement".
Les seaux microscopiques : où l'énergie est stockée
Différents matériaux ont différents types de "seaux" microscopiques, formellement appelés degrés de liberté. Chacun offre une manière différente de stocker l'énergie thermique.
1. Énergie de translation (Le seau de base)
C'est l'énergie d'un atome ou d'une molécule se déplaçant d'un endroit à un autre. Tous les matériaux ont cela. C'est le principal contributeur à ce que nous mesurons comme température.
Pour une substance simple comme l'hélium gazeux, dont les atomes sont des sphères individuelles, c'est presque la seule façon de stocker de l'énergie. Sa capacité thermique est très faible.
2. Énergie de rotation (Pour les molécules)
Un seul atome ne peut pas tourner de manière significative pour stocker de l'énergie, mais une molécule le peut. Une molécule simple à deux atomes comme l'azote (N₂) peut tourner sur deux axes différents, comme un bâton qui tourne.
Une molécule non linéaire plus complexe comme l'eau (H₂O) peut tourner sur trois axes différents. Chaque axe de rotation est un autre "seau" pour stocker de l'énergie, augmentant sa capacité thermique.
3. Énergie de vibration (Un facteur de différenciation clé)
Les liaisons qui maintiennent les atomes ensemble dans une molécule ne sont pas des tiges rigides ; elles ressemblent davantage à des ressorts. Elles peuvent s'étirer, se plier et se tordre. Chacun de ces modes de vibration est un autre seau d'énergie très efficace.
Une molécule diatomique simple a un mode de vibration. Une molécule complexe avec de nombreux atomes et liaisons en a des dizaines. C'est une raison principale pour laquelle les substances complexes comme les huiles et les polymères ont des capacités thermiques plus élevées que les gaz simples.
4. Forces intermoléculaires (L'exemple de l'eau)
Dans les liquides et les solides, l'énergie est également utilisée pour travailler contre les forces entre les molécules. L'eau en est l'exemple ultime. Ses molécules sont liées par de fortes liaisons hydrogène.
Avant que les molécules d'eau ne puissent accélérer de manière significative (augmenter la température), une grande partie de l'énergie thermique ajoutée doit d'abord servir à secouer et à briser ces puissantes liaisons. Cela agit comme un énorme puits d'énergie, donnant à l'eau l'une des capacités thermiques spécifiques les plus élevées de toutes les substances courantes.
Comprendre les nuances
Lorsque l'on compare des matériaux, le contexte est essentiel. Regarder simplement un chiffre peut être trompeur sans comprendre ce qu'il représente.
Chaleur spécifique vs. Capacité thermique molaire
La capacité thermique spécifique est l'énergie requise pour élever un gramme d'une substance d'un degré Celsius (J/g°C). C'est utile pour l'ingénierie et les applications du monde réel où la masse est la principale préoccupation.
La capacité thermique molaire est l'énergie nécessaire pour élever une mole d'une substance d'un degré (J/mol°C). C'est souvent plus utile pour les physiciens et les chimistes, car elle compare un nombre égal de molécules, offrant une comparaison plus juste de la complexité moléculaire. Par exemple, la chaleur spécifique de l'eau est plus de quatre fois celle du cuivre, mais sa capacité thermique molaire n'est qu'environ trois fois plus grande.
L'impact de l'état (Gaz, Liquide, Solide)
La capacité thermique d'une substance change en fonction de son état.
- Les gaz ont des capacités thermiques plus faibles car leurs molécules sont éloignées et n'interagissent pas beaucoup.
- Les liquides ont des capacités plus élevées en raison de l'énergie nécessaire pour surmonter les forces intermoléculaires.
- Les solides stockent l'énergie dans un réseau collectif de vibrations (appelées phonons). Leur capacité est souvent similaire à leur forme liquide mais peut être plus faible à très basses températures.
Pourquoi les métaux ont une capacité thermique modérée
On pourrait s'attendre à ce que les métaux, étant des atomes simples, aient une faible capacité thermique. Leur capacité est modérée en raison de leur structure unique : un réseau rigide d'ions au sein d'une "mer" d'électrons libres. Cette mer d'électrons peut également absorber de l'énergie thermique, agissant comme un seau de stockage d'énergie supplémentaire que les gaz atomiques simples n'ont pas.
Faire le bon choix pour votre objectif
La façon dont vous interprétez les données de capacité thermique dépend entièrement de votre objectif.
- Si votre objectif principal est l'ingénierie ou la gestion thermique : Utilisez la capacité thermique spécifique (par gramme), car elle informe directement sur la quantité de chaleur qu'une masse donnée de matériau accumulera dans une conception réelle.
- Si votre objectif principal est la chimie ou la physique fondamentale : Comparez la capacité thermique molaire (par mole) pour isoler les effets de la structure moléculaire, des degrés de liberté et des liaisons sur le stockage d'énergie.
- Si votre objectif principal est la science du climat ou la biologie : Reconnaissez que la capacité thermique spécifique exceptionnellement élevée de l'eau, due aux liaisons hydrogène, est le facteur le plus important pour stabiliser le climat de la Terre et modérer la température corporelle chez les organismes vivants.
En fin de compte, la capacité thermique d'un matériau est la signature macroscopique de son monde microscopique.
Tableau récapitulatif :
| Facteur | Effet sur la capacité thermique | Exemple de matériau |
|---|---|---|
| Complexité moléculaire | Molécules plus complexes = capacité plus élevée | Eau (H₂O) vs. Hélium (He) |
| Degrés de liberté | Plus de façons de stocker l'énergie (rotation, vibration) = capacité plus élevée | Polymères vs. Gaz nobles |
| Forces intermoléculaires | Forces plus fortes (ex. liaisons hydrogène) = capacité plus élevée | Eau liquide |
| État de la matière | Liquides/Solides généralement plus élevés que les Gaz | Cuivre (solide) vs. Azote (gaz) |
| Électrons libres | La mer d'électrons dans les métaux ajoute une capacité modérée | Métaux comme l'aluminium |
Besoin d'un contrôle thermique précis pour vos processus de laboratoire ? Comprendre la capacité thermique est crucial pour des applications telles que la synthèse chimique, les tests de matériaux et l'analyse thermique. KINTEK est spécialisé dans les équipements et consommables de laboratoire, vous fournissant les outils dont vous avez besoin pour gérer efficacement l'énergie thermique. Que vous ayez besoin de fours, de chauffages ou de systèmes de surveillance de la température, nos solutions sont conçues pour la précision et la fiabilité. Contactez nos experts dès aujourd'hui pour discuter de la manière dont nous pouvons soutenir vos besoins spécifiques en laboratoire et améliorer vos résultats de recherche.
Guide Visuel