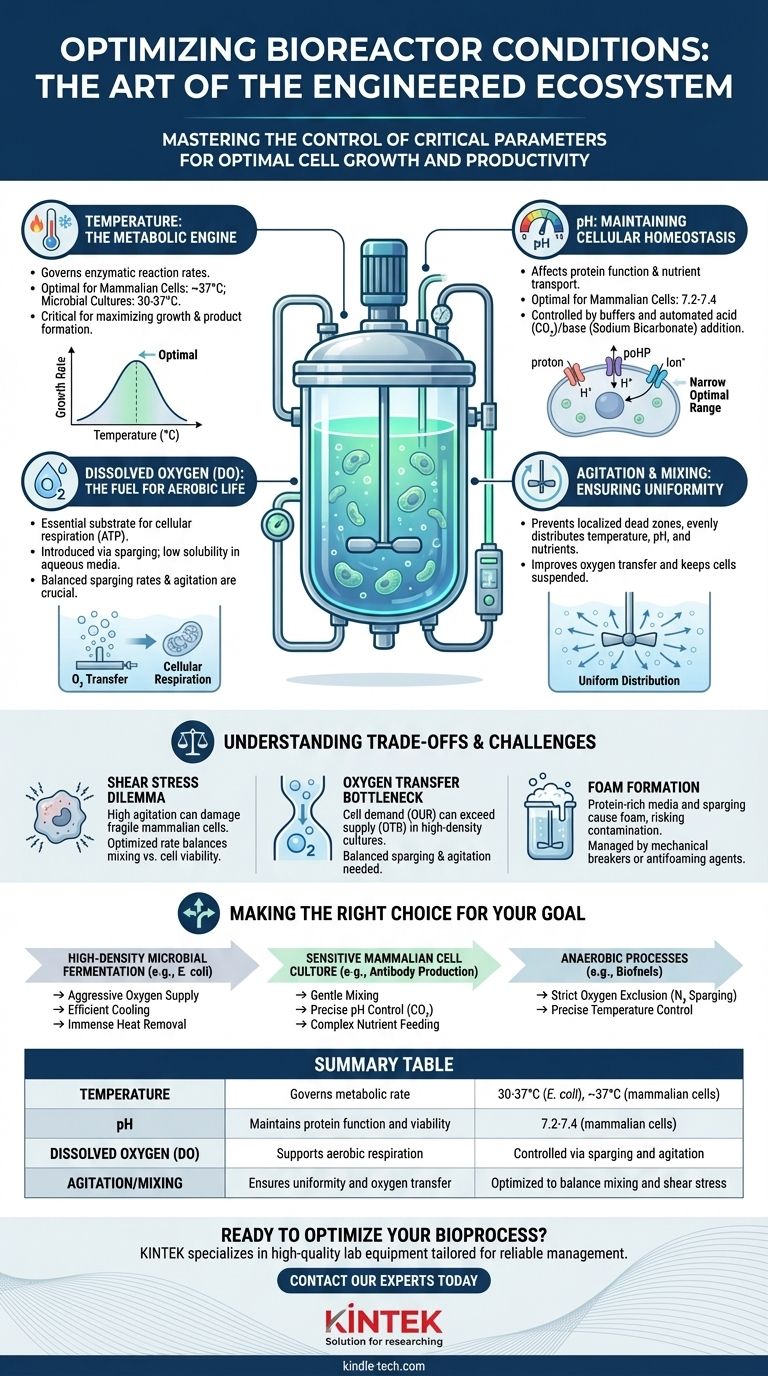
En bref, un bioréacteur contrôle méticuleusement un ensemble de conditions environnementales critiques pour assurer une croissance cellulaire et une productivité optimales. Les paramètres les plus fondamentaux maintenus sont la température, le pH, l'oxygène dissous (OD) et l'agitation pour le mélange. Celles-ci sont soutenues par un apport contrôlé de nutriments et l'élimination des déchets métaboliques.
Un bioréacteur n'est pas seulement un récipient ; c'est un écosystème conçu pour reproduire et optimiser l'environnement physiologique idéal pour une population spécifique de cellules ou de micro-organismes. Maîtriser le contrôle de ces conditions fait la différence entre un lot raté et un bioprocédé à haut rendement.

Les piliers fondamentaux du contrôle en bioréacteur
Pour obtenir une culture réussie, un bioréacteur doit gérer avec précision plusieurs variables interdépendantes. Chacune sert un objectif biologique distinct, et une défaillance dans l'une peut avoir des répercussions sur l'ensemble du système.
Température : Le moteur du métabolisme
La température régit directement la vitesse de toutes les réactions enzymatiques au sein des cellules, ce qui en fait l'un des paramètres les plus critiques.
Une température optimale maximise le taux métabolique pour la croissance et la formation de produits. Même un léger écart peut ralentir les processus ou, dans des cas extrêmes, provoquer des dommages irréversibles et la mort cellulaire. Par exemple, les cellules de mammifères (comme les cellules CHO) prospèrent autour de 37°C, tandis que de nombreuses cultures microbiennes (comme E. coli) préfèrent des températures comprises entre 30 et 37°C.
pH : Maintenir l'homéostasie cellulaire
Le pH du milieu de culture affecte la fonction des protéines, le transport des nutriments à travers la membrane cellulaire et la viabilité cellulaire globale.
Les cellules ont une plage de pH optimale très étroite. Pour les cellules de mammifères, elle se situe généralement entre 7,2 et 7,4. Les bioréacteurs maintiennent ce niveau en utilisant un système tampon dans le milieu et en ajoutant automatiquement un acide (souvent du CO₂ gazeux) ou une base (comme le bicarbonate de sodium) pour corriger tout écart causé par le métabolisme cellulaire.
Oxygène dissous (OD) : Le carburant de la vie aérobie
Pour les organismes aérobies, l'oxygène est un substrat essentiel à la respiration cellulaire, le processus principal de génération d'énergie (ATP).
La concentration en oxygène dissous (OD) est un facteur limitant clé car l'oxygène a une faible solubilité dans les milieux aqueux. Les bioréacteurs introduisent de l'oxygène par un processus appelé spargage, où de l'air filtré ou de l'oxygène pur est mis en bulles dans la culture. Le niveau d'OD doit être suffisamment élevé pour soutenir le métabolisme, mais pas trop élevé au point de devenir toxique par la création d'espèces réactives de l'oxygène.
Agitation et mélange : Assurer l'uniformité
Un bioréacteur n'est pas un environnement statique. Un mélange constant, entraîné par une turbine, est essentiel pour plusieurs raisons.
L'agitation assure que la température, le pH et les nutriments sont répartis uniformément dans tout le récipient, empêchant la formation de zones mortes localisées. Elle aide également à briser les bulles de gaz injectées pour améliorer le transfert d'oxygène dans le liquide et maintient les cellules en suspension de manière uniforme plutôt que de se déposer au fond.
Comprendre les compromis et les défis
Le maintien de ces conditions idéales est un exercice d'équilibrage constant, comportant plusieurs défis d'ingénierie inhérents.
Le dilemme des contraintes de cisaillement
Bien que l'agitation soit nécessaire au mélange, des vitesses de turbine élevées peuvent créer de puissantes forces hydrodynamiques appelées contraintes de cisaillement.
Les cellules microbiennes sont généralement robustes, mais les cellules de mammifères fragiles peuvent être facilement endommagées ou tuées par un cisaillement excessif. Par conséquent, le taux d'agitation doit être soigneusement optimisé pour assurer un mélange adéquat sans compromettre la viabilité cellulaire.
Le goulot d'étranglement du transfert d'oxygène
À mesure que la densité cellulaire augmente, la demande d'oxygène de la culture (le Taux d'Absorption d'Oxygène, ou TAO) peut dépasser la capacité du bioréacteur à le fournir (le Taux de Transfert d'Oxygène, ou TTO).
Ceci est un goulot d'étranglement courant dans les cultures à haute densité. Les ingénieurs doivent équilibrer les taux de spargage et l'agitation pour maximiser le transfert d'oxygène sans créer de mousse excessive ou de contraintes de cisaillement.
Formation de mousse
L'injection de gaz dans un milieu de culture riche en protéines est une recette parfaite pour la mousse.
L'excès de mousse peut bloquer les filtres d'échappement, entraînant une accumulation de pression et une contamination potentielle. Les bioréacteurs gèrent cela grâce à des brise-mousse mécaniques ou à l'ajout automatisé d'agents antimousse chimiques.
Faire le bon choix pour votre objectif
Les points de consigne spécifiques et les stratégies de contrôle d'un bioréacteur dépendent entièrement des cellules cultivées et du résultat souhaité.
- Si votre objectif principal est la fermentation microbienne à haute densité (par exemple, E. coli) : Votre priorité sera un apport d'oxygène agressif et un système de refroidissement efficace pour éliminer l'immense chaleur générée par un métabolisme rapide.
- Si votre objectif principal est la culture de cellules de mammifères sensibles (par exemple, pour la production d'anticorps) : Vous privilégiez un mélange doux pour minimiser les contraintes de cisaillement, un contrôle précis du pH à l'aide de CO₂, et potentiellement des stratégies d'alimentation en nutriments complexes.
- Si votre objectif principal est un processus anaérobie (par exemple, certaines productions de biocarburants) : La clé est l'exclusion stricte de l'oxygène par spargage avec un gaz inerte comme l'azote, ainsi qu'un contrôle précis de la température.
En fin de compte, maîtriser l'interaction de ces conditions est la compétence fondamentale pour traduire avec succès un processus biologique du laboratoire à la production à l'échelle industrielle.
Tableau récapitulatif :
| Condition | Objectif | Plage typique/Exemple |
|---|---|---|
| Température | Régit le taux métabolique | 30-37°C (E. coli), ~37°C (cellules de mammifères) |
| pH | Maintient la fonction protéique et la viabilité | 7,2-7,4 (cellules de mammifères) |
| Oxygène dissous (OD) | Soutient la respiration aérobie | Contrôlé via le spargage et l'agitation |
| Agitation/Mélange | Assure l'uniformité et le transfert d'oxygène | Optimisé pour équilibrer le mélange et les contraintes de cisaillement |
Prêt à optimiser votre bioprocédé grâce à des conditions de bioréacteur contrôlées avec précision ? KINTEK est spécialisée dans les équipements de laboratoire et les consommables de haute qualité adaptés à la gestion fiable de la température, du pH et de l'oxygène dissous — que vous mettiez à l'échelle une fermentation microbienne ou que vous cultiviez des cellules de mammifères sensibles. Contactez nos experts dès aujourd'hui pour discuter de la manière dont nos solutions peuvent améliorer la productivité et le rendement de votre laboratoire.
Guide Visuel
Produits associés
- Réacteurs de laboratoire personnalisables à haute température et haute pression pour diverses applications scientifiques
- Réacteur visuel à haute pression pour observation in-situ
- Réacteurs haute pression personnalisables pour des applications scientifiques et industrielles avancées
- Réacteur Autoclave Haute Pression en Acier Inoxydable pour Laboratoire
- Mini autoclave à réacteur haute pression en acier inoxydable pour laboratoire
Les gens demandent aussi
- Comment contrôler la haute pression dans un réacteur ? Un guide pour une opération sûre et stable
- Quel est le rôle principal d'un réacteur à haute température et haute pression dans le processus de glycérolyse ?
- Quelles conditions expérimentales sont fournies par un réacteur HTHP pour les tubes enroulés ? Optimiser la simulation de la corrosion de fond
- Pourquoi la désaération à l'azote doit-elle être effectuée dans un réacteur avant les tests de corrosion au CO2 ? Assurer des données de test valides
- Quel rôle joue une couverture de gaz argon de haute pureté dans les tests de corrosion à haute température ? Assurer une précision de données précise





