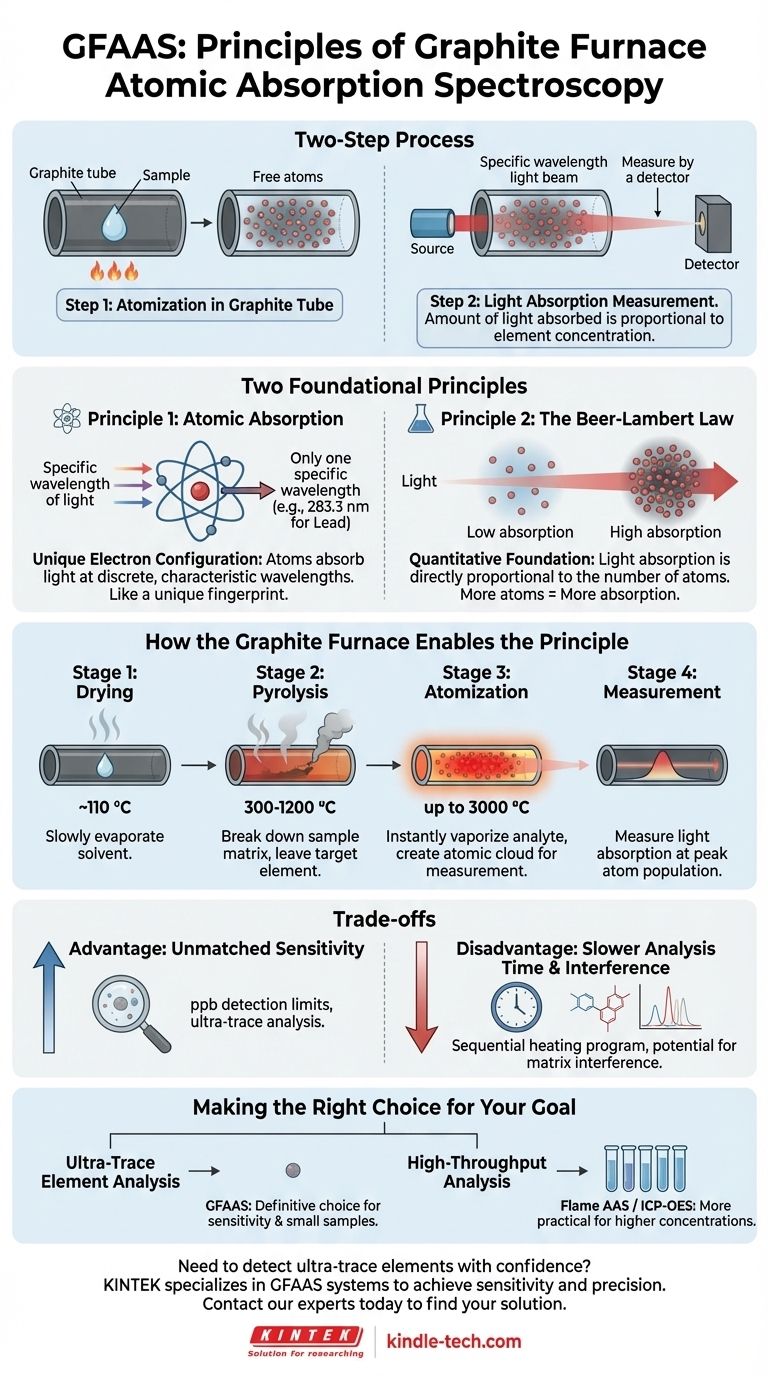
À la base, le principe de la spectroscopie d'absorption atomique à four en graphite (SAAG) est un processus en deux étapes. Premièrement, un échantillon est chauffé dans un tube en graphite pour créer un nuage confiné d'atomes libres et neutres. Deuxièmement, un faisceau lumineux spécifique à l'élément mesuré traverse ce nuage, et la quantité de lumière absorbée est directement proportionnelle à la concentration de l'élément dans l'échantillon.
Le principe clé n'est pas seulement que les atomes absorbent la lumière, mais que le four en graphite fournit un environnement hautement efficace et contrôlé pour convertir la totalité de l'échantillon en vapeur atomique, la piégeant brièvement dans le trajet optique pour une sensibilité maximale.

Les deux principes fondamentaux
La SAAG fonctionne sur la base de deux lois scientifiques bien établies qui agissent de concert. Comprendre ces deux lois est essentiel pour saisir comment la technique atteint sa précision remarquable.
Principe 1 : L'absorption atomique
Chaque élément possède une configuration électronique unique. Pour cette raison, les atomes d'un élément spécifique n'absorberont la lumière qu'à des longueurs d'onde très discrètes et caractéristiques.
Ce phénomène agit comme une empreinte digitale unique. Par exemple, les atomes de plomb n'absorberont la lumière qu'à 283,3 nm, tandis que les atomes de cuivre absorbent à 324,8 nm. La SAAG exploite ceci en utilisant une source lumineuse qui émet la longueur d'onde précise de l'élément d'intérêt.
Principe 2 : La loi de Beer-Lambert
Cette loi fournit la base quantitative de la mesure. Elle stipule que la quantité de lumière absorbée par le nuage atomique est directement proportionnelle au nombre d'atomes dans le trajet optique.
En termes simples : plus il y a d'atomes, plus l'absorption de lumière est importante. En mesurant la diminution de l'intensité lumineuse lorsqu'elle traverse l'échantillon, nous pouvons déterminer avec précision la concentration de l'élément cible.
Comment le four en graphite permet ce principe
Le « four en graphite » est l'atomiseur — le composant responsable de la création du nuage d'atomes libres à partir de l'échantillon liquide ou solide initial. Sa conception et son chauffage programmé sont ce qui rend cette technique si puissante.
Le tube en graphite comme micro-four
Le cœur de l'instrument est un petit tube creux en graphite. L'échantillon (typiquement quelques microlitres) est placé à l'intérieur de ce tube.
Le tube est positionné de manière à ce qu'un faisceau lumineux puisse passer directement par son centre. Il est également connecté à des électrodes capables de faire passer un courant élevé, le chauffant par effet Joule jusqu'à des températures allant jusqu'à 3000 °C en quelques secondes.
Le programme de chauffage contrôlé
Contrairement à une simple flamme, le four suit un programme de température précis et multi-étapes pour préparer l'échantillon à la mesure.
- Séchage : Le tube est d'abord chauffé doucement (par exemple, ~110 °C) pour évaporer lentement le solvant sans provoquer d'éclaboussures de l'échantillon.
- Pyrolyse (Calcination) : La température est augmentée significativement (par exemple, 300-1200 °C) pour décomposer et éliminer la matrice de l'échantillon (comme la matière organique ou les sels complexes) tout en laissant l'élément cible.
- Atomisation : Pendant quelques secondes, la température est rapidement portée à son maximum. Cette chaleur intense vaporise instantanément l'analyte, créant un nuage dense et localisé d'atomes libres à l'état fondamental directement dans le trajet optique.
- Mesure : L'instrument mesure l'absorption lumineuse uniquement pendant cette brève étape d'atomisation lorsque la population atomique est à son apogée.
Comprendre les compromis
La méthode du four en graphite offre des avantages incroyables, mais il est essentiel de comprendre son contexte opérationnel et ses limites.
Avantage : Sensibilité inégalée
L'avantage principal de la SAAG est sa sensibilité. En contenant la totalité de l'échantillon atomisé dans une petite zone pendant quelques secondes, elle atteint des limites de détection des milliers de fois inférieures à celles d'autres méthodes comme la SAAG à flamme, souvent dans la gamme des parties par milliard (ppb).
Inconvénient : Temps d'analyse plus lent
La nature séquentielle du programme de chauffage (séchage, pyrolyse, atomisation, refroidissement) signifie que chaque analyse d'échantillon prend plusieurs minutes. Cela rend la SAAG nettement plus lente que les techniques capables d'analyser les échantillons en continu.
Inconvénient : Potentiel d'interférence
L'environnement complexe à l'intérieur du four peut entraîner des interférences chimiques et spectrales dues à la matrice de l'échantillon. Celles-ci doivent être soigneusement gérées par le développement de méthodes et l'utilisation de technologies de correction de fond pour garantir des résultats précis.
Faire le bon choix pour votre objectif
Le choix de la technique analytique appropriée dépend entièrement de votre objectif.
- Si votre objectif principal est l'analyse d'éléments ultra-traces : La SAAG est le choix définitif en raison de sa sensibilité exceptionnelle et du très faible volume d'échantillon qu'elle nécessite.
- Si votre objectif principal est l'analyse à haut débit de nombreux échantillons : Une technique plus rapide comme la SAAG à flamme ou l'ICP-OES est plus pratique, à condition que vos concentrations d'éléments soient suffisamment élevées pour leurs limites de détection.
En comprenant le principe de l'atomisation totale contrôlée, vous pouvez tirer parti de la puissance de la SAAG lorsque la sensibilité analytique ultime est l'exigence critique.
Tableau récapitulatif :
| Aspect clé | Description |
|---|---|
| Principe de base | Processus en deux étapes : atomiser l'échantillon dans un four en graphite, puis mesurer l'absorption de lumière par les atomes libres. |
| Loi quantitative | Loi de Beer-Lambert : l'absorption lumineuse est proportionnelle à la concentration de l'élément. |
| Avantage principal | Sensibilité inégalée pour l'analyse d'ultra-traces (gamme des parties par milliard). |
| Considération clé | Temps d'analyse plus lent par échantillon par rapport à la SAAG à flamme ou à l'ICP-OES. |
Besoin de détecter des éléments ultra-traces avec confiance ? KINTEK est spécialisée dans les équipements de laboratoire, y compris les spectromètres d'absorption atomique. Nos experts peuvent vous aider à choisir le bon système SAAG pour atteindre la sensibilité et la précision que votre laboratoire exige. Contactez notre équipe dès aujourd'hui pour discuter de vos défis analytiques spécifiques et trouver la solution parfaite.
Guide Visuel
Produits associés
- Four de Graphitization Expérimental à Vide de Graphite IGBT
- Four à vide graphite pour la graphitisation de matériaux négatifs
- Four de graphitisation sous vide vertical à haute température
- Four de graphitisation de film de haute conductivité thermique sous vide de graphite
- Four de graphitisation sous vide horizontal à haute température de graphite
Les gens demandent aussi
- Quels sont les avantages et les inconvénients du four à graphite ? Libérez les performances de chaleur extrême
- Quelles sont les interférences du four à graphite ? Surmonter les problèmes de matrice et de spectre pour une GFAAS précise
- Quel gaz est utilisé dans le four à graphite ? Maximisez la précision avec le bon gaz inerte
- Quelle est la température d'un four à graphite ? Atteignez une chaleur extrême jusqu'à 3000°C
- Quelle est la température d'absorption atomique dans un four en graphite ? Maîtriser le programme de chauffage multi-étapes
















