Oui, le métal s'évapore absolument dans le vide. En fait, la création d'un vide est l'étape essentielle qui permet d'évaporer les métaux et autres matériaux de manière contrôlée et utile. Ce processus, connu sous le nom d'évaporation sous vide ou d'évaporation thermique, est une pierre angulaire de la fabrication moderne pour tout, des puces informatiques aux lentilles optiques.
L'idée essentielle est qu'un vide ne provoque pas l'évaporation, mais il abaisse considérablement la température et l'énergie nécessaires à sa survenue. Il dégage le chemin pour que les atomes évaporés voyagent, permettant la création de films ultra-minces et précis.

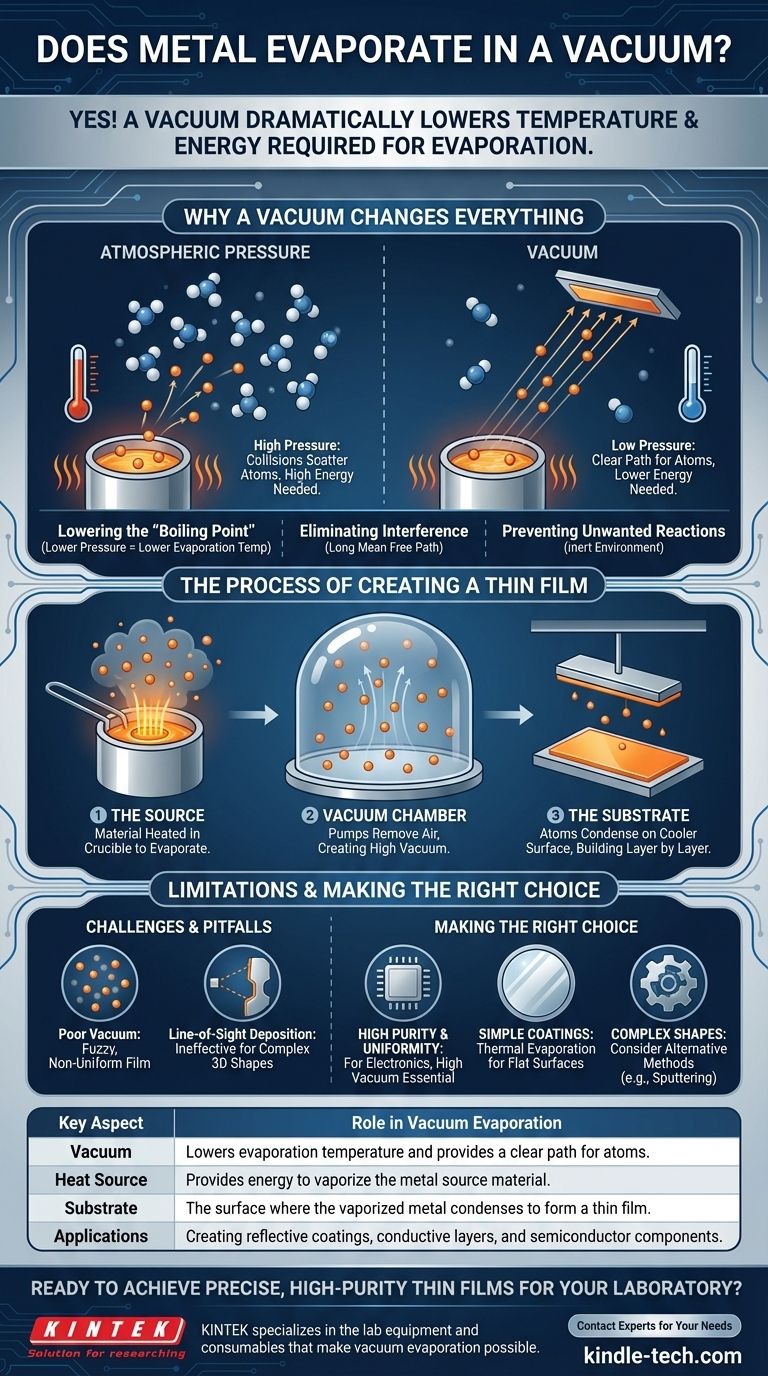
Pourquoi le vide change tout pour l'évaporation
Pour comprendre le processus, nous devons d'abord comprendre le rôle de la pression. L'évaporation est la transition d'une substance d'un état solide ou liquide à un état gazeux. Un vide est simplement un espace avec une pression extrêmement basse et très peu de particules d'air.
Abaissement du « Point d'ébullition »
Chaque matériau a une température à laquelle ses atomes ont suffisamment d'énergie pour s'échapper de sa surface. À pression atmosphérique normale, cette température est très élevée pour les métaux.
Un vide réduit considérablement la pression qui s'exerce sur la surface du matériau. Une fois cette force d'opposition supprimée, les atomes métalliques ont besoin de beaucoup moins d'énergie thermique pour se libérer et passer à l'état gazeux. Cela abaisse efficacement la température d'évaporation du matériau, de la même manière que l'eau bout à une température plus basse en haute altitude.
Élimination des interférences
Dans des conditions atmosphériques normales, un atome de métal évaporé entrerait presque instantanément en collision avec des milliards de molécules d'air (comme l'oxygène et l'azote). Ces collisions disperseraient les atomes métalliques, les empêchant de voyager dans une direction prévisible.
Dans un vide poussé, le chemin est dégagé. Les atomes métalliques évaporés peuvent voyager en ligne droite de la source à leur cible sans interférence. C'est ce qu'on appelle un libre parcours moyen long.
Prévention des réactions indésirables
De nombreux métaux sont très réactifs à leurs températures d'évaporation. S'ils sont exposés à l'air, ils s'oxyderont immédiatement ou formeront d'autres composés, contaminant le produit final.
Un vide fournit un environnement inerte, garantissant que le matériau évaporé reste pur lorsqu'il voyage de la source à la surface cible.
Le processus de création d'un film mince
L'évaporation sous vide est une méthode de dépôt physique en phase vapeur (PVD) utilisée pour appliquer un film mince de matériau sur une surface, appelée substrat.
Les trois composants clés
- La Source : Le matériau à déposer (par exemple, aluminium, or, chrome) est placé dans un récipient appelé creuset. Il est ensuite chauffé, généralement en faisant passer un courant électrique important à travers un filament résistant, jusqu'à ce qu'il commence à s'évaporer.
- La Chambre à vide : L'ensemble de ce processus se déroule à l'intérieur d'une chambre scellée où des pompes ont retiré presque tout l'air, créant un environnement de vide poussé.
- Le Substrat : C'est l'objet à revêtir (par exemple, une tranche de silicium, un morceau de verre, une pièce en plastique). Il est positionné au-dessus de la source de manière à être dans la trajectoire directe des atomes évaporants.
Lorsque les atomes métalliques traversent le vide, ils finissent par frapper la surface plus froide du substrat. Lors de l'impact, ils perdent leur énergie, se recondensent à l'état solide et s'accumulent couche par couche pour former un film lisse, uniforme et extrêmement mince.
Comprendre les limites et les pièges
Bien que puissante, l'évaporation sous vide n'est pas sans défis. La qualité du résultat dépend entièrement du contrôle des variables.
L'importance du vide poussé
Le niveau du vide est primordial. Un vide médiocre signifie qu'il reste trop de molécules de gaz résiduelles dans la chambre. Cela entraîne des collisions qui dispersent les atomes métalliques, ce qui donne un film non uniforme ou « flou » qui manque des propriétés souhaitées.
Dépôt en ligne de visée
Étant donné que les atomes évaporés voyagent en ligne droite, cette méthode ne peut revêtir que les surfaces qui se trouvent dans sa ligne de visée directe. Elle n'est pas efficace pour revêtir des formes 3D complexes avec des contre-dépouilles ou des surfaces cachées.
Compatibilité des matériaux
Tous les matériaux ne conviennent pas à l'évaporation thermique. Certains composés peuvent se décomposer lorsqu'ils sont chauffés au lieu de s'évaporer proprement, tandis que les matériaux avec des points d'ébullition extrêmement élevés peuvent être difficiles et énergivores à traiter.
Faire le bon choix pour votre objectif
Comprendre les principes de l'évaporation sous vide vous permet de l'appliquer correctement pour des objectifs techniques spécifiques.
- Si votre objectif principal est de créer des films de haute pureté et uniformes pour l'électronique : Un vide de haute qualité est non négociable pour garantir un processus propre et une excellente adhérence du film.
- Si votre objectif principal est d'appliquer un revêtement réfléchissant ou conducteur simple : L'évaporation thermique est une méthode efficace et rentable pour revêtir des surfaces planes ou légèrement courbées.
- Si votre objectif principal est de revêtir un objet complexe en trois dimensions : Vous devriez envisager des méthodes de dépôt alternatives, telles que la pulvérisation cathodique (sputtering), qui n'ont pas les mêmes limitations de ligne de visée.
En contrôlant la pression, vous obtenez un contrôle précis sur l'état fondamental de la matière, transformant un matériau brut en une surface conçue.
Tableau récapitulatif :
| Aspect clé | Rôle dans l'évaporation sous vide |
|---|---|
| Vide | Abaisse la température d'évaporation et fournit un chemin clair pour les atomes. |
| Source de chaleur | Fournit l'énergie nécessaire pour vaporiser le matériau source métallique. |
| Substrat | La surface où le métal vaporisé se condense pour former un film mince. |
| Applications | Création de revêtements réfléchissants, de couches conductrices et de composants semi-conducteurs. |
Prêt à obtenir des films minces précis et de haute pureté pour votre laboratoire ?
KINTEK est spécialisé dans l'équipement de laboratoire et les consommables qui rendent possible l'évaporation sous vide. Que vous développiez des composants électroniques avancés, des revêtements optiques ou des matériaux spécialisés, notre expertise garantit que votre processus est efficace et fiable.
Contactez nos experts dès aujourd'hui pour discuter de la manière dont nos solutions peuvent répondre à vos besoins spécifiques en laboratoire et améliorer vos capacités de recherche et de production.
Guide Visuel
Produits associés
- Bateau d'évaporation de molybdène, tungstène et tantale pour applications à haute température
- Bateau d'évaporation spécial en molybdène, tungstène et tantale
- Système de fusion par induction sous vide pour la fabrication de bandes et de fils
- Machine de Moulage à Froid sous Vide pour la Préparation d'Échantillons
- Pompe à vide à eau en circulation pour usage en laboratoire et industriel
Les gens demandent aussi
- Quelle est la différence entre l'évaporation thermique et l'évaporation par faisceau d'électrons ? Choisissez la bonne méthode pour votre couche mince
- De quel matériau est fabriqué le creuset le plus couramment utilisé dans l'évaporation thermique ? Choisir le bon matériau pour un dépôt de haute pureté
- Comment fonctionne une source d'évaporation de molybdène dans une atmosphère de sulfure d'hydrogène lors de la synthèse de films minces de disulfure de molybdène ?
- Que sont les sources d'évaporation thermique ? Types clés et comment choisir la bonne
- Quelles sont les sources d'évaporation thermique ? Un guide sur le chauffage résistif vs. le chauffage par faisceau d'électrons



















