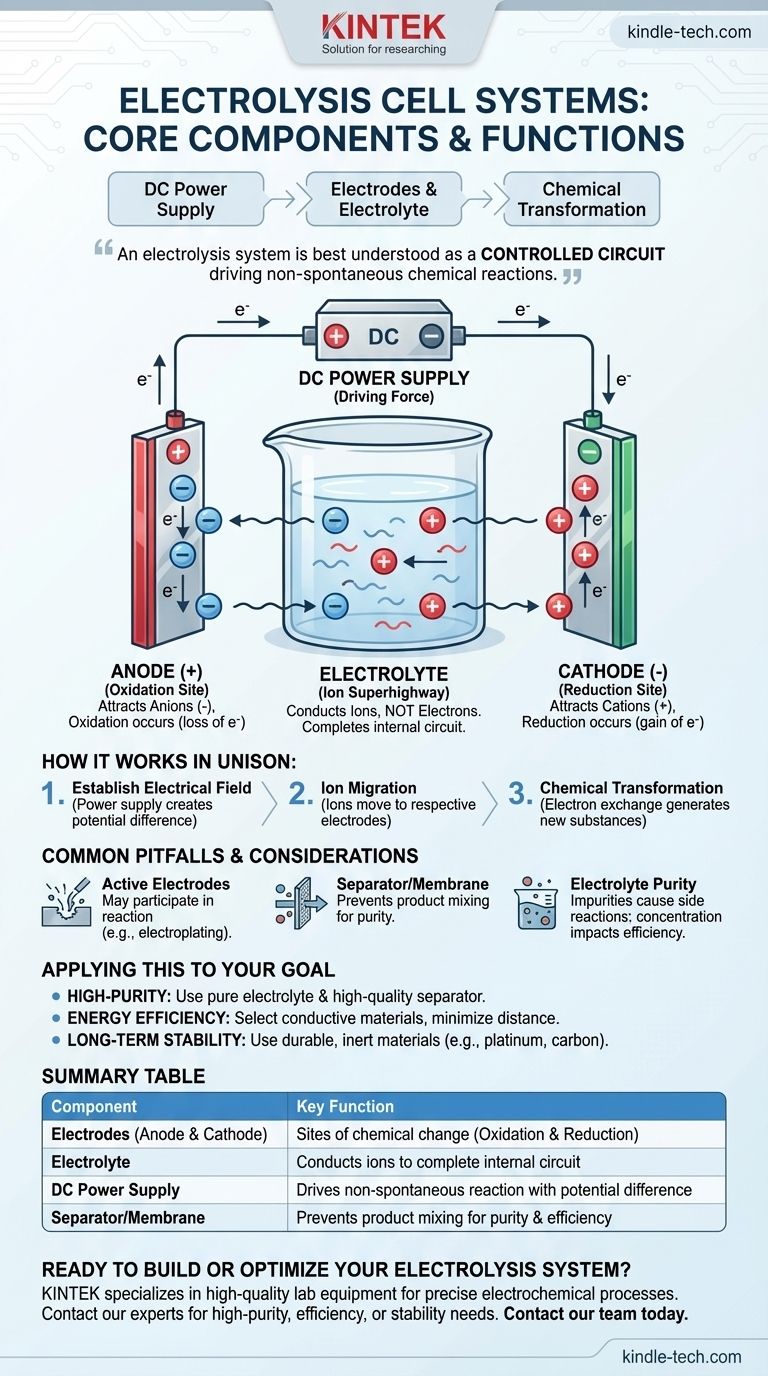
Au cœur, un système de cellule d'électrolyse est composé de trois éléments essentiels : deux électrodes (une anode et une cathode), un électrolyte contenant des ions, et une alimentation externe en courant continu (CC). Ces éléments fonctionnent à l'unisson pour utiliser l'énergie électrique afin de forcer une réaction chimique qui ne se produirait pas spontanément.
Un système d'électrolyse est mieux compris non pas comme une collection de pièces, mais comme un circuit contrôlé. L'alimentation électrique crée un potentiel électrique, entraînant les ions à travers l'électrolyte jusqu'aux électrodes, où ils subissent des transformations chimiques.

Les composants essentiels et leurs rôles
Pour saisir le fonctionnement de l'électrolyse, vous devez d'abord comprendre la fonction spécifique de chaque composant principal. Chacun joue un rôle indispensable et distinct dans le processus.
Les électrodes : sites du changement chimique
L'anode et la cathode sont des matériaux conducteurs, généralement des métaux ou du graphite, qui servent d'interface physique entre le circuit externe et l'électrolyte.
L'anode est l'électrode positive. Elle attire les ions chargés négativement (anions) de l'électrolyte. À la surface de l'anode, ces ions perdent des électrons dans un processus appelé oxydation.
La cathode est l'électrode négative. Elle attire les ions chargés positivement (cations). Ici, les ions gagnent des électrons dans un processus appelé réduction.
L'électrolyte : l'autoroute des ions
L'électrolyte est une substance contenant des ions libres, ce qui la rend électriquement conductrice. Il s'agit souvent d'une solution d'un acide, d'une base ou d'un sel dissous dans l'eau.
Son seul but est de conduire les ions, et non les électrons. Le mouvement de ces ions entre les électrodes complète le circuit électrique à l'intérieur de la cellule, permettant à la réaction de se maintenir.
L'alimentation CC : la force motrice
C'est le moteur externe du système, souvent une batterie ou un redresseur. Il entraîne la réaction non spontanée en créant une différence de potentiel électrique aux bornes des électrodes.
L'alimentation injecte des électrons dans la cathode, la rendant négative, et les retire de l'anode, la rendant positive. Il est crucial qu'il s'agisse d'une source à courant continu (CC) pour maintenir cette polarité fixe.
Comment le système fonctionne à l'unisson
Les composants ne sont pas indépendants ; ils forment un système intégré où la fonction de chaque partie permet la suivante.
1. Établissement du champ électrique
Le processus commence lorsque l'alimentation est mise sous tension. Elle établit immédiatement une charge positive sur l'anode et une charge négative sur la cathode.
2. Migration des ions
Ce potentiel électrique exerce une force sur les ions présents dans l'électrolyte. Les cations chargés positivement sont attirés vers la cathode négative, tandis que les anions chargés négativement sont attirés vers l'anode positive.
3. La transformation chimique
Lorsque les ions atteignent leurs électrodes respectives, l'échange d'électrons se produit. La substance est décomposée à mesure que de nouveaux composés ou éléments se forment aux surfaces des électrodes, comme la production de gaz hydrogène à la cathode et de gaz oxygène à l'anode lors de l'électrolyse de l'eau.
Pièges courants et considérations
Une compréhension fonctionnelle nécessite de reconnaître les facteurs pratiques qui influencent le résultat et l'efficacité du processus.
Le matériau de l'électrode n'est pas toujours inerte
Bien que de nombreux systèmes utilisent des électrodes inertes (comme le platine ou le carbone) qui ne font que faciliter la réaction, certaines applications utilisent des électrodes actives. Ces électrodes participent à la réaction, se dissolvant ou étant recouvertes de métal, comme on le voit dans la galvanoplastie ou l'affinage.
Le séparateur est souvent nécessaire
Dans de nombreuses applications industrielles, un séparateur ou une membrane est placé entre l'anode et la cathode. Cette barrière physique permet aux ions de passer mais empêche les produits nouvellement formés de se mélanger et de réagir entre eux, ce qui diminuerait la pureté et l'efficacité.
La pureté et la concentration de l'électrolyte sont importantes
L'efficacité de la cellule est directement liée à la capacité de l'électrolyte à conduire les ions. Les impuretés peuvent provoquer des réactions secondaires indésirables, tandis qu'une concentration incorrecte peut entraver le flux d'ions et ralentir l'ensemble du processus.
Application à votre objectif
Votre conception et votre orientation opérationnelle dépendront entièrement du résultat souhaité de l'électrolyse.
- Si votre objectif principal est des produits de haute pureté : Privilégiez une membrane séparatrice de haute qualité et un électrolyte pur pour éviter la contamination croisée et les réactions secondaires.
- Si votre objectif principal est l'efficacité énergétique : Sélectionnez des matériaux d'électrode hautement conducteurs et minimisez la distance physique entre eux pour réduire la résistance électrique.
- Si votre objectif principal est la stabilité à long terme : Utilisez des matériaux d'électrode durables et inertes qui résistent à la corrosion due à l'électrolyte et aux produits de la réaction.
En comprenant comment ces composants essentiels interagissent, vous pouvez manipuler les réactions chimiques avec précision et contrôle.
Tableau récapitulatif :
| Composant | Fonction clé |
|---|---|
| Électrodes (Anode & Cathode) | Sites de changement chimique (Oxydation & Réduction) |
| Électrolyte | Conduit les ions pour compléter le circuit électrique interne |
| Alimentation CC | Entraîne la réaction non spontanée en créant une différence de potentiel |
| Séparateur/Membrane (Courant) | Prévient le mélange des produits, augmentant la pureté et l'efficacité |
Prêt à construire ou à optimiser votre système d'électrolyse ? KINTEK est spécialisé dans la fourniture d'équipements de laboratoire et de consommables de haute qualité pour des processus électrochimiques précis. Que votre objectif soit la production de produits de haute pureté, l'efficacité énergétique ou la stabilité à long terme, nos experts peuvent vous aider à choisir les bons composants. Contactez notre équipe dès aujourd'hui pour discuter des besoins spécifiques de votre laboratoire !
Guide Visuel
Produits associés
- Cellules d'électrolyse PEM personnalisables pour diverses applications de recherche
- Cellule électrochimique à électrolyse spectrale en couche mince
- Cellule de diffusion de gaz électrolytique électrochimique à flux liquide
- Cellule électrochimique électrolytique à cinq ports
- Cellule électrochimique électrolytique en quartz pour expériences électrochimiques
Les gens demandent aussi
- Quelles sont les précautions à prendre lors du chauffage ou de la stérilisation d'une cellule d'électrolyse ? Éviter d'endommager les composants sensibles
- Quelle est la procédure de stockage appropriée pour une cellule d'électrolyse et ses composants ? Un guide étape par étape pour préserver la précision
- Quelle est la procédure appropriée pour arrêter l'expérience après électrolyse ? Un guide de sécurité étape par étape
- Quels paramètres doivent être strictement contrôlés pendant le processus d'électrolyse ? Assurer la précision et l'efficacité
- Quelle est la procédure de nettoyage immédiat après utilisation d'une cellule d'électrolyse ? Prévenir l'accumulation de résidus pour des résultats précis



















