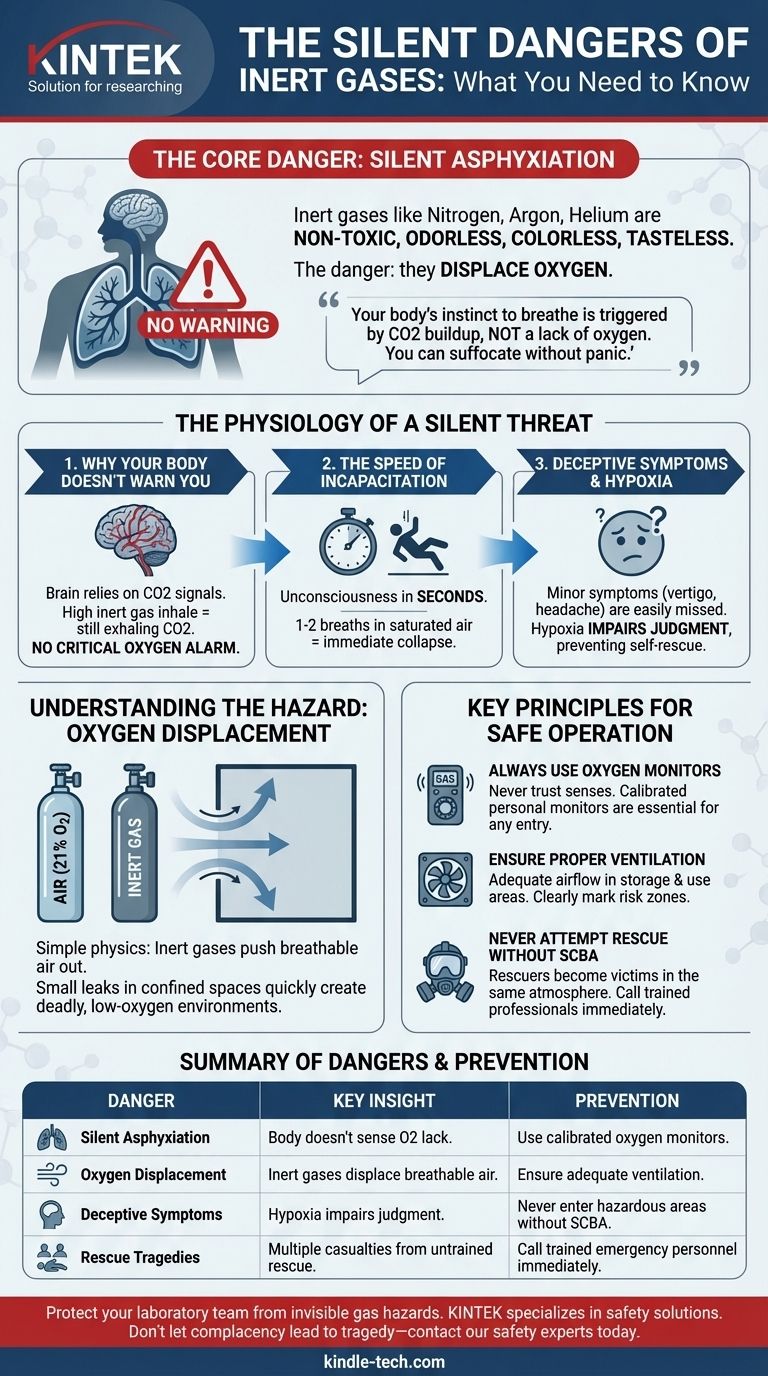
Le danger principal des gaz inertes est l'asphyxie silencieuse. Contrairement à d'autres matières dangereuses, les gaz comme l'azote ou l'argon ne sont pas toxiques et n'ont ni odeur, ni couleur, ni goût. Leur danger réside dans leur capacité à déplacer l'oxygène de l'air à un niveau tel qu'une ou deux respirations peuvent provoquer une perte de connaissance immédiate et une mort rapide, le tout sans que la victime ne ressente la sensation d'étouffement.
Le danger fondamental des gaz inertes n'est pas ce qu'ils sont, mais ce qu'ils ne sont pas : ils ne sont pas de l'oxygène. L'instinct de respirer de votre corps est déclenché par une accumulation de dioxyde de carbone, et non par un manque d'oxygène, ce qui signifie que vous pouvez vous asphyxier avec un gaz inerte sans aucun avertissement physique ni panique.

La physiologie d'une menace silencieuse
La raison pour laquelle l'exposition aux gaz inertes est si dangereuse est qu'elle contourne les mécanismes de défense naturels du corps. C'est un angle mort biologique qui peut avoir des conséquences fatales.
Pourquoi votre corps ne vous avertit pas
Votre envie impérieuse de prendre une bouffée d'air n'est pas motivée par un manque d'oxygène. C'est une réponse à l'augmentation des niveaux de dioxyde de carbone (CO2) dans votre sang.
Lorsque vous respirez une forte concentration de gaz inerte, vous continuez d'expirer du CO2. Votre cerveau, par conséquent, ne reçoit jamais le signal d'alarme indiquant qu'il est dangereusement faible en oxygène.
La rapidité de l'incapacité
En l'absence d'oxygène, la perte de connaissance survient en quelques secondes. Le cerveau est privé de carburant et s'éteint simplement.
La référence à « 1 à 2 respirations » n'est pas une exagération. Une personne entrant dans un environnement saturé d'azote peut perdre connaissance avant même d'avoir eu la chance de faire demi-tour et de sortir.
Symptômes trompeurs et peu fiables
Dans une atmosphère où l'oxygène est faible mais pas totalement absent, quelques symptômes mineurs peuvent apparaître. Ceux-ci peuvent inclure des vertiges, des maux de tête ou des difficultés à parler.
Cependant, un effet critique du manque d'oxygène (hypoxie) est l'altération du jugement. La victime est incapable de reconnaître ces symptômes comme un signe d'asphyxie imminente et ne pourra prendre aucune mesure corrective ni appeler à l'aide.
Comprendre le danger : le déplacement de l'oxygène
Le danger n'est pas une réaction chimique ; c'est une question de physique simple. Les gaz inertes sont plus lourds ou plus légers que l'air et repoussent physiquement l'atmosphère respirable d'un espace.
La nature du gaz inerte
Les gaz inertes sont des éléments qui ne réagissent pas facilement avec d'autres substances. Les exemples courants dans les milieux industriels et de laboratoire comprennent l'azote (N₂), l'argon (Ar) et l'hélium (He).
Parce qu'ils ne sont ni toxiques ni inflammables, ils sont souvent perçus comme « sûrs », ce qui conduit à la complaisance.
Comment un environnement devient mortel
L'air normal contient environ 21 % d'oxygène. Lorsqu'un gaz inerte est libéré dans un espace mal ventilé ou confiné, il dilue le pourcentage d'oxygène disponible.
Si une bouteille d'azote comprimé fuyait dans une petite pièce, elle abaisserait rapidement le niveau d'oxygène à un point qui ne peut soutenir la conscience ou la vie.
Pièges courants et scénarios à haut risque
La conscience du danger est la plus élevée dans les espaces confinés évidents, mais les incidents mortels se produisent souvent dans des situations apparemment anodines.
Espaces confinés ou clos
C'est le scénario classique et le plus létal. Tout travail dans des réservoirs, des cuves, des fosses ou même de petites pièces non ventilées où des gaz inertes sont utilisés présente un risque extrême.
Fuites « mineures »
Une fuite lente et silencieuse d'un raccord de conduite de gaz ou d'une vanne dans un placard de rangement peut suffire à créer une atmosphère mortelle sur plusieurs heures. L'absence d'odeur ou de couleur rend la détection impossible sans équipement approprié.
La tragédie de la tentative de sauvetage
Un scénario courant et tragique implique un sauveteur potentiel. Voyant un collègue s'effondrer, son premier réflexe est de se précipiter pour aider. Ce faisant, il pénètre dans la même atmosphère déficiente en oxygène et devient rapidement une deuxième victime.
Principes clés pour un fonctionnement sûr
Puisque vous ne pouvez pas vous fier à vos sens pour détecter la présence d'un danger lié aux gaz inertes, vous devez vous fier à des procédures et des technologies établies.
- Si votre objectif principal est d'entrer dans tout espace de travail contenant des gaz inertes : Utilisez toujours un moniteur d'oxygène personnel calibré. Ne vous fiez jamais à vos sens et considérez chaque zone close comme potentiellement dangereuse jusqu'à preuve du contraire.
- Si votre objectif principal est la conception et le stockage des systèmes : Assurez-vous que toutes les zones où des gaz inertes sont utilisés ou stockés disposent d'une ventilation adéquate et marquez clairement toutes les zones à risque potentiel avec des panneaux d'avertissement.
- Si votre objectif principal est l'intervention d'urgence : N'entrez jamais dans une zone pour secourir une personne effondrée sans appareil respiratoire autonome (ARA) approprié. Appelez immédiatement des intervenants d'urgence formés.
En fin de compte, la sécurité avec les gaz inertes dépend de la reconnaissance que le danger est à la fois invisible et neurologiquement trompeur.
Tableau récapitulatif :
| Danger | Idée clé | Prévention |
|---|---|---|
| Asphyxie silencieuse | Le corps ne détecte pas le manque d'oxygène ; perte de connaissance en quelques secondes | Utiliser des moniteurs d'oxygène calibrés |
| Déplacement de l'oxygène | Les gaz inertes déplacent l'air respirable dans les espaces confinés | Assurer une ventilation adéquate |
| Symptômes trompeurs | L'hypoxie altère le jugement ; les victimes ne peuvent pas se sauver elles-mêmes | Ne jamais entrer dans des zones dangereuses sans ARA |
| Tragédies de sauvetage | Plusieurs victimes lorsque des intervenants non formés pénètrent dans la zone | Appeler immédiatement le personnel d'urgence formé |
Protégez votre équipe de laboratoire contre les dangers invisibles des gaz. KINTEK se spécialise dans l'équipement et les consommables de laboratoire, répondant aux besoins des laboratoires avec des solutions de sécurité fiables, y compris des systèmes de surveillance des gaz et des équipements de ventilation. Ne laissez pas la complaisance mener à la tragédie — contactez nos experts en sécurité dès aujourd'hui pour évaluer vos risques liés aux gaz inertes et mettre en œuvre des protocoles vitaux.
Guide Visuel