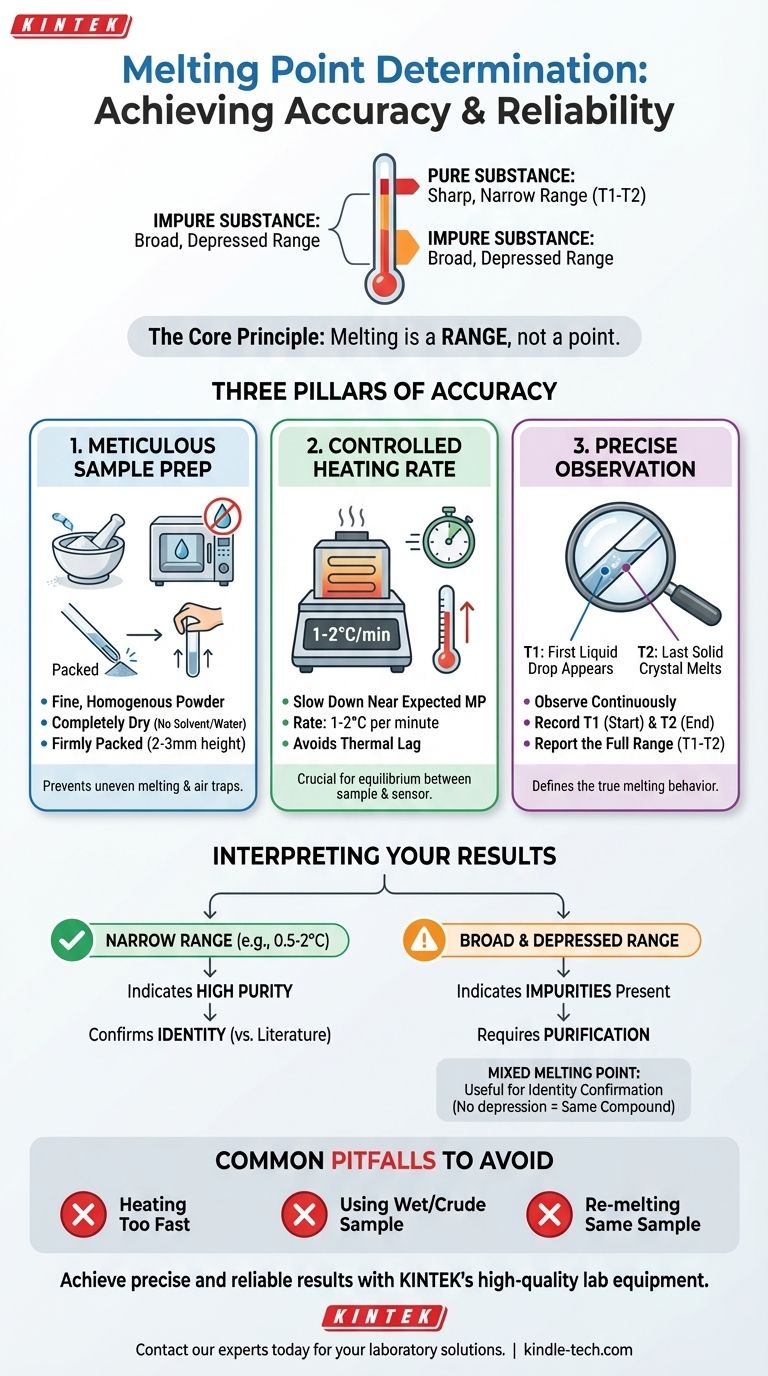
En pratique, une détermination précise du point de fusion repose sur trois facteurs : une préparation méticuleuse de l'échantillon, un taux de chauffage lent et contrôlé, et une observation précise de toute la plage de fusion. Cette technique est un outil fondamental en chimie, utilisé principalement pour confirmer l'identité d'un composé et pour évaluer sa pureté. Une mesure correctement exécutée fournit des données claires et reproductibles.
Le principe fondamental à comprendre est que le point de fusion n'est pas une température unique mais une plage. Pour une substance pure, cette plage est étroite et nette. Pour une substance impure, la plage devient large et abaissée, ce qui signifie qu'elle commence à fondre à une température plus basse et sur une étendue plus large.

Le principe : Que se passe-t-il pendant la fusion ?
Une transition d'états
La fusion est le processus physique par lequel une substance passe d'un réseau cristallin solide hautement ordonné à un état liquide désordonné. Cela nécessite de l'énergie, sous forme de chaleur, pour surmonter les forces intermoléculaires qui maintiennent les molécules dans leurs positions fixes.
La définition d'une plage de fusion
Le point de fusion est officiellement enregistré comme une plage de températures. La première température (T1) est le point où la première goutte de liquide apparaît parmi les cristaux solides. La deuxième température (T2) est le point où le dernier cristal solide fond en liquide.
Facteurs clés pour une mesure précise
Pour obtenir une plage de fusion fiable, vous devez contrôler plusieurs variables clés. Chaque étape est conçue pour garantir que la température que vous lisez sur le thermomètre est la vraie température de l'échantillon.
La préparation de l'échantillon est critique
L'échantillon doit être une poudre fine et homogène. Les gros cristaux fondent de manière inégale et emprisonnent l'air, ce qui entraîne un mauvais transfert de chaleur et une plage imprécise et large.
L'échantillon doit également être complètement sec. Tout solvant résiduel, y compris l'eau de l'air, agira comme une impureté et abaissera le point de fusion.
Enfin, l'échantillon doit être tassé fermement dans un tube capillaire jusqu'à une hauteur ne dépassant pas 2-3 mm. Trop d'échantillon entraînera une différence de température significative entre le haut et le bas, élargissant artificiellement la plage de fusion.
L'importance d'un taux de chauffage lent
C'est la source d'erreur la plus courante. Près du point de fusion attendu, le taux de chauffage doit être ralenti à 1-2 °C par minute.
Si vous chauffez l'échantillon trop rapidement, la température du bloc chauffant augmentera plus vite que la chaleur ne peut être transférée à l'échantillon et au thermomètre. Ce "décalage thermique" entraîne une plage de fusion observée significativement plus élevée que la valeur réelle.
Observation précise de la température
Vous devez observer l'échantillon continuellement à mesure qu'il approche du point de fusion. Enregistrez la température (T1) à l'instant où vous voyez la première petite goutte de liquide se former.
Continuez à observer à la fois l'échantillon et le thermomètre. Enregistrez la deuxième température (T2) au moment exact où la dernière particule solide disparaît. La valeur finale rapportée est toujours cette plage : T1 - T2.
Interprétation de vos résultats : Pureté et identité
La plage de fusion est un outil de diagnostic puissant. Sa largeur et sa position racontent une histoire sur votre composé.
La signature d'un composé pur
Un composé organique cristallin pur aura une plage de fusion nette et étroite, s'étendant généralement sur seulement 0,5 °C à 2 °C. Sa plage observée sera également en étroite concordance avec la valeur littéraire établie pour cette substance.
L'effet des impuretés (abaissement du point de fusion)
Les impuretés perturbent la structure uniforme du réseau cristallin. Cela rend le réseau moins stable et nécessite moins d'énergie (une température plus basse) pour le briser.
En conséquence, une substance impure présentera un abaissement du point de fusion. Sa plage de fusion sera à la fois plus basse et plus large que celle du composé pur. Plus il y a d'impuretés, plus l'abaissement est important et plus la plage est large.
Utilisation du point de fusion mixte pour l'identification
Cette technique est utilisée pour confirmer l'identité d'une substance inconnue (A) lorsque vous suspectez qu'il s'agit d'un composé connu (X).
Vous préparez un échantillon contenant un mélange intime de A et X, généralement dans un rapport 1:1. Si A et X sont le même composé, le point de fusion du mélange sera net et identique à celui du X pur. Si A et X sont différents, A agira comme une impureté pour X (et vice-versa), provoquant un abaissement significatif du point de fusion et une plage large.
Pièges courants et comment les éviter
Même les chimistes expérimentés peuvent faire des erreurs. Être conscient de ces erreurs courantes est la première étape pour les prévenir.
Chauffer trop rapidement
C'est le péché capital de la détermination du point de fusion. Cela conduit systématiquement à une plage de fusion à la fois artificiellement élevée et large. Effectuez toujours une mesure rapide "d'exploration" d'abord pour trouver la plage approximative, puis effectuez une deuxième mesure lente pour la précision.
Utiliser un échantillon "humide" ou non purifié
Ne prenez jamais le point de fusion d'un produit brut ou d'un échantillon qui n'est pas complètement sec. Les résultats seront trompeurs et ne refléteront pas les propriétés du composé pur.
Refondre le même échantillon
Ne réutilisez jamais un échantillon qui a déjà fondu. De nombreux composés organiques se décomposent légèrement à leur point de fusion. Une deuxième mesure sur le même échantillon montrera souvent une plage abaissée et large en raison de cette impureté auto-générée. Utilisez toujours un échantillon frais pour chaque essai.
Faire le bon choix pour votre objectif
Votre approche de la détermination du point de fusion dépend de votre objectif.
- Si votre objectif principal est de confirmer l'identité d'une substance : Comparez votre plage de fusion nette et étroite avec la valeur littéraire et, si possible, effectuez un point de fusion mixte avec un échantillon authentique.
- Si votre objectif principal est d'évaluer la pureté de votre produit : Une plage de fusion étroite (par exemple, < 2 °C) proche de la valeur littéraire est un indicateur fort de haute pureté. Une plage large et abaissée signale la nécessité d'une purification supplémentaire.
- Si votre objectif principal est de caractériser un nouveau composé inconnu : Effectuez plusieurs mesures minutieuses pour établir une plage de fusion hautement reproductible et étroite, qui servira de constante physique clé pour votre nouvelle substance.
Maîtriser cette technique apparemment simple est une pierre angulaire de l'analyse et de la caractérisation chimique rigoureuses.
Tableau récapitulatif :
| Facteur | Considération clé | Impact sur le résultat |
|---|---|---|
| Préparation de l'échantillon | Poudre fine et sèche, tassée fermement dans le capillaire | Assure une plage de fusion nette et étroite |
| Taux de chauffage | Taux lent (1-2°C/min) près du point de fusion | Prévient le décalage thermique et les lectures élevées inexactes |
| Observation | Enregistrer le premier liquide (T1) et le dernier solide (T2) | Définit la véritable plage de fusion (T1-T2) |
| Interprétation | Plage étroite = composé pur ; Plage large et abaissée = impur | Critique pour évaluer la pureté et confirmer l'identité |
Obtenez des résultats précis et fiables dans votre laboratoire.
La détermination précise du point de fusion est fondamentale pour confirmer l'identité des composés et évaluer la pureté. KINTEK est spécialisé dans la fourniture d'équipements de laboratoire et de consommables de haute qualité conçus pour soutenir ces analyses critiques. Des appareils de point de fusion fiables aux outils essentiels de préparation d'échantillons, nos produits sont conçus pour améliorer la précision et l'efficacité de votre travail.
Laissez-nous vous aider à maîtriser cette technique fondamentale. Contactez nos experts dès aujourd'hui pour trouver les solutions parfaites pour les besoins spécifiques de votre laboratoire et assurez-vous que votre analyse chimique repose sur une base de précision.
Guide Visuel
Produits associés
- Sonde de détermination de l'hydrogène pour mesurer rapidement la teneur en hydrogène avec un taux de réussite élevé
- Four de Fusion par Induction sous Vide à l'Échelle du Laboratoire
- Four de fusion par induction à arc sous vide
- Potentiostat de poste de travail électrochimique de laboratoire pour une utilisation en laboratoire
- Sonde à oxygène pour mesurer la température et la teneur en oxygène actif dans l'acier liquide
Les gens demandent aussi
- Quels sont les principaux avantages et inconvénients de l'utilisation d'une sonde à oxygène ? Optimisez votre stratégie de contrôle d'atmosphère
- Avec quels métaux peut-on forger ? Découvrez les métaux malléables pour chaque projet
- Quelle chose est déterminée dans la teneur en cendres ? Mesurer les matières inorganiques pour le contrôle qualité
- À quelle température l'acier se liquéfie-t-il ? Comprendre la plage de fusion pour vos applications
- Pourquoi déterminons-nous la teneur en cendres du charbon ? Découvrez sa véritable valeur énergétique et évitez des temps d'arrêt coûteux.






