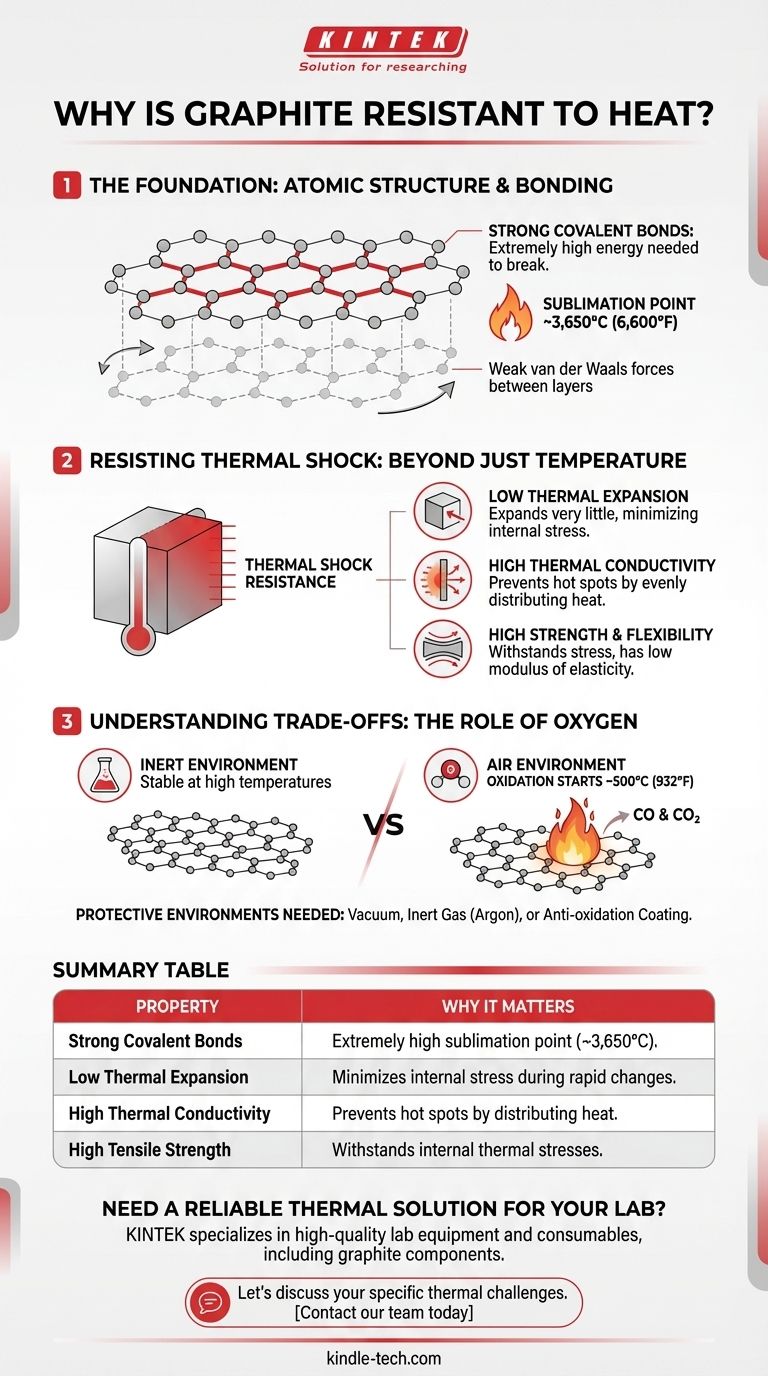
La raison fondamentale de la résistance à la chaleur du graphite réside dans sa structure atomique unique. Les atomes de carbone au sein de ses couches sont liés par des liaisons covalentes extrêmement solides, qui nécessitent une quantité énorme d'énergie thermique pour se rompre. Il en résulte un point de sublimation exceptionnellement élevé et une capacité à maintenir son intégrité structurelle à des températures où la plupart des métaux seraient liquides.
Le terme « résistance à la chaleur » englobe deux concepts distincts : la capacité à supporter une température élevée sans fondre et la capacité à survivre à des changements rapides de température sans se fissurer. Le graphite excelle dans les deux domaines grâce à ses liaisons atomiques puissantes et à une combinaison unique de propriétés thermiques qui préviennent les contraintes internes.

Le Fondement : Structure Atomique et Liaisons
Pour comprendre la performance thermique du graphite, nous devons d'abord examiner comment ses atomes de carbone sont agencés. Ses propriétés sont le résultat direct de sa structure interne.
Des Liaisons Covalentes Solides
Le graphite est constitué de couches d'atomes de carbone disposés en réseau hexagonal. À l'intérieur de chaque couche, chaque atome de carbone est lié à trois autres par des liaisons covalentes solides. Ce sont les mêmes types de liaisons que l'on trouve dans le diamant.
La rupture de ces liaisons nécessite une énergie immense, ce qui explique pourquoi le graphite ne fond pas à pression atmosphérique, mais se sublime (passe de l'état solide directement à l'état gazeux) à une température extrêmement élevée, environ 3 650 °C (6 600 °F).
Une Histoire de Deux Liaisons
Bien que les liaisons à l'intérieur de chaque couche soient incroyablement fortes, les forces qui maintiennent les couches ensemble (forces de van der Waals) sont très faibles. C'est pourquoi les couches peuvent glisser les unes sur les autres, faisant du graphite un excellent lubrifiant, mais c'est la force interne aux couches qui lui confère sa stabilité thermique.
Résister au Choc Thermique : Au-delà de la Simple Température
De nombreux matériaux peuvent supporter une chaleur élevée mais se fracturer lorsque la température change trop rapidement. Cette défaillance est appelée choc thermique. Le graphite y est exceptionnellement résistant.
Le choc thermique se produit lorsque différentes parties d'un matériau se dilatent ou se contractent à des vitesses différentes, créant une contrainte interne qui dépasse la résistance du matériau.
Faible Coefficient de Dilatation Thermique
L'une des propriétés les plus importantes du graphite est son très faible coefficient de dilatation thermique. Cela signifie que lorsqu'il chauffe, il se dilate très peu.
Comme il n'essaie pas de changer drastiquement de taille, il génère beaucoup moins de contraintes internes par rapport à des matériaux comme les céramiques ou les métaux lors d'un chauffage ou d'un refroidissement rapide.
Haute Conductivité Thermique
Le graphite est un excellent conducteur thermique. Il propage efficacement la chaleur à travers sa structure, empêchant la formation de « points chauds ».
Cette capacité à uniformiser rapidement la température à travers le matériau signifie qu'il n'y a pas de gradients de température sévères pour provoquer une dilatation différentielle et des contraintes en premier lieu.
Haute Résistance et Flexibilité
Bien qu'il soit connu comme un matériau tendre, le graphite possède une résistance à la traction élevée, surtout lorsque les températures augmentent. Il peut supporter les contraintes internes qui parviennent à s'accumuler.
De plus, il présente un faible module d'élasticité, ce qui signifie qu'il n'est ni parfaitement rigide ni cassant. Il possède une légère capacité de « jeu », lui permettant de fléchir sous la contrainte thermique plutôt que de se briser.
Comprendre les Compromis : Le Rôle de l'Oxygène
Aucun matériau n'est parfait, et la principale faiblesse du graphite à haute température réside dans son interaction avec l'environnement.
Oxydation dans l'Air
Bien que le graphite soit exceptionnellement stable sous vide ou dans une atmosphère inerte, ses performances changent radicalement en présence d'oxygène.
Le graphite commencera à s'oxyder, ou à brûler, dans l'air à des températures commençant autour de 500 °C (932 °F). Cette réaction chimique consomme le graphite, le transformant en monoxyde de carbone et en dioxyde de carbone gazeux.
Le Besoin d'Environnements Protecteurs
Cette limite signifie que pour les applications à très haute température comme les composants de fours ou les tuyères de fusée, le graphite doit être utilisé sous vide, dans une atmosphère de gaz inerte (comme l'argon), ou être protégé par un revêtement anti-oxydation spécial.
Faire le Bon Choix pour Votre Objectif
Lors de l'évaluation du graphite, votre environnement d'exploitation est aussi important que la température elle-même.
- Si votre objectif principal est la stabilité dans un environnement inerte : Le graphite est l'un des meilleurs matériaux disponibles en raison de son point de sublimation extrêmement élevé, résultat direct de ses liaisons covalentes solides.
- Si votre objectif principal est de survivre à des cycles rapides de chauffage et de refroidissement : La combinaison du faible coefficient de dilatation thermique, de la haute conductivité thermique et de la bonne résistance du graphite le rend exceptionnellement résistant aux chocs thermiques.
- Si vous opérez dans un environnement riche en oxygène au-dessus de 500 °C : Vous devez tenir compte de la sensibilité du graphite à l'oxydation et soit fournir une atmosphère protectrice, soit choisir un autre matériau.
En comprenant ces propriétés distinctes, vous pouvez tirer efficacement parti des forces thermiques incroyables du graphite tout en respectant ses limites environnementales.
Tableau Récapitulatif :
| Propriété | Pourquoi c'est important pour la résistance à la chaleur |
|---|---|
| Liaisons Covalentes Solides | Confère un point de sublimation extrêmement élevé (~3 650 °C). |
| Faible Dilatation Thermique | Minimise les contraintes internes lors de changements rapides de température. |
| Haute Conductivité Thermique | Prévient les points chauds en répartissant uniformément la chaleur. |
| Haute Résistance à la Traction | Résiste aux contraintes thermiques internes, surtout à haute température. |
Besoin d'une solution thermique fiable pour votre laboratoire ?
Les propriétés uniques du graphite le rendent idéal pour les processus à haute température, mais ses performances dépendent de la bonne application et du bon environnement. Chez KINTEK, nous sommes spécialisés dans la fourniture d'équipements et de consommables de laboratoire de haute qualité, y compris des composants en graphite conçus pour les fours et autres systèmes thermiques. Nos experts peuvent vous aider à choisir les bons matériaux pour améliorer l'efficacité et la sécurité de votre laboratoire.
Discutons de vos défis thermiques spécifiques. Contactez notre équipe dès aujourd'hui pour trouver la solution parfaite pour les besoins de votre laboratoire.
Guide Visuel