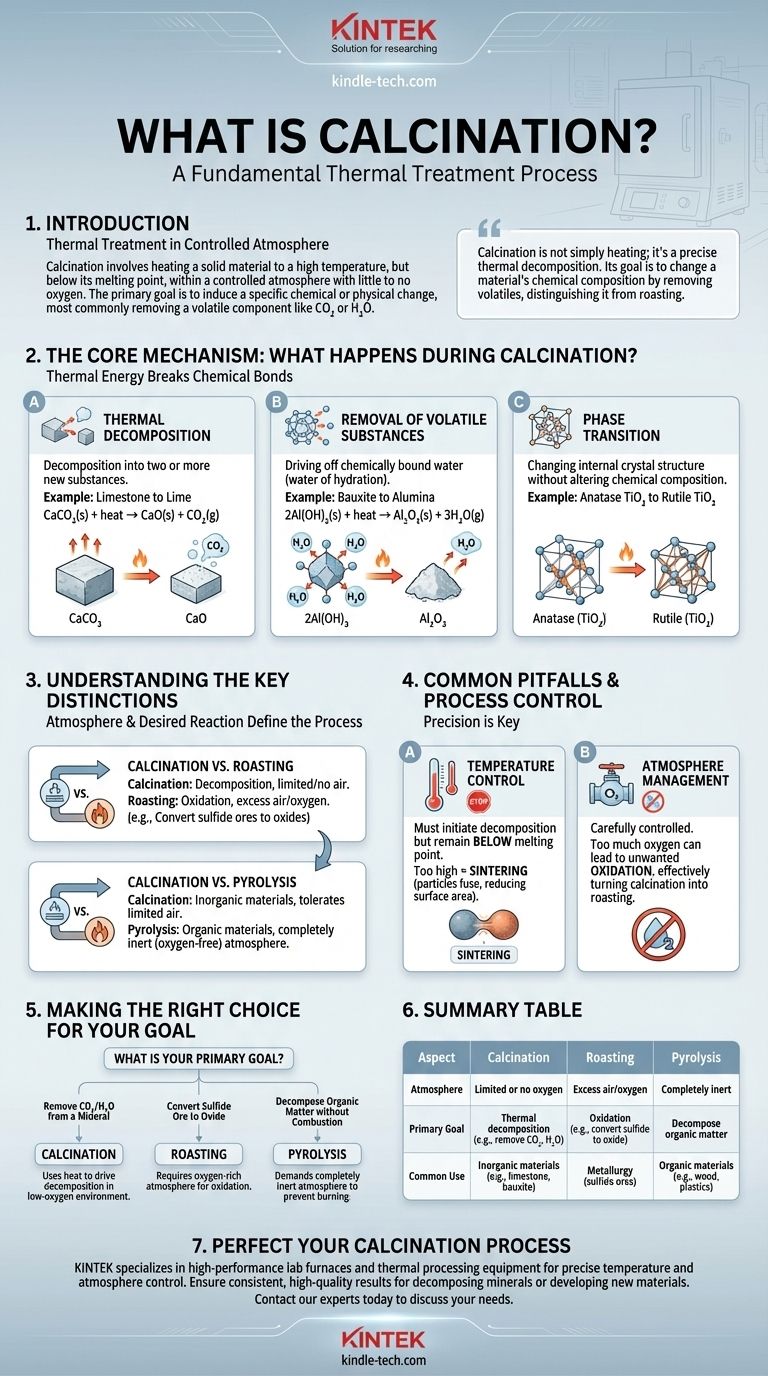
En science des matériaux et en métallurgie, la calcination est un traitement thermique fondamental. Elle implique le chauffage d'un matériau solide à une température élevée, mais inférieure à son point de fusion, dans une atmosphère contrôlée contenant peu ou pas d'oxygène. Ce processus n'est pas conçu pour faire fondre le matériau, mais pour induire un changement chimique ou physique spécifique, le plus souvent pour éliminer un composant volatil comme le dioxyde de carbone ou l'eau.
La calcination n'est pas simplement un chauffage ; c'est une décomposition thermique précise. Son objectif principal est de modifier la composition chimique d'un matériau en éliminant les composants volatils, ce qui la distingue d'autres traitements thermiques comme la torréfaction, qui implique une réaction chimique avec l'atmosphère du four.

Le mécanisme central : que se passe-t-il pendant la calcination ?
La calcination fonctionne en fournissant suffisamment d'énergie thermique pour rompre les liaisons chimiques, conduisant à une transformation prévisible du matériau solide. Ce changement se classe généralement dans l'une des trois catégories suivantes.
Décomposition thermique
C'est l'objectif le plus courant de la calcination. La chaleur provoque la décomposition du matériau en deux substances nouvelles ou plus.
L'exemple par excellence est la production de chaux (oxyde de calcium) à partir de calcaire (carbonate de calcium). Lorsqu'il est chauffé, le carbonate de calcium se décompose, libérant du gaz carbonique et laissant derrière lui de l'oxyde de calcium solide.
CaCO₃(s) + chaleur → CaO(s) + CO₂(g)
Élimination des substances volatiles
La calcination est très efficace pour éliminer l'eau chimiquement liée (eau d'hydratation) des minéraux.
Par exemple, dans la production d'alumine à partir de bauxite, la calcination est utilisée pour convertir les hydroxydes d'aluminium en oxyde d'aluminium (alumine) en éliminant les molécules d'eau.
2Al(OH)₃(s) + chaleur → Al₂O₃(s) + 3H₂O(g)
Transition de phase
Moins fréquemment, la calcination est utilisée pour modifier la structure cristalline interne d'un matériau (sa phase) sans en altérer la composition chimique.
Ce processus augmente la stabilité du matériau ou modifie ses propriétés. Par exemple, le chauffage de l'anatase, une forme de dioxyde de titane (TiO₂), la convertit en la phase rutile, plus stable et industriellement précieuse.
Comprendre les distinctions clés
Le terme « calcination » est souvent confondu avec d'autres traitements thermiques. La différence essentielle réside dans l'atmosphère utilisée et la réaction chimique souhaitée.
Calcination par rapport à la torréfaction
Le point de confusion le plus courant concerne la calcination et la torréfaction. Bien que les deux utilisent la chaleur, leurs objectifs et leurs atmosphères sont opposés.
La torréfaction est effectuée en présence d'un excès d'air ou d'oxygène. Son objectif est de faire réagir le solide avec l'oxygène, généralement pour convertir les minerais sulfurés en oxydes.
La calcination, en revanche, est effectuée en l'absence ou avec un apport très limité d'air. Son objectif est la décomposition, et non l'oxydation.
Calcination par rapport à la pyrolyse
La pyrolyse est un autre processus de décomposition thermique, mais elle se définit par son utilisation d'une atmosphère complètement inerte (sans oxygène).
Elle est le plus souvent associée à la décomposition de matériaux organiques, comme la production de charbon de bois à partir de bois. La calcination est généralement utilisée pour les matériaux inorganiques comme les minéraux et peut tolérer une quantité limitée d'air, tandis que la pyrolyse ne le peut pas.
Pièges courants et contrôle du processus
Réussir une calcination nécessite un contrôle précis des variables clés. Ne pas le faire peut entraîner une réaction incomplète ou des sous-produits indésirables.
Le contrôle de la température est essentiel
La température du processus doit être suffisamment élevée pour déclencher la décomposition, mais rester en dessous du point de fusion du matériau.
Si la température est trop élevée, elle peut provoquer la frittage, où les particules commencent à fusionner. Cela réduit la surface et la réactivité du produit final, ce qui est souvent indésirable.
Gestion de l'atmosphère
La quantité d'air ou de gaz réactif dans le four est soigneusement contrôlée. Introduire trop d'oxygène peut entraîner une oxydation indésirable, transformant effectivement un processus de calcination en un processus de torréfaction.
Faire le bon choix pour votre objectif
Le choix du traitement thermique correct dépend entièrement de votre matériau de départ et du produit final chimique souhaité.
- Si votre objectif principal est d'éliminer le CO₂ ou l'eau d'un minéral : La calcination est le processus correct, car elle utilise la chaleur pour provoquer la décomposition dans un environnement pauvre en oxygène.
- Si votre objectif principal est de convertir un minerai sulfuré en oxyde : La torréfaction est le processus nécessaire, car elle nécessite une atmosphère riche en oxygène pour faciliter une réaction d'oxydation.
- Si votre objectif principal est de décomposer de la matière organique sans combustion : La pyrolyse est le choix correct, car elle exige une atmosphère complètement inerte pour empêcher le matériau de brûler.
En fin de compte, le choix du bon traitement thermique dépend de la compréhension de si vous souhaitez éliminer une partie du matériau ou le faire réagir avec quelque chose de nouveau.
Tableau récapitulatif :
| Aspect | Calcination | Torréfaction | Pyrolyse |
|---|---|---|---|
| Atmosphère | Oxygène limité ou nul | Excès d'air/oxygène | Complètement inerte |
| Objectif principal | Décomposition thermique (ex. : éliminer CO₂, H₂O) | Oxydation (ex. : convertir le sulfure en oxyde) | Décomposer la matière organique |
| Utilisation courante | Matériaux inorganiques (ex. : calcaire, bauxite) | Métallurgie (minerais sulfurés) | Matériaux organiques (ex. : bois, plastiques) |
Prêt à perfectionner votre processus de calcination ? KINTEK est spécialisé dans les fours de laboratoire haute performance et les équipements de traitement thermique conçus pour un contrôle précis de la température et de l'atmosphère. Que vous décomposiez des minéraux ou développiez de nouveaux matériaux, nos solutions garantissent des résultats constants et de haute qualité. Contactez nos experts dès aujourd'hui pour discuter de vos besoins spécifiques en laboratoire et découvrir l'équipement adapté à votre application.
Guide Visuel
Produits associés
- Petite usine de pyrolyse continue à four rotatif électrique pour le chauffage
- Fourneuse de pyrolyse de four rotatif électrique Machine calcineuse Petit four rotatif Four rotatif
- Four à moufle haute température pour déliantage et pré-frittage en laboratoire
- Four de fusion par induction à arc sous vide
- Four à pressage à chaud par induction sous vide 600T pour traitement thermique et frittage
Les gens demandent aussi
- Quels sont les principes d'un four rotatif ? Maîtriser la mécanique du traitement à haute température
- Quels sont les différents types de calcinateurs ? Un guide pour choisir le bon équipement de traitement thermique
- Le four rotatif est-il un four ? Découvrez les différences clés pour le traitement industriel
- Pourquoi y a-t-il des chaînes à l'intérieur d'un four rotatif ? Améliorez l'efficacité et le contrôle grâce à l'échange de chaleur interne
- À quelle température la pyrolyse se produit-elle ? Un guide pour contrôler le rendement de votre produit





