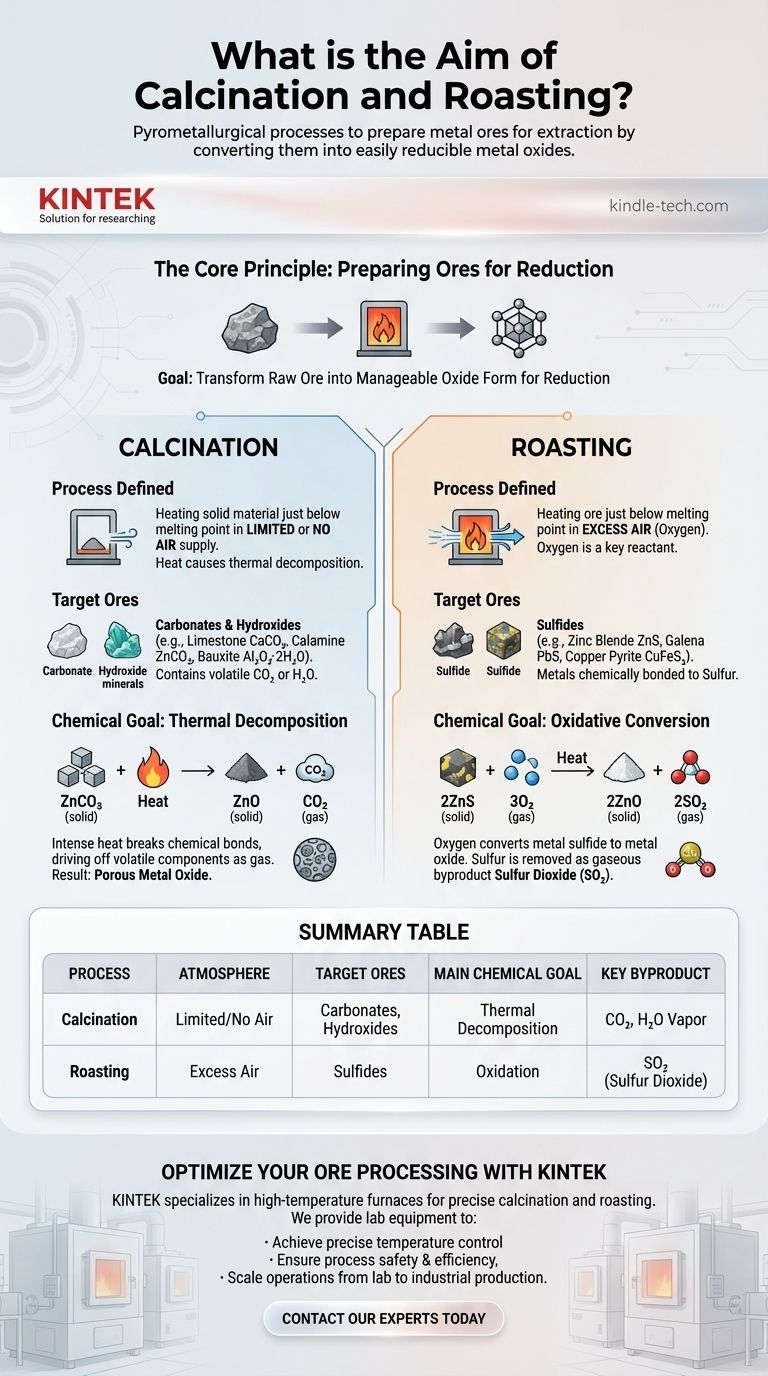
En bref, la calcination et le grillage sont des processus pyrométallurgiques conçus pour préparer les minerais métalliques à l'extraction. Les deux utilisent une chaleur élevée pour convertir les minerais en oxydes métalliques, une forme chimique beaucoup plus facile à réduire en métal pur. La calcination y parvient en décomposant thermiquement le minerai dans un air limité ou sans air, tandis que le grillage utilise un excès d'air pour oxyder le minerai.
La distinction fondamentale réside dans le type de minerai traité. La calcination est destinée aux minerais qui se décomposent par la chaleur seule, comme les carbonates et les hydroxydes. Le grillage est destiné aux minerais qui nécessitent de l'oxygène pour être convertis, principalement les sulfures.

Le principe fondamental : préparer les minerais pour la réduction
L'objectif ultime de la métallurgie est d'extraire un métal pur de son minerai naturel. La plupart des minerais, tels que les carbonates (comme le calcaire) ou les sulfures (comme la blende), ne sont pas facilement convertis directement en métal.
Cependant, les oxydes métalliques sont facilement "réduits" à leur forme métallique, souvent en les faisant réagir avec du carbone (coke) dans un four à haute température. Par conséquent, la calcination et le grillage servent tous deux d'étape de prétraitement cruciale : transformer le minerai brut en cette forme d'oxyde plus facile à gérer.
Comprendre la calcination
Définition du processus
La calcination implique de chauffer un matériau solide à une température élevée, juste en dessous de son point de fusion, en absence totale ou en très faible quantité d'air.
La chaleur elle-même est le principal agent de changement, provoquant la décomposition du matériau sans combustion.
Les minerais cibles
Ce processus est idéal pour les minerais de carbonate et d'hydroxyde. Ces minerais contiennent des composants volatils comme le dioxyde de carbone (CO₂) ou l'eau (H₂O) liés chimiquement au sein de leur structure.
Les exemples courants incluent le calcaire (CaCO₃), la calamine (ZnCO₃) et la bauxite (Al₂O₃·2H₂O).
L'objectif chimique : la décomposition thermique
Le but de la calcination est la décomposition thermique. La chaleur intense rompt les liaisons chimiques dans le minerai, entraînant l'expulsion des composants volatils sous forme de gaz.
Pour un minerai de carbonate comme le carbonate de zinc, la réaction est simple :
ZnCO₃ (solide) + Chaleur → ZnO (solide) + CO₂ (gaz)
Le résultat est un oxyde métallique solide et poreux (oxyde de zinc) prêt pour l'étape suivante de réduction.
Comprendre le grillage
Définition du processus
Le grillage implique de chauffer un minerai à une température élevée, également inférieure à son point de fusion, mais en présence d'un excès d'air (oxygène).
Contrairement à la calcination, l'oxygène est un réactif clé dans le processus.
Les minerais cibles
Le grillage est la méthode standard pour le traitement des minerais de sulfure. Ces minerais contiennent des métaux précieux liés chimiquement au soufre.
Des exemples célèbres incluent la blende (ZnS), la galène (PbS) et la pyrite de cuivre (CuFeS₂).
L'objectif chimique : la conversion oxydative
Le but du grillage est d'utiliser l'oxygène de l'air pour convertir le sulfure métallique en oxyde métallique. Le soufre est éliminé sous forme de sous-produit gazeux, le dioxyde de soufre (SO₂).
Pour un minerai de sulfure comme la blende, la réaction est :
2ZnS (solide) + 3O₂ (gaz) + Chaleur → 2ZnO (solide) + 2SO₂ (gaz)
Cette réaction remplace le soufre par l'oxygène, produisant à nouveau l'oxyde métallique désiré (oxyde de zinc).
Comprendre les compromis et les différences clés
Apport d'air : le facteur déterminant
La différence la plus critique est l'atmosphère à l'intérieur du four.
La calcination nécessite l'exclusion de l'air pour garantir que le minerai se décompose simplement. Le grillage nécessite une abondance d'air pour fournir l'oxygène nécessaire à la réaction d'oxydation.
Gestion des sous-produits
Les sous-produits de chaque processus sont fondamentalement différents et ont des implications environnementales et économiques distinctes.
La calcination produit principalement du dioxyde de carbone (CO₂) ou de la vapeur d'eau, qui sont relativement inoffensifs. Le grillage produit du dioxyde de soufre (SO₂), un polluant atmosphérique majeur responsable des pluies acides. Les fonderies modernes doivent capter ce SO₂, qui est souvent utilisé pour fabriquer de l'acide sulfurique, transformant un déchet nocif en une matière première précieuse.
Pourquoi ne pas simplement calciner un minerai de sulfure ?
Chauffer un minerai de sulfure sans air (calcination) n'éliminerait pas efficacement le soufre ni ne le convertirait en oxyde. Le processus repose sur l'oxygène pour rompre la liaison métal-soufre et former la liaison métal-oxygène plus stable.
Sélectionner le processus de prétraitement correct
Le choix entre la calcination et le grillage n'est pas une question de préférence mais une nécessité chimique dictée par la composition du minerai.
- Si votre objectif principal est de traiter un minerai de carbonate ou d'hydroxyde : Utilisez la calcination pour décomposer thermiquement le minerai et expulser le dioxyde de carbone ou l'eau.
- Si votre objectif principal est de traiter un minerai de sulfure : Utilisez le grillage pour oxyder le minerai avec un excès d'air, le convertissant en oxyde métallique et éliminant le soufre sous forme de dioxyde de soufre.
Associer le processus pyrométallurgique correct à la chimie spécifique du minerai est l'étape fondamentale pour une extraction métallique efficace et réussie.
Tableau récapitulatif :
| Processus | Atmosphère | Minerais cibles | Objectif chimique principal | Sous-produit clé |
|---|---|---|---|---|
| Calcination | Air limité/absent | Carbonates, Hydroxydes | Décomposition thermique | CO₂, Vapeur H₂O |
| Grillage | Excès d'air | Sulfures | Oxydation | SO₂ (Dioxyde de soufre) |
Optimisez votre traitement des minerais avec KINTEK
Comprendre le processus de prétraitement correct est la première étape vers une extraction métallique efficace. KINTEK est spécialisé dans la fourniture de fours robustes et à haute température nécessaires aux opérations précises de calcination et de grillage.
Nous fournissons l'équipement de laboratoire et les consommables essentiels pour vous aider à :
- Atteindre un contrôle précis de la température pour une décomposition thermique ou une oxydation efficace.
- Assurer la sécurité et l'efficacité des processus, que vous travailliez avec des carbonates ou des sulfures.
- Faire évoluer vos opérations de la recherche en laboratoire à la production industrielle.
Prêt à améliorer vos processus pyrométallurgiques ? Contactez nos experts dès aujourd'hui pour discuter de la solution de four parfaite pour la chimie de votre minerai spécifique et vos objectifs de production.
Guide Visuel