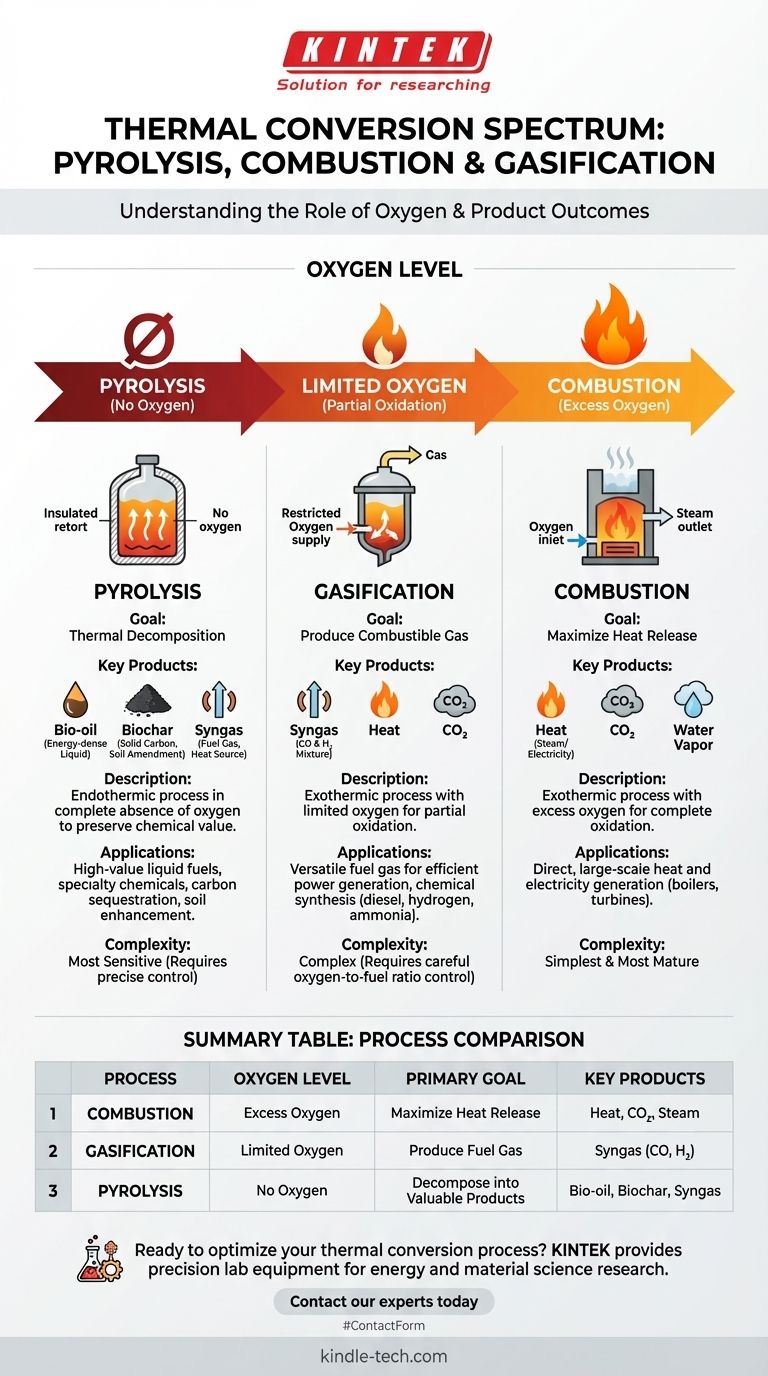
À la base, la différence entre la pyrolyse, la combustion et la gazéification réside dans la quantité d'oxygène présente pendant le processus thermique. La combustion implique une oxydation complète en présence d'un excès d'oxygène pour produire de la chaleur. La gazéification utilise une quantité limitée d'oxygène pour une oxydation partielle afin de créer un gaz combustible. La pyrolyse, en revanche, se produit en l'absence totale d'oxygène, utilisant la chaleur pour décomposer la matière en huiles, gaz et charbon de bois à haute densité énergétique.
Bien que les trois soient des technologies de conversion thermique, l'essentiel est de les considérer non pas comme des processus isolés, mais comme des points sur un spectre contrôlé par l'oxygène. La quantité d'oxygène que vous introduisez détermine directement si votre produit principal est de la chaleur, du gaz combustible ou des produits chimiques de grande valeur.

Le rôle de l'oxygène : un spectre de conversion
Comprendre ces technologies est plus simple si vous les considérez comme un continuum basé sur le rapport oxygène/matière première. Chaque processus a un objectif distinct dicté par son environnement chimique unique.
Combustion : oxydation complète pour une chaleur maximale
La combustion est le processus le plus familier, essentiellement la combustion rapide de matière organique. Elle fonctionne avec une abondance d'oxygène.
L'objectif ici est simple : maximiser le dégagement de chaleur. En fournissant plus qu'assez d'oxygène, le combustible est entièrement oxydé, convertissant son énergie chimique en énergie thermique, en dioxyde de carbone (CO₂) et en eau.
Gazéification : oxydation partielle pour le gaz combustible
La gazéification est un juste milieu. Elle prive délibérément la réaction de l'oxygène nécessaire à une combustion complète.
En utilisant seulement une quantité limitée d'oxygène, la matière organique n'est que partiellement oxydée. Ce processus génère un mélange de gaz combustibles connu sous le nom de gaz de synthèse, ou syngas (principalement du monoxyde de carbone et de l'hydrogène), ainsi que du CO₂ et de la chaleur.
Pyrolyse : décomposition thermique sans oxygène
La pyrolyse se situe à l'extrémité du spectre sans oxygène. Ce n'est pas un processus de combustion mais plutôt une décomposition thermique, semblable à la "cuisson" de la matière première dans un récipient scellé et sans oxygène.
Comme il n'y a pas d'oxygène pour réagir, la matière se décompose en molécules plus petites. Ce processus est endothermique, ce qui signifie qu'il nécessite une source de chaleur externe constante. Il préserve l'énergie de la matière première d'origine sous de nouvelles formes précieuses.
Comparaison des produits et des applications
Les différents environnements chimiques conduisent à des produits très différents, chacun ayant son propre ensemble d'applications. Le choix du processus dépend entièrement du produit final souhaité.
Produits de combustion : chaleur et énergie
Le principal produit de la combustion est une grande quantité de chaleur. Cette chaleur est le plus souvent utilisée pour faire bouillir de l'eau, créer de la vapeur et faire tourner une turbine pour produire de l'électricité. C'est la voie la plus directe du combustible solide à l'énergie.
Produits de gazéification : le syngas comme combustible polyvalent
Le produit principal de la gazéification, le syngas, est très flexible. Il peut être brûlé directement dans un moteur à gaz ou une turbine pour produire de l'électricité, souvent plus efficacement que la combustion directe.
Alternativement, le syngas peut servir de bloc de construction chimique pour synthétiser des carburants liquides (comme le diesel et l'essence), de l'hydrogène, ou des produits chimiques précieux comme le méthanol et l'ammoniac.
Produits de pyrolyse : bio-huile et biochar
La pyrolyse décompose la matière première en trois produits principaux :
- Bio-huile (ou huile de pyrolyse) : Un liquide sombre et à haute densité énergétique qui peut être valorisé en carburants de transport ou utilisé pour produire des produits chimiques spécialisés.
- Biochar : Un solide stable et riche en carbone qui est un excellent amendement du sol et un outil puissant pour la séquestration du carbone.
- Syngas : Une fraction gazeuse qui peut être utilisée pour fournir la chaleur nécessaire pour soutenir la réaction de pyrolyse endothermique elle-même.
Comprendre les compromis
Le choix de la bonne technologie nécessite de reconnaître les compromis inhérents en termes de complexité, d'efficacité et de gestion des matières premières.
Complexité et contrôle du processus
La combustion est la plus simple et la plus mature des trois technologies. La gazéification est plus complexe, nécessitant un contrôle minutieux du rapport oxygène/combustible pour maximiser la qualité du syngas.
La pyrolyse est le processus le plus sensible. Elle exige un environnement véritablement sans oxygène et une gestion précise de la température pour contrôler la distribution finale des produits (huile vs charbon vs gaz).
Bilan énergétique
La combustion et la gazéification sont exothermiques – elles libèrent de l'énergie une fois initiées. Cela les rend auto-entretenues tant que le combustible et l'oxygène sont fournis.
La pyrolyse, étant endothermique, nécessite un apport continu d'énergie pour entraîner la décomposition. Cette énergie est souvent fournie en brûlant une partie du syngas produit, ce qui a un impact sur la production nette d'énergie globale du système.
Faire le bon choix pour votre objectif
Votre décision finale doit être alignée sur votre objectif stratégique.
- Si votre objectif principal est la production directe et à grande échelle de chaleur ou d'électricité : La combustion est la voie la plus établie, la plus rentable et la plus directe.
- Si votre objectif principal est de produire un gaz combustible polyvalent pour une production d'énergie efficace ou une synthèse chimique : La gazéification offre la flexibilité nécessaire pour convertir les matières premières solides en un intermédiaire gazeux précieux.
- Si votre objectif principal est de créer des carburants liquides, des produits chimiques ou des produits du sol séquestrant le carbone de grande valeur : La pyrolyse est le choix optimal, car elle est conçue pour préserver la valeur chimique de ses produits matériels.
En fin de compte, maîtriser ces technologies commence par comprendre que l'oxygène est l'interrupteur de contrôle fondamental qui détermine votre produit final.
Tableau récapitulatif :
| Processus | Niveau d'oxygène | Objectif principal | Produits clés |
|---|---|---|---|
| Combustion | Excès d'oxygène | Maximiser le dégagement de chaleur | Chaleur, CO₂, Vapeur |
| Gazéification | Oxygène limité | Produire du gaz combustible | Syngas (CO, H₂) |
| Pyrolyse | Pas d'oxygène | Décomposer en produits précieux | Bio-huile, Biochar, Syngas |
Prêt à optimiser votre processus de conversion thermique ? Que vous produisiez de la chaleur, du syngas ou des bioproduits de grande valeur, l'équipement de laboratoire de précision de KINTEK est conçu pour répondre à vos besoins spécifiques. Des réacteurs aux analyseurs de gaz, nous fournissons des solutions fiables pour les laboratoires axés sur l'énergie et la science des matériaux. Contactez nos experts dès aujourd'hui pour discuter de la manière dont nous pouvons soutenir vos objectifs de recherche et développement !
Guide Visuel