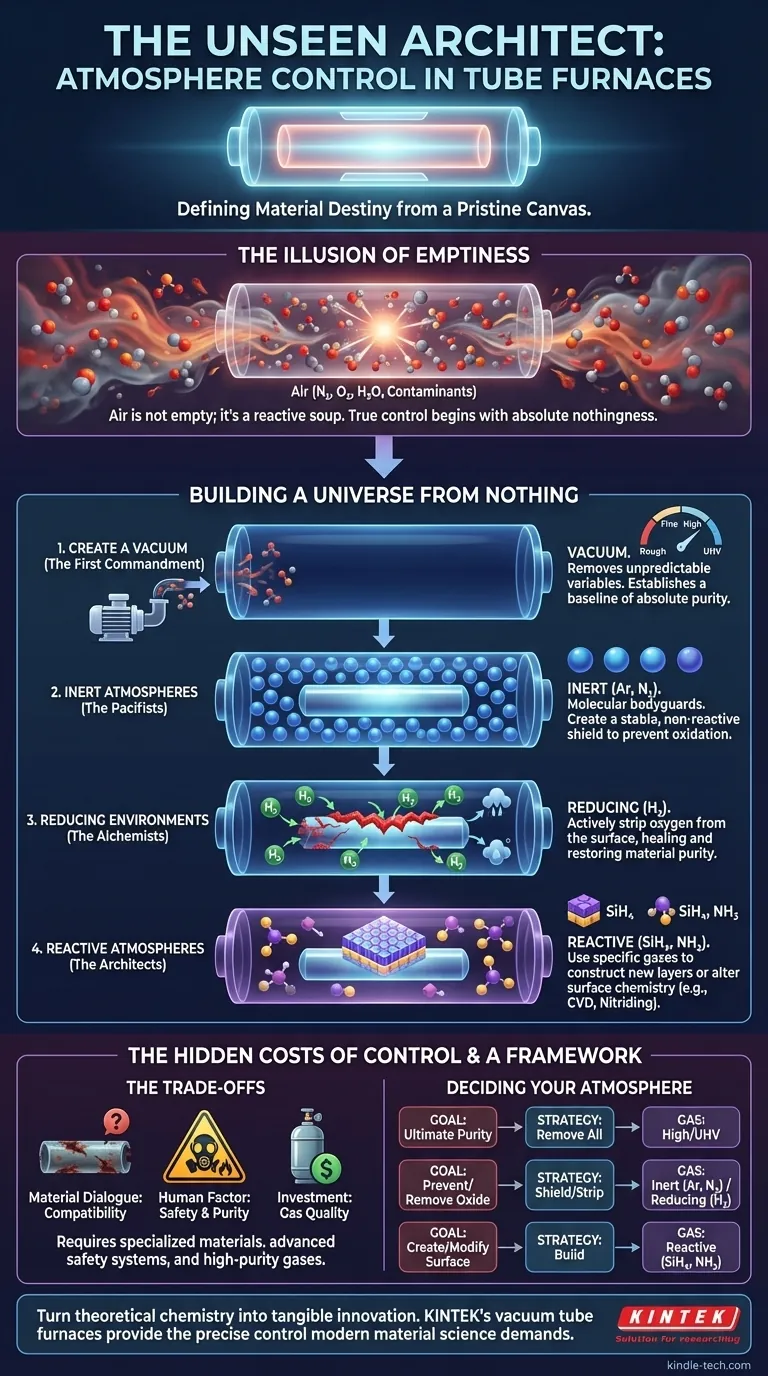
L'illusion du vide
En science des matériaux, l'ennemi le plus dangereux est souvent invisible. L'air que nous respirons, un mélange apparemment bénin d'azote et d'oxygène, devient un agent violemment réactif à haute température. Pour un ingénieur synthétisant un nouvel alliage ou un chercheur cultivant un cristal parfait, l'air ambiant n'est pas un espace vide ; c'est une soupe chaotique de contaminants attendant de ruiner une semaine de travail.
C'est le premier obstacle psychologique à surmonter : réaliser que le vrai contrôle commence non pas par l'ajout de quelque chose, mais par le retrait de tout. L'objectif est de créer une poche de néant absolu — un vide parfait — et à partir de cette toile immaculée, de construire un monde nouveau et précisément contrôlé pour que votre matériau puisse naître.
Construire un univers à partir de rien
Un four tubulaire sous vide est plus qu'un simple appareil de chauffage ; c'est un créateur d'univers à petite échelle. Sa puissance réside dans sa capacité à d'abord atteindre le vide, préparant ainsi le terrain pour toute atmosphère contrôlée dont un processus pourrait avoir besoin.
Le premier commandement : créer un vide
L'évacuation est la première étape non négociable. En éliminant l'air, vous supprimez les variables imprévisibles : oxygène, humidité et autres gaz traces. Ce n'est pas seulement un nettoyage ; c'est l'établissement d'une base de pureté absolue. La qualité de ce « néant » peut être adaptée :
- Vide grossier et fin : Suffisant pour de nombreux processus où l'objectif est une oxydation minimale.
- Vide poussé et ultra-vide (UHV) : Essentiel pour les applications sensibles telles que la recherche sur les semi-conducteurs ou le dépôt de couches minces, où même une seule molécule errante peut constituer un défaut critique.
Les pacifistes : les atmosphères inertes
Une fois le vide créé, la première impulsion est souvent de le protéger. Les gaz inertes sont des gardes du corps moléculaires. Le remplissage du tube avec de l'argon ou de l'azote crée un bouclier stable et non réactif autour de l'échantillon.
Ces gaz ne participent pas à la réaction ; leur rôle est simplement d'être présents, empêchant le chaos du monde extérieur de s'infiltrer et arrêtant les réactions indésirables comme l'oxydation. L'hélium, avec sa haute conductivité thermique, peut même aider en accélérant les cycles de chauffage et de refroidissement.
Les alchimistes : les atmosphères réductrices
Parfois, la prévention ne suffit pas. Un matériau peut déjà avoir une fine couche d'oxyde à sa surface. C'est là qu'interviennent les atmosphères réductrices. Ce sont les alchimistes du traitement des matériaux.
L'introduction d'un mélange contrôlé d'hydrogène (H₂) élimine activement les atomes d'oxygène de la surface du matériau, le guérissant et le restaurant dans un état métallique pur. C'est un processus de purification qui inverse activement les dommages, garantissant que le matériau final est chimiquement vierge.
Les architectes : les atmosphères réactives
Le niveau de contrôle final n'est pas seulement de protéger ou de purifier, mais de construire. Les atmosphères réactives utilisent des gaz spécifiques comme éléments de construction pour créer de nouvelles couches ou modifier la chimie de surface du matériau.
Dans des processus tels que le dépôt chimique en phase vapeur (CVD), des gaz comme le silane (SiH₄) sont introduits pour se décomposer à haute température, déposant un film mince de silicium. Dans la nitruration, l'ammoniac (NH₃) est utilisé pour durcir la surface d'un métal. C'est de l'architecture matérielle à l'échelle atomique, et cela exige des équipements capables de manipuler ces éléments de construction souvent corrosifs, tels que des fours équipés de tubes en quartz ou en alumine.
Les coûts cachés du contrôle
Maîtriser le contrôle atmosphérique est un jeu de compromis, où chaque choix a des conséquences.
Le dialogue des matériaux
Les composants du four doivent être compatibles avec l'atmosphère choisie. Un gaz réactif comme l'ammoniac attaquera un tube métallique standard, entraînant une défaillance de l'équipement et une contamination de l'échantillon. Cela nécessite une compréhension approfondie de la compatibilité des matériaux — un dialogue entre votre gaz de processus et votre four. Le choix d'un système avec le bon tube et la bonne technologie d'étanchéité est primordial.
Le facteur humain
La puissance de gaz tels que l'hydrogène et le monoxyde de carbone s'accompagne de responsabilités. Leur inflammabilité et leur toxicité exigent le respect, nécessitant des interverrouillages de sécurité avancés, une ventilation et des systèmes de détection de gaz. De même, la pureté de votre source de gaz est un investissement direct dans la qualité de votre résultat. Économiser sur la pureté du gaz, c'est parier contre votre propre succès.
Un cadre pour décider de votre atmosphère
L'objectif de votre processus dicte votre choix d'atmosphère. La logique est simple :
| Résultat souhaité | Stratégie atmosphérique | Gaz courants |
|---|---|---|
| Pureté ultime | Éliminer toutes les molécules réactives. | Vide poussé/ultra-vide |
| Prévention de l'oxydation | Protéger l'échantillon avec un tampon non réactif. | Argon (Ar), Azote (N₂) |
| Élimination/Réduction des oxydes | Éliminer activement l'oxygène de la surface. | Hydrogène (H₂) |
| Création/Modification de surface | Introduire des atomes spécifiques pour construire ou modifier la surface. | Silane (SiH₄), Ammoniac (NH₃) |
Atteindre ce niveau de contrôle nécessite non seulement des connaissances, mais aussi les bons instruments. Les fours tubulaires sous vide de KINTEK sont conçus pour fournir le contrôle atmosphérique précis et fiable qu'exige la science des matériaux moderne, de l'UHV aux mélanges de gaz réactifs complexes. Ce sont les outils qui transforment la chimie théorique en innovation tangible. Pour trouver le four adapté à l'univers que vous devez construire, Contactez nos experts
Guide Visuel
Produits associés
- Four tubulaire rotatif à fonctionnement continu scellé sous vide
- Four à tube sous vide haute pression de laboratoire
- Four tubulaire rotatif inclinable sous vide de laboratoire
- Four tubulaire CVD à chambre divisée avec station de vide, équipement de dépôt chimique en phase vapeur
- Four à atmosphère contrôlée 1200℃, four à atmosphère inerte à l’azote
Articles associés
- Explorer les avantages des fours à tubes rotatifs dans les applications industrielles et de laboratoire
- Explorer les avantages et les applications des fours rotatifs : un guide complet
- Débloquer l'efficacité : Le guide ultime des fours à tubes rotatifs
- La Quête de Pureté : Comment un Four à Vide Scellé Assure la Certitude Métallurgique
- La géométrie de la chaleur : pourquoi le mouvement est essentiel dans la synthèse des matériaux




















