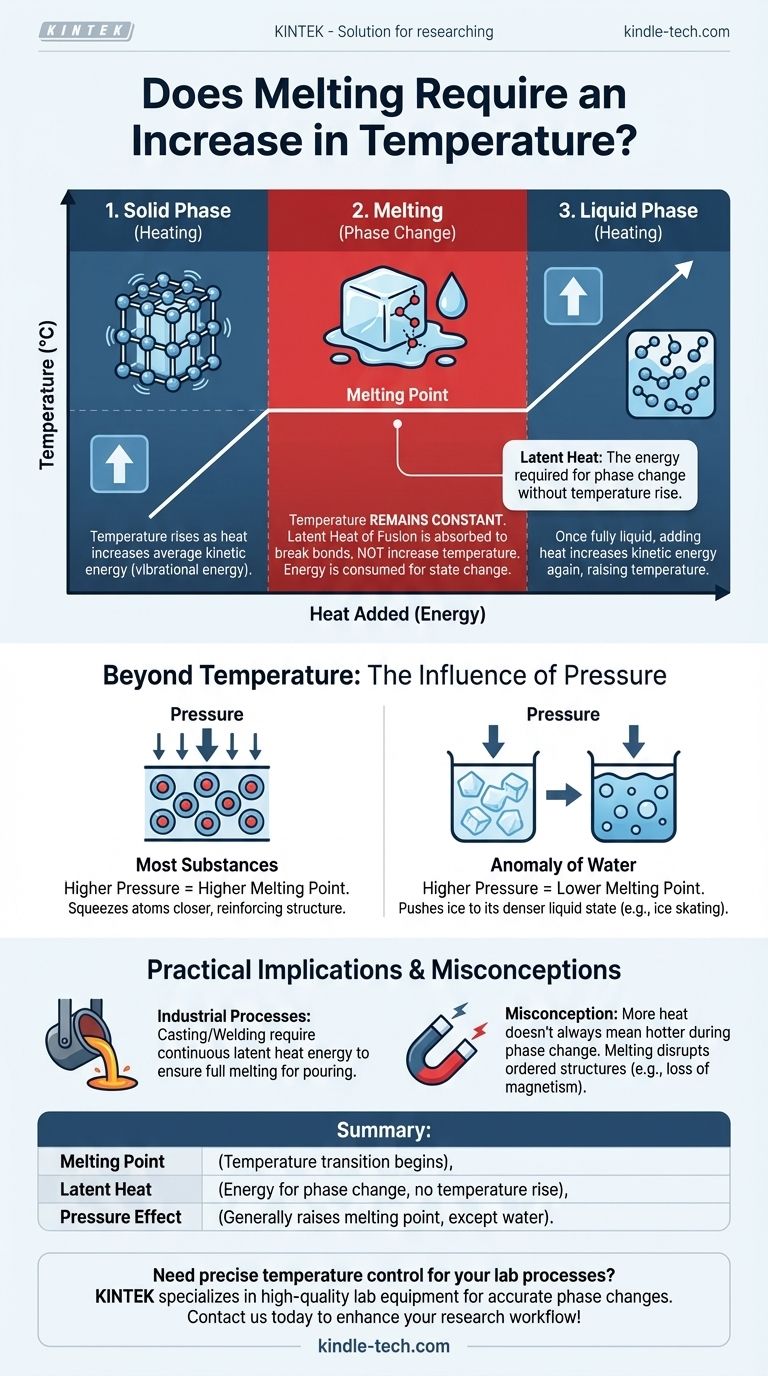
La relation entre la chaleur, la température et la fusion est souvent mal comprise. Pour faire fondre un solide, il faut lui ajouter de l'énergie sous forme de chaleur. Ce processus élève d'abord la température de la substance jusqu'à ce qu'elle atteigne son point de fusion spécifique. Cependant, pendant la transition réelle du solide au liquide, la température reste constante même si plus de chaleur est fournie.
Bien qu'une substance doive d'abord être chauffée jusqu'à son point de fusion, le processus de fusion lui-même se produit à une température constante. L'énergie ajoutée, connue sous le nom de chaleur latente, est utilisée pour briser les liaisons de la structure solide, et non pour augmenter la température globale de la substance.

La physique d'un changement de phase
Pour comprendre pourquoi la fusion se produit à une température constante, nous devons d'abord distinguer la chaleur de la température. Elles sont liées, mais ne sont pas identiques.
Qu'est-ce que la température ?
La température est une mesure de l'énergie cinétique moyenne des atomes ou des molécules au sein d'une substance. Dans un solide, ces atomes sont enfermés dans une structure fixe, comme un réseau cristallin, mais ils vibrent constamment. Lorsque vous ajoutez de la chaleur, vous augmentez cette énergie vibratoire, ce que nous mesurons comme une augmentation de la température.
Atteindre le point de fusion
À mesure que vous continuez à ajouter de la chaleur, les atomes vibrent de plus en plus violemment. Finalement, ils atteignent un niveau d'énergie où les vibrations sont suffisamment fortes pour commencer à briser les liaisons rigides qui les maintiennent dans leurs positions fixes. Cette température spécifique est le point de fusion.
Le rôle de la chaleur latente
Au point de fusion, un changement critique se produit. Toute énergie thermique supplémentaire que vous fournissez – connue sous le nom de chaleur latente de fusion – est désormais utilisée exclusivement pour briser les liaisons restantes de la structure solide. Elle n'est pas utilisée pour faire vibrer les molécules plus rapidement.
Parce que l'énergie est consommée pour changer l'état de la substance (du solide au liquide) plutôt que pour augmenter son énergie cinétique, la température reste parfaitement constante jusqu'à ce que tout le solide se soit transformé en liquide.
L'état liquide
Une fois que le dernier morceau de solide a fondu, la substance est entièrement à l'état liquide. À partir de ce moment, toute chaleur supplémentaire que vous ajoutez augmentera à nouveau l'énergie cinétique des molécules, provoquant l'élévation de la température du liquide.
Au-delà de la température : l'influence de la pression
La température n'est pas le seul facteur qui régit la fusion. La pression joue un rôle crucial, et parfois contre-intuitif.
Comment la pression affecte la fusion
Pour la plupart des substances, l'augmentation de la pression externe élève le point de fusion. Une pression élevée comprime physiquement les atomes, renforçant la structure solide. Cela signifie qu'une plus grande énergie (et donc une température plus élevée) est nécessaire pour briser les liaisons et permettre à la substance de fondre.
L'anomalie de l'eau
L'eau est une exception notable. La forme solide de l'eau (la glace) est moins dense que sa forme liquide. L'augmentation de la pression sur la glace la pousse vers son état plus dense – l'eau liquide. Cela signifie que sous haute pression, la glace peut fondre à une température inférieure à son point de fusion standard de 0°C (32°F). Ce principe contribue à la façon dont la lame d'un patin à glace glisse sur la glace.
Implications pratiques et idées fausses
Comprendre ce processus n'est pas seulement académique ; il a des conséquences directes en science et en ingénierie.
Idée fausse : Plus de chaleur signifie toujours plus chaud
L'idée fausse la plus courante est que l'ajout continu de chaleur rendra toujours quelque chose plus chaud. Lors d'un changement de phase, comme la fusion ou l'ébullition, c'est incorrect. L'apport d'énergie effectue le travail de changement d'état du matériau, et non d'augmentation de sa température.
Pourquoi cela est important en pratique
Dans les processus industriels comme la coulée ou le soudage des métaux, ce principe est essentiel. Un four doit non seulement amener un métal à son point de fusion, mais aussi fournir une quantité significative et continue d'énergie supplémentaire (la chaleur latente) pour s'assurer que toute la masse devienne entièrement liquide pour la coulée. De même, la fusion perturbe la structure atomique ordonnée des matériaux. C'est pourquoi chauffer un morceau d'acier magnétisé au-delà d'un certain point (sa température de Curie, qui est liée mais distincte de son point de fusion) lui fera perdre son magnétisme, car les domaines magnétiques organisés sont brisés.
Faire le bon choix pour votre objectif
Votre application détermine quelle partie de ce processus est la plus importante pour vous.
- Si votre objectif principal est de comprendre la physique de base : Rappelez-vous que la température est constante pendant un changement de phase ; l'énergie ajoutée est appelée chaleur latente et est utilisée pour changer l'état.
- Si votre objectif principal est la science des matériaux ou l'ingénierie : Reconnaissez que la fusion complète d'une substance nécessite un apport d'énergie précis et continu, même après qu'elle ait atteint sa température de fusion.
- Si vous considérez les effets environnementaux : Sachez que la pression peut modifier considérablement le point de fusion d'une substance, l'augmentant pour la plupart des matériaux mais l'abaissant pour une exception importante comme l'eau.
Comprendre cette distinction entre température et énergie thermique est fondamental pour contrôler et prédire le comportement de tout matériau.
Tableau récapitulatif :
| Concept | Description |
|---|---|
| Point de fusion | Température à laquelle un solide commence à passer à l'état liquide. |
| Chaleur latente de fusion | Énergie absorbée pendant la fusion sans changement de température. |
| Effet de la pression | Une pression élevée augmente le point de fusion (sauf pour l'eau, qui le diminue). |
| Application pratique | Critique pour les processus industriels comme la coulée et le soudage des métaux. |
Besoin d'un contrôle précis de la température pour vos processus de laboratoire ? KINTEK est spécialisé dans les équipements de laboratoire de haute qualité, y compris les fours et les systèmes de chauffage, conçus pour gérer les changements de phase comme la fusion avec précision. Que vous travailliez avec des métaux, des polymères ou d'autres matériaux, nos solutions garantissent une gestion efficace de l'énergie et des résultats constants. Contactez-nous dès aujourd'hui pour découvrir comment nos équipements de laboratoire peuvent améliorer votre recherche ou votre flux de production !
Guide Visuel