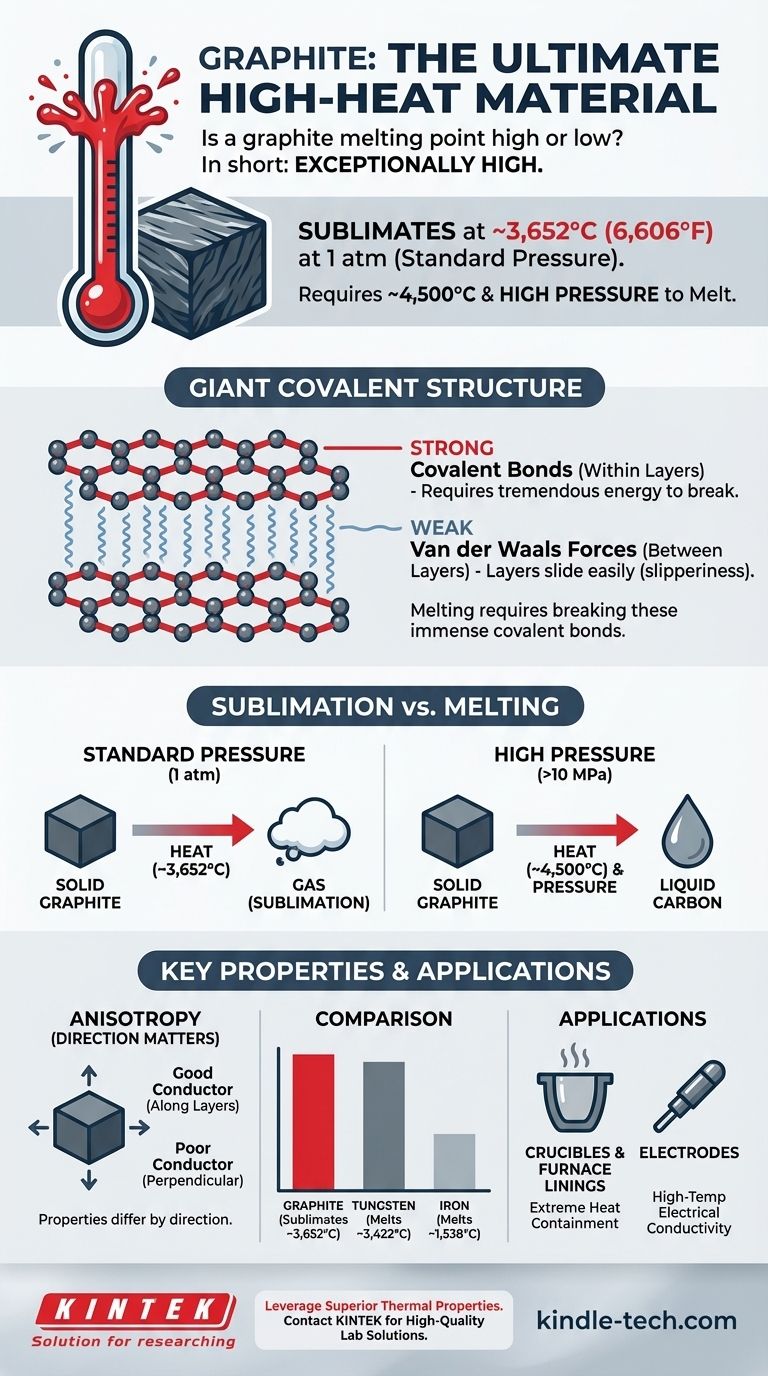
En bref, le graphite possède un point de fusion exceptionnellement élevé. Plus précisément, à pression atmosphérique standard, il se sublime — passant directement de l'état solide à gazeux — à une température extrême d'environ 3 652 °C (6 606 °F). Pour atteindre une véritable fusion à l'état liquide, des températures très élevées (environ 4 500 °C) et une pression élevée sont nécessaires.
La raison principale de la résilience thermique du graphite est sa structure atomique. Faire fondre le graphite n'est pas une simple question de séparer ses couches, mais de rompre les liaisons covalentes immensément fortes qui forment le matériau lui-même, ce qui nécessite une quantité énorme d'énergie.

La structure covalente géante du graphite
Pour comprendre le point de fusion élevé du graphite, il faut d'abord comprendre sa structure. Ce n'est pas une simple collection de molécules, mais une structure covalente géante.
Liaisons covalentes fortes au sein des couches
Chaque atome de carbone dans le graphite est lié à trois autres atomes de carbone par de liaisons covalentes fortes. Ces atomes forment un réseau hexagonal, créant de vastes feuilles ou couches bidimensionnelles.
Ces liaisons covalentes sont du même type que celles trouvées dans les diamants et sont incroyablement fortes, nécessitant une quantité massive d'énergie thermique pour être rompues.
Forces faibles entre les couches
Bien que les atomes au sein d'une couche soient fortement liés, les couches elles-mêmes sont maintenues ensemble par des forces intermoléculaires beaucoup plus faibles appelées forces de van der Waals.
Ces forces faibles sont facilement surmontées, ce qui explique pourquoi le graphite est doux et glissant au toucher. Cette propriété permet aux couches de glisser, faisant du graphite un excellent matériau pour la mine de crayon et comme lubrifiant solide.
Ce que signifie réellement la « fusion » pour le graphite
Cette distinction entre les deux types de forces est cruciale. Le caractère glissant du graphite est dû aux forces faibles entre les couches, mais son point de fusion est dicté par les liaisons covalentes fortes au sein des couches.
Pour faire passer le graphite de l'état solide à l'état liquide, il faut fournir suffisamment d'énergie pour rompre les liaisons covalentes fortes et permettre aux atomes de carbone de se déplacer librement. C'est pourquoi il possède l'un des points de fusion/sublimation les plus élevés de tous les matériaux connus.
Comprendre les compromis et les nuances
Les propriétés du graphite ne sont pas uniformes, et son comportement sous l'effet de la chaleur s'accompagne de conditions et de limites spécifiques qui sont cruciales pour les applications pratiques.
Sublimation contre fusion
À pression atmosphérique normale, le graphite ne fond pas. Lorsqu'il est chauffé, il atteint son point de sublimation et se transforme directement en gaz.
Une véritable phase liquide du carbone n'existe qu'à de très hautes pressions, à partir d'environ 10 mégapascals (MPa), soit environ 100 fois la pression atmosphérique standard.
Anisotropie : la direction compte
Le graphite est un matériau anisotrope, ce qui signifie que ses propriétés diffèrent selon la direction de mesure.
Il conduit très bien la chaleur et l'électricité le long de ses couches, mais c'est un mauvais conducteur perpendiculairement à celles-ci. Cela doit être pris en compte dans les applications de gestion thermique.
Comparaison avec le diamant et les métaux
Le point de sublimation du graphite est comparable à, et dans certaines conditions dépasse, celui du diamant — un autre allotrope du carbone. Les deux sont élevés pour la même raison : rompre les liaisons covalentes fortes.
Comparé aux métaux, le graphite se distingue. Par exemple, le fer fond à 1 538 °C et le tungstène, l'un des métaux à point de fusion le plus élevé, fond à 3 422 °C — toujours en dessous du point de sublimation du graphite.
Faire le bon choix pour votre application
Comprendre ces principes vous permet de sélectionner et d'utiliser efficacement le graphite en fonction de votre objectif spécifique.
- Si votre objectif principal est le confinement thermique extrême : Le graphite est un choix de premier ordre pour les creusets, les revêtements de fours et les tuyères de fusée en raison de son point de sublimation incroyablement élevé et de sa stabilité structurelle à des températures où la plupart des métaux seraient liquides ou gazeux.
- Si votre objectif principal est la conductivité électrique à haute température : Le graphite est idéal pour les électrodes dans les fours à arc électrique, car il peut résister à l'immense chaleur générée tout en conduisant efficacement des courants électriques massifs.
- Si votre objectif principal est la compréhension de la science des matériaux : N'oubliez pas que le point de fusion d'un matériau est fondamentalement lié à la force des liaisons qui maintiennent ses atomes ensemble, et le graphite est un exemple classique de structure covalente géante.
En fin de compte, le point de fusion élevé du graphite est une conséquence directe de sa structure atomique robuste, ce qui en fait l'un des matériaux les plus résilients thermiquement connus.
Tableau récapitulatif :
| Propriété | Valeur / Description |
|---|---|
| Point de sublimation | ~3 652 °C (6 606 °F) à 1 atm |
| Point de fusion | ~4 500 °C (nécessite une haute pression) |
| Caractéristique structurelle clé | Structure covalente géante avec des liaisons fortes au sein des couches |
| Principale limitation thermique | Oxydation dans l'air à des températures supérieures à ~400 °C |
Tirez parti des propriétés thermiques supérieures du graphite dans votre laboratoire
La résistance exceptionnelle à la chaleur du graphite le rend indispensable pour les applications à haute température telles que les revêtements de fours, les creusets et les électrodes.
Chez KINTEK, nous sommes spécialisés dans la fourniture d'équipements et de consommables de laboratoire de haute qualité, y compris des produits en graphite de première qualité adaptés aux environnements de laboratoire exigeants. Nos matériaux garantissent fiabilité, performance et sécurité à des températures extrêmes.
Prêt à améliorer vos processus à haute température ? Contactez nos experts dès aujourd'hui pour trouver la solution en graphite parfaite pour vos besoins spécifiques !
Guide Visuel
Produits associés
- Four de graphitation sous vide à ultra-haute température au graphite
- Four de traitement thermique sous vide graphite 2200 ℃
- Four de graphitisation sous vide horizontal à haute température de graphite
- Four de graphitisation sous vide vertical à haute température
- Grand four de graphitisation sous vide vertical en graphite
Les gens demandent aussi
- Quelle est la température d'absorption atomique dans un four en graphite ? Maîtriser le programme de chauffage multi-étapes
- Quelle est la plage de température d'un four à graphite ? Atteignez jusqu'à 3000°C pour le traitement des matériaux avancés.
- Quels sont les avantages et les inconvénients du four à graphite ? Libérez les performances de chaleur extrême
- Quelle est la fonction du four à graphite ? Atteindre une chaleur extrême pour l'analyse et le traitement des matériaux
- Quels sont les inconvénients du four à graphite ? Limitations clés et coûts opérationnels



















