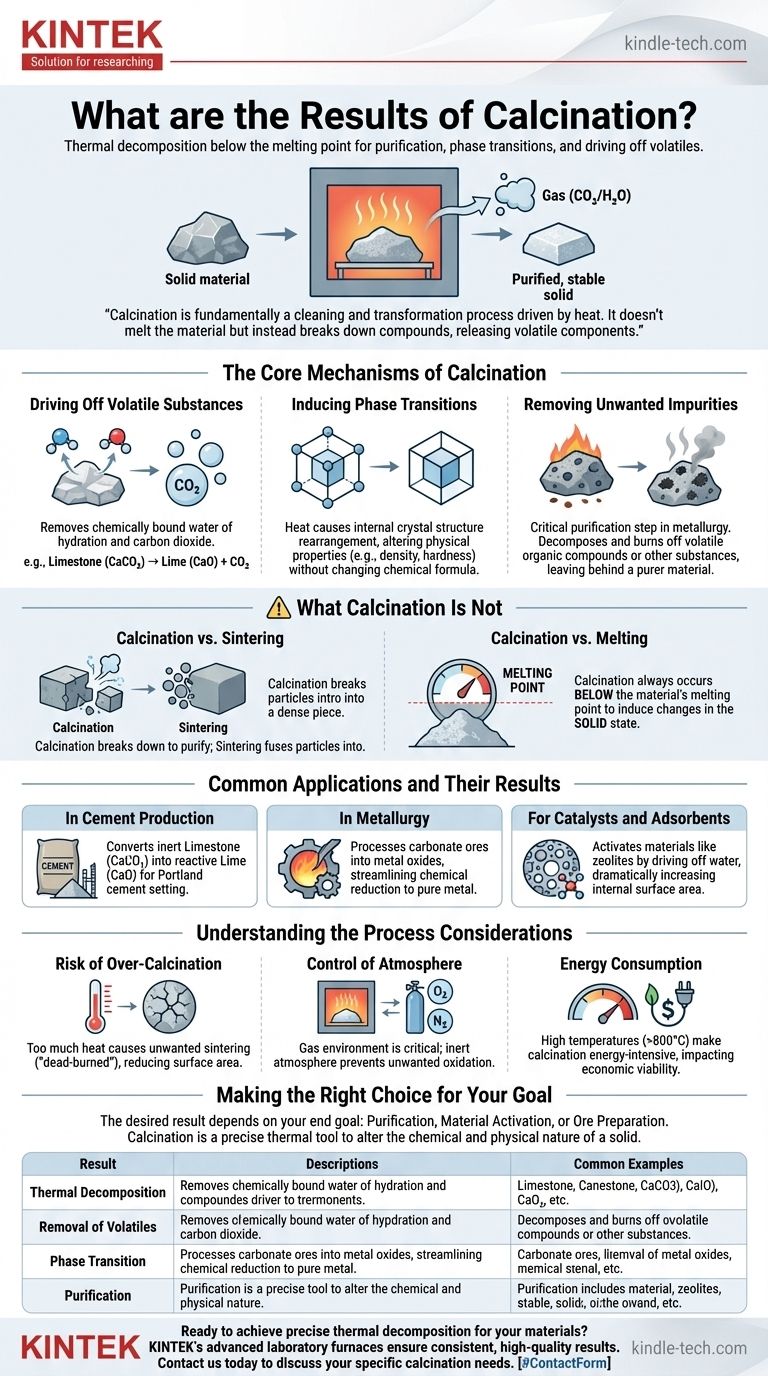
Le résultat principal de la calcination est la décomposition thermique d'un matériau solide. Ce processus de chauffage à haute température, mené en dessous du point de fusion du matériau, est conçu pour éliminer les substances volatiles, induire des transitions de phase ou purifier le matériau en décomposant des composés et en chassant des composants comme l'eau et le dioxyde de carbone.
La calcination est fondamentalement un processus de nettoyage et de transformation piloté par la chaleur. Elle ne fait pas fondre le matériau, mais décompose plutôt les composés qu'il contient, libérant les composants volatils pour produire un produit solide purifié, plus stable ou plus réactif.

Les mécanismes fondamentaux de la calcination
Pour comprendre les résultats, nous devons d'abord comprendre ce qui arrive à un matériau au niveau chimique et physique pendant ce processus.
Élimination des substances volatiles
Le résultat le plus courant de la calcination est l'élimination des composants volatils qui sont chimiquement liés à la structure du solide. La chaleur fournit l'énergie nécessaire pour rompre ces liaisons.
Cela inclut l'élimination de l'eau d'hydratation des minéraux hydratés et l'expulsion du dioxyde de carbone des matériaux carbonatés. L'exemple classique est la calcination du calcaire (carbonate de calcium, CaCO₃) pour produire de la chaux (oxyde de calcium, CaO) pour le ciment.
Induction de transitions de phase
La chaleur peut également provoquer le réarrangement de la structure cristalline interne d'un matériau en une forme différente, souvent plus stable ou plus utile.
Il s'agit d'une transition de phase. Bien que la formule chimique du matériau reste la même, ses propriétés physiques — comme la densité, la dureté et la réactivité chimique — peuvent changer de manière significative.
Élimination des impuretés indésirables
En métallurgie et dans le traitement des matériaux, la calcination est une étape de purification critique.
En contrôlant soigneusement la température, les composés organiques volatils ou d'autres substances indésirables présentes dans un minerai peuvent être décomposés et brûlés, laissant derrière eux un matériau désiré plus concentré et plus pur.
Ce que la calcination n'est pas : une distinction clé
Comprendre ce que la calcination ne fait pas est tout aussi important que de comprendre ce qu'elle fait. Son but est souvent confondu avec d'autres processus thermiques.
Calcination vs. Frittage
Ces deux processus ont des objectifs opposés. La calcination décompose un matériau pour le purifier ou en chasser des composants.
Le frittage, en revanche, utilise la chaleur pour fusionner de petites particules, les soudant en une seule pièce dense et plus solide. La calcination prépare la poudre ; le frittage la consolide.
Calcination vs. Fusion
Une règle critique de la calcination est qu'elle se produit toujours en dessous du point de fusion du matériau. L'objectif est d'induire des changements chimiques et physiques pendant que la substance reste à l'état solide.
Applications courantes et leurs résultats
Le résultat spécifique de la calcination est directement lié à son application industrielle.
Dans la production de ciment
La calcination du calcaire est l'étape fondamentale de la fabrication du ciment Portland. Le résultat est la conversion du carbonate de calcium inerte en oxyde de calcium (chaux) hautement réactif, qui est l'ingrédient principal permettant au ciment de prendre et de durcir.
En métallurgie
La calcination est utilisée pour traiter les minerais métalliques avant l'étape finale de la fusion. Par exemple, les minerais carbonatés sont convertis en leurs formes d'oxydes métalliques, qui sont beaucoup plus faciles à réduire chimiquement en un métal pur.
Pour les catalyseurs et les adsorbants
Des matériaux comme les zéolithes et l'alumine sont activés par calcination. Le processus chasse l'eau de leurs pores microscopiques, augmentant considérablement leur surface interne et les rendant très efficaces comme catalyseurs ou adsorbants chimiques.
Comprendre les considérations du processus
L'obtention du résultat souhaité nécessite un contrôle minutieux, car plusieurs facteurs peuvent entraîner des résultats indésirables.
Risque de sur-calcination
Appliquer trop de chaleur ou pendant trop longtemps peut être contre-productif. Cela peut provoquer un frittage indésirable, ce qui réduit la surface et la réactivité du matériau. On parle souvent alors de production d'un matériau "mort-calciné".
Contrôle de l'atmosphère
L'environnement gazeux à l'intérieur du four est critique. La calcination à l'air peut provoquer une oxydation, ce qui peut être souhaitable pour certains processus mais préjudiciable pour d'autres. L'utilisation d'une atmosphère inerte (comme l'azote) prévient ces réactions indésirables.
Consommation d'énergie
Le chauffage des matériaux aux températures élevées requises pour la calcination (souvent >800°C) est un processus extrêmement énergivore. Le coût de l'énergie est un facteur majeur dans la viabilité économique de toute opération de calcination.
Faire le bon choix pour votre objectif
Le "résultat" que vous attendez de la calcination dépend entièrement de votre objectif final.
- Si votre objectif principal est la purification et la décomposition : Votre objectif clé est un contrôle précis de la température pour chasser les substances volatiles sans provoquer de changements de phase indésirables ou de frittage.
- Si votre objectif principal est l'activation des matériaux (par exemple, pour les catalyseurs) : Votre objectif est de maximiser la surface en éliminant l'eau adsorbée, ce qui nécessite des rampes de température soigneuses et un contrôle strict de l'atmosphère.
- Si votre objectif principal est de préparer un minerai pour la fusion : Le résultat principal est la conversion d'un carbonate ou d'un hydrate complexe en un oxyde plus simple, ce qui simplifie la réduction chimique ultérieure en métal pur.
En fin de compte, la calcination est un outil thermique précis utilisé pour modifier fondamentalement la nature chimique et physique d'un solide afin de le préparer à son usage final.
Tableau récapitulatif :
| Résultat de la calcination | Description | Exemple courant |
|---|---|---|
| Décomposition thermique | Décomposition des composés par la chaleur en dessous du point de fusion. | CaCO₃ (calcaire) → CaO (chaux) + CO₂ |
| Élimination des substances volatiles | Élimination de l'eau (déshydratation) ou du dioxyde de carbone (décarbonatation). | Séchage et activation de catalyseurs comme les zéolithes. |
| Transition de phase | Changement de structure cristalline pour modifier les propriétés physiques comme la dureté. | Conversion d'un minéral en une forme cristalline plus stable. |
| Purification | Élimination des impuretés organiques ou d'autres contaminants d'un minerai. | Préparation des minerais métalliques pour la fusion. |
Prêt à réaliser une décomposition thermique précise pour vos matériaux ?
Les fours de laboratoire avancés de KINTEK sont conçus pour le contrôle exact de la température et la gestion de l'atmosphère requis pour des processus de calcination réussis. Que vous purifiiez des minerais, activiez des catalyseurs ou produisiez du ciment, notre équipement garantit des résultats constants et de haute qualité tout en optimisant l'efficacité énergétique.
Contactez-nous dès aujourd'hui en utilisant le formulaire ci-dessous pour discuter de vos besoins spécifiques en matière de calcination. Nos experts vous aideront à sélectionner la solution parfaite pour transformer vos matériaux et améliorer les capacités de votre laboratoire.
Guide Visuel
Produits associés
- Petite usine de pyrolyse continue à four rotatif électrique pour le chauffage
- Fourneuse de pyrolyse de four rotatif électrique Machine calcineuse Petit four rotatif Four rotatif
- Four de graphitisation sous vide vertical à haute température
- Four de graphitation à décharge par le bas pour matériaux en graphite pour matériaux carbonés
Les gens demandent aussi
- Quels sont les principes d'un four rotatif ? Maîtriser la mécanique du traitement à haute température
- Quelles sont les caractéristiques des modes de mouvement du lit par glissement, affaissement et roulement ? Optimisez votre processus rotatif
- Comment les fours rotatifs sont-ils chauffés ? Explication des méthodes de chauffage direct et indirect
- Quels sont les différents types de calcinateurs ? Un guide pour choisir le bon équipement de traitement thermique
- Quel est le processus du four rotatif ? Réaliser une transformation précise des matériaux industriels



