À la base, la calcination est un processus de purification. Elle utilise une chaleur élevée — soigneusement contrôlée pour rester en dessous du point de fusion du matériau — afin d'induire des changements chimiques. Dans un environnement avec peu ou pas d'air, ce processus expulse les substances volatiles comme le dioxyde de carbone ou l'eau, transformant une matière première en une forme plus concentrée et stable.
La véritable signification de la calcination n'est pas seulement le chauffage, mais une transformation chimique contrôlée. Elle sert d'étape préparatoire critique pour décomposer les composés et éliminer les impuretés, rendant une matière première adaptée aux processus ultérieurs comme l'extraction des métaux.

Comment fonctionne fondamentalement la calcination
La calcination est un traitement thermique précis conçu pour modifier la composition chimique d'un matériau, et non son état physique de solide à liquide. Ceci est réalisé grâce à trois principes clés agissant de concert.
Le rôle de la chaleur élevée (en dessous du point de fusion)
Le processus repose sur l'application d'une énergie thermique suffisante pour briser des liaisons chimiques spécifiques au sein d'un composé.
En maintenant la température en dessous du point de fusion, le matériau reste solide. Cela garantit que l'objectif est la décomposition chimique, et non un changement de phase.
L'atmosphère contrôlée (air limité)
La calcination est généralement effectuée en l'absence ou avec un apport très limité d'air.
C'est essentiel car cela prévient l'oxydation ou la combustion. L'objectif est de décomposer le matériau existant, et non de le faire réagir avec l'oxygène de l'air.
Le résultat : la décomposition thermique
La chaleur fournit l'énergie nécessaire pour décomposer le matériau en deux parties : le solide désiré et un gaz volatile qui est expulsé.
Un exemple classique est la calcination du calcaire (carbonate de calcium, CaCO₃), qui se décompose en chaux (oxyde de calcium, CaO) et en dioxyde de carbone (CO₂) gazeux. La chaux solide est le produit de valeur.
Les principales applications de la calcination
Ce processus est une pierre angulaire du traitement des matériaux, en particulier en métallurgie et en fabrication chimique. Son objectif principal est la purification et la préparation.
Extraction des métaux des minerais
La calcination est une première étape cruciale pour le traitement de nombreux minerais, en particulier les carbonates et les hydrates.
Le chauffage d'un minerai de carbonate métallique élimine le dioxyde de carbone, laissant derrière lui un oxyde métallique plus concentré. Cet oxyde métallique est alors beaucoup plus facile à réduire en métal pur final lors d'une étape ultérieure.
Élimination de l'eau chimiquement liée
De nombreux minéraux existent sous forme d'hydrates, ce qui signifie que des molécules d'eau sont incorporées dans leur structure cristalline.
La calcination fournit l'énergie nécessaire pour expulser cette eau liée, convertissant le matériau en sa forme anhydre (sans eau), qui est souvent plus stable et concentrée.
Comprendre les distinctions clés
Pour saisir pleinement l'importance de la calcination, il est essentiel de la distinguer des autres processus thermiques courants. Confondre ces processus peut entraîner des résultats incorrects.
Calcination vs. Grillage
La principale différence est la présence d'air. La calcination se produit avec peu ou pas d'air pour provoquer la décomposition.
Le grillage, en revanche, est effectué avec un excès d'air spécifiquement pour induire une réaction d'oxydation, comme la conversion d'un sulfure métallique en un oxyde métallique.
Calcination vs. Frittage
Ces processus ont des objectifs opposés. La calcination décompose les composés et expulse les impuretés.
Le frittage utilise la chaleur pour fusionner de petites particules en une seule pièce solide sans les faire fondre. C'est un processus de consolidation, pas de purification.
Faire le bon choix pour votre objectif
L'application du processus thermique correct est essentielle pour obtenir les propriétés matérielles souhaitées. Votre objectif déterminera si la calcination est la bonne approche.
- Si votre objectif principal est la purification d'un minerai : La calcination est la méthode idéale pour éliminer les composants volatils comme le CO₂ ou le H₂O des carbonates et hydrates minéraux.
- Si votre objectif principal est la conversion chimique : Utilisez la calcination pour décomposer thermiquement une matière première en un intermédiaire plus réactif ou utile, comme la conversion du calcaire en chaux pour la production de ciment.
- Si votre objectif est de fusionner des particules ou de faire réagir un matériau avec l'air : Vous avez besoin d'un processus entièrement différent, comme le frittage pour la fusion ou le grillage pour l'oxydation.
En fin de compte, la calcination est un outil fondamental pour contrôler la pureté chimique et la réactivité des matériaux inorganiques.
Tableau récapitulatif :
| Aspect clé | Description |
|---|---|
| Objectif principal | Décomposition chimique et purification, pas de fusion. |
| Atmosphère | Air limité ou absent pour prévenir l'oxydation. |
| Intrants clés | Matières premières comme les carbonates métalliques ou les hydrates. |
| Extrants clés | Solides purifiés (par exemple, oxydes métalliques) et gaz volatils expulsés. |
| Applications principales | Extraction des métaux des minerais, production de ciment, élimination de l'eau chimiquement liée. |
Prêt à optimiser votre processus de purification des matériaux ?
La calcination est une étape critique pour obtenir des matériaux de haute pureté en métallurgie et en fabrication chimique. L'équipement adéquat est essentiel pour un contrôle précis de la température et une atmosphère contrôlée afin d'assurer une décomposition réussie sans oxydation.
KINTEK est spécialisé dans les fours de laboratoire à haute température idéaux pour les processus de calcination. Notre équipement robuste et fiable vous aide à :
- Purifier les minerais efficacement pour l'extraction des métaux.
- Décomposer les carbonates et les hydrates avec des résultats constants.
- Atteindre des profils thermiques précis pour une transformation chimique contrôlée.
Discutons de votre application spécifique. Contactez nos experts dès aujourd'hui pour trouver la solution de traitement thermique parfaite pour vos besoins de laboratoire.
Guide Visuel
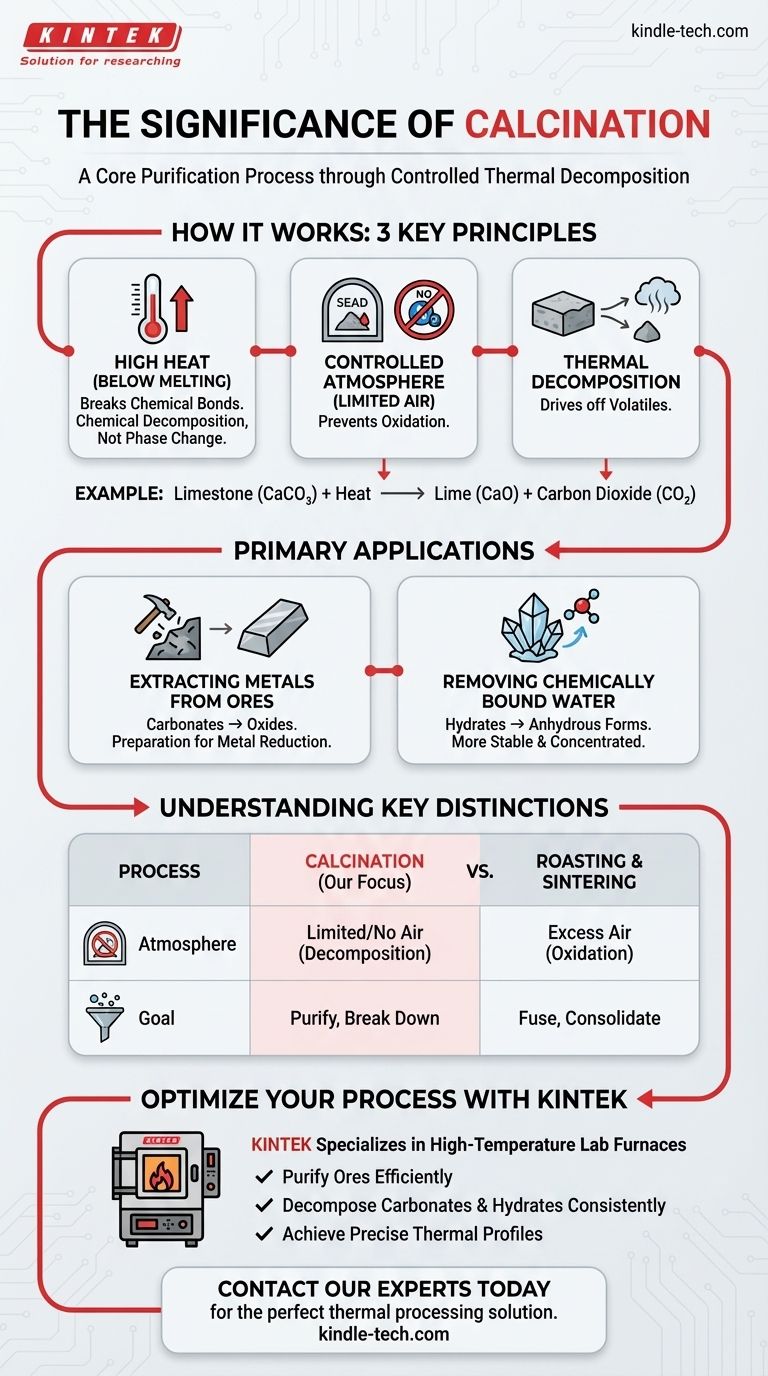
Produits associés
- Fourneuse de pyrolyse de four rotatif électrique Machine calcineuse Petit four rotatif Four rotatif
- Petite usine de pyrolyse continue à four rotatif électrique pour le chauffage
- Four de graphitisation sous vide vertical à haute température
- Four de graphitisation de film de haute conductivité thermique sous vide de graphite
- Four de graphitation sous vide à ultra-haute température au graphite
Les gens demandent aussi
- Quelles sont les caractéristiques des modes de mouvement du lit par glissement, affaissement et roulement ? Optimisez votre processus rotatif
- Qu'est-ce qu'un four électrique rotatif ? Obtenez un chauffage uniforme supérieur pour vos matériaux
- Le four rotatif est-il un four ? Découvrez les différences clés pour le traitement industriel
- Comment les fours rotatifs sont-ils chauffés ? Explication des méthodes de chauffage direct et indirect
- Quels sont les avantages du four rotatif ? Obtenez une uniformité et une efficacité supérieures



















