Oui, le graphite est un conducteur très efficace de l'électricité et de la chaleur. Contrairement à la plupart des non-métaux, la structure atomique unique du graphite lui permet de se comporter comme un métal dans sa capacité à conduire. C'est pourquoi il présente une très faible résistance électrique et une excellente résistance aux chocs thermiques, ce qui en fait un matériau essentiel dans de nombreuses applications haute performance.
La clé pour comprendre le graphite est de reconnaître sa double nature. C'est un non-métal qui conduit exceptionnellement bien l'électricité et la chaleur, mais presque exclusivement le long de ses couches bidimensionnelles, une propriété qui découle directement de son arrangement unique d'atomes de carbone.

La structure atomique unique du graphite
Pour comprendre pourquoi le graphite conduit, nous devons d'abord examiner sa structure fondamentale. C'est un allotrope du carbone, ce qui signifie qu'il est composé des mêmes atomes que le diamant, mais agencés d'une manière profondément différente.
Liaisons fortes au sein des couches
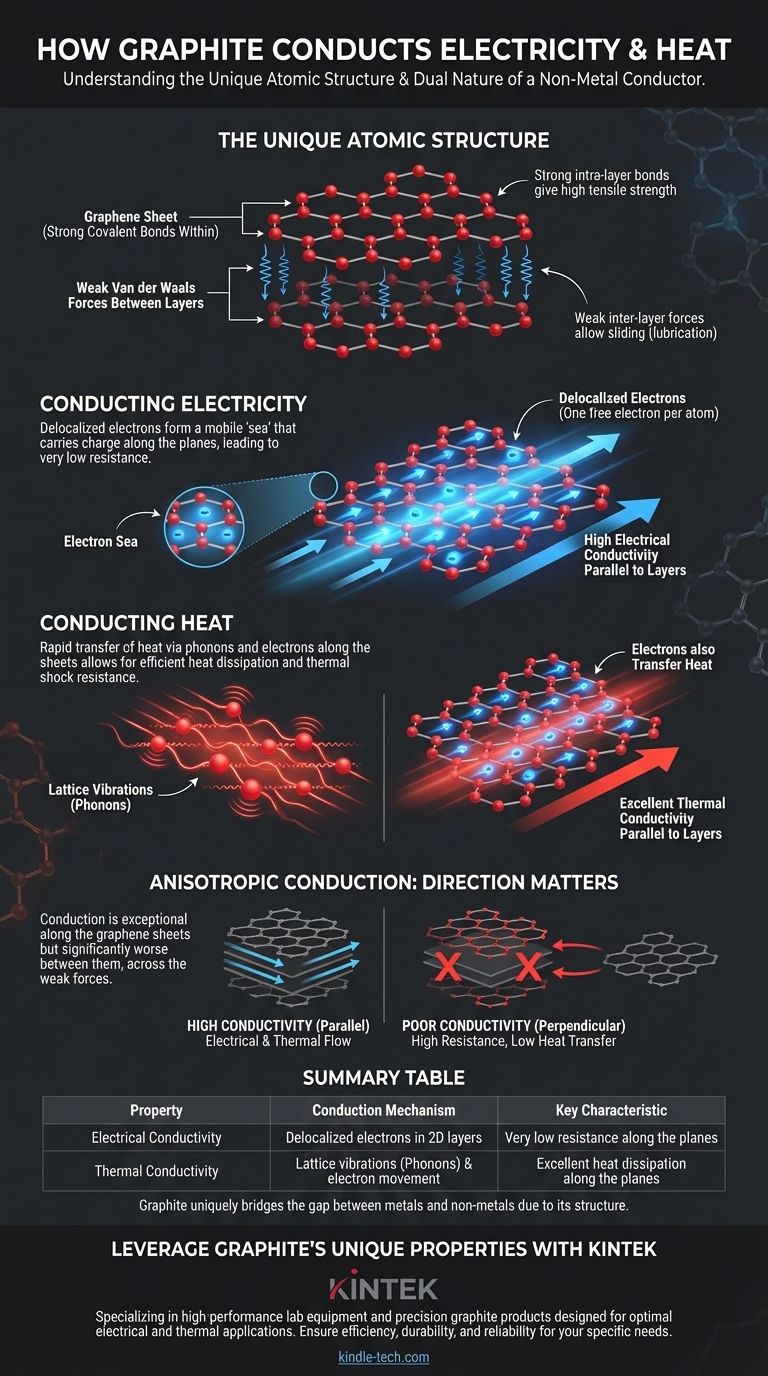
Le graphite est composé d'innombrables couches d'atomes de carbone. Au sein de chaque couche, chaque atome de carbone est lié à trois autres atomes de carbone dans un réseau hexagonal, formant une structure plate en forme de feuille souvent appelée feuille de graphène.
Ces liaisons covalentes sont incroyablement fortes, conférant aux couches individuelles de graphite une immense résistance à la traction et une grande stabilité.
Liaisons faibles entre les couches
Alors que les atomes au sein d'une couche sont fortement liés, les couches elles-mêmes sont maintenues ensemble par des forces beaucoup plus faibles, connues sous le nom de forces de van der Waals.
Ces faibles connexions permettent aux couches de glisser facilement les unes sur les autres, ce qui confère au graphite sa douceur et ses propriétés lubrifiantes caractéristiques.
Comment le graphite conduit l'électricité
La capacité du graphite à conduire l'électricité est le résultat direct de sa structure de liaison au sein des couches de carbone.
Le rôle des électrons délocalisés
Chaque atome de carbone possède quatre électrons externes disponibles pour la liaison. Dans le graphite, seuls trois de ces électrons sont utilisés pour former les fortes liaisons covalentes avec les atomes voisins dans la feuille hexagonale.
Cela laisse un électron par atome – le quatrième – non lié. Cet électron devient délocalisé, ce qui signifie qu'il est libre de se déplacer n'importe où au sein de sa couche bidimensionnelle.
Une "mer d'électrons" en deux dimensions
Ces électrons libres forment une "mer" mobile de charges. Lorsqu'une tension est appliquée, ces électrons délocalisés peuvent circuler facilement le long des couches, créant un puissant courant électrique.
Ce mécanisme explique pourquoi le graphite a une si faible résistance électrique, une propriété mentionnée dans les matériaux haute performance comme le graphite isostatique.
Comment le graphite conduit la chaleur
Les mêmes caractéristiques structurelles qui permettent la conductivité électrique font également du graphite un excellent conducteur thermique.
Vibrations du réseau (phonons)
L'énergie thermique est principalement transférée à travers un matériau via les vibrations de son réseau atomique. Les fortes liaisons covalentes au sein des couches de graphite permettent à ces vibrations, appelées phonons, de se propager très rapidement et efficacement à travers la feuille.
Ce transfert rapide d'énergie vibratoire entraîne une conductivité thermique élevée.
Le double rôle des électrons
En plus des vibrations du réseau, les mêmes électrons délocalisés qui transportent la charge électrique transportent et transfèrent également l'énergie thermique. Ce rôle à double usage améliore encore la capacité du graphite à dissiper la chaleur.
Comprendre les compromis : la conduction anisotrope
Un concept essentiel pour toute application pratique est que la conductivité du graphite est anisotrope, ce qui signifie qu'elle n'est pas la même dans toutes les directions.
Conduction élevée le long des couches
L'électricité et la chaleur se propagent avec une facilité exceptionnelle parallèlement aux feuilles de graphène. C'est le chemin de moindre résistance, où les électrons délocalisés et les vibrations du réseau peuvent se déplacer librement.
Faible conduction entre les couches
En revanche, la conduction perpendiculairement aux couches est significativement moins bonne. Les électrons et les vibrations doivent "sauter" à travers les faibles espaces de van der Waals entre les feuilles, un processus beaucoup moins efficace. Cela entraîne une résistance beaucoup plus élevée et une conductivité thermique plus faible dans cette direction.
Faire le bon choix pour votre objectif
Comprendre la conductivité directionnelle du graphite est essentiel pour l'utiliser efficacement.
- Si votre objectif principal est les applications électriques (comme les électrodes ou les anodes de batterie) : Vous devez orienter le matériau de manière à ce que le courant électrique circule le long des couches de graphite pour une efficacité maximale.
- Si votre objectif principal est la gestion thermique (comme les diffuseurs de chaleur ou les dissipateurs) : Le graphite doit être positionné pour évacuer la chaleur d'une source le long de ses plans hautement conducteurs.
- Si votre objectif principal est la stabilité à haute température (comme dans les fours) : Sa capacité à résister aux chocs thermiques est liée à sa capacité à dissiper efficacement les gradients de chaleur le long de ses couches, évitant ainsi l'accumulation de contraintes.
La structure unique du graphite en fait un matériau remarquable qui comble de manière unique le fossé entre les métaux et les non-métaux.
Tableau récapitulatif :
| Propriété | Mécanisme de conduction | Caractéristique clé |
|---|---|---|
| Conductivité électrique | Électrons délocalisés se déplaçant dans des couches 2D | Très faible résistance le long des plans |
| Conductivité thermique | Vibrations du réseau (phonons) et mouvement des électrons | Excellente dissipation thermique le long des plans |
| Nature anisotrope | Conduction dépendante de la direction | Haute conductivité parallèle aux couches ; Faible perpendiculairement aux couches |
Exploitez les propriétés uniques du graphite dans votre laboratoire
Comprendre la conductivité anisotrope du graphite est crucial pour maximiser les performances dans des applications telles que les composants de fours, les systèmes de gestion thermique et les électrodes.
KINTEK est spécialisé dans les équipements et consommables de laboratoire haute performance, y compris les produits en graphite de précision conçus pour des performances thermiques et électriques optimales. Nos experts peuvent vous aider à sélectionner le bon matériau et la bonne orientation pour vos besoins spécifiques en laboratoire, garantissant efficacité, durabilité et fiabilité.
Prêt à améliorer votre application avec la bonne solution de graphite ? Contactez notre équipe dès aujourd'hui pour une consultation et découvrez comment KINTEK peut soutenir le succès de votre laboratoire.
Guide Visuel
Produits associés
- Four de graphitisation de film de haute conductivité thermique sous vide de graphite
- Électrode électrochimique en graphite, tige et plaque de graphite
- Four de graphitation sous vide à ultra-haute température au graphite
- Creuset en graphite pur de haute pureté pour l'évaporation
- Plaque de graphite carboné fabriquée par la méthode de pressage isostatique
Les gens demandent aussi
- Quels sont les inconvénients du four à graphite ? Limitations clés et coûts opérationnels
- Quelle est la plage de température d'un four à graphite ? Atteignez jusqu'à 3000°C pour le traitement des matériaux avancés.
- Quel est l'inconvénient du four à graphite ? Gérer la réactivité et les risques de contamination
- Quelle est la température d'un four à graphite ? Atteignez une chaleur extrême jusqu'à 3000°C
- Que fait un four à graphite ? Atteindre une chaleur extrême et une analyse ultra-sensible












