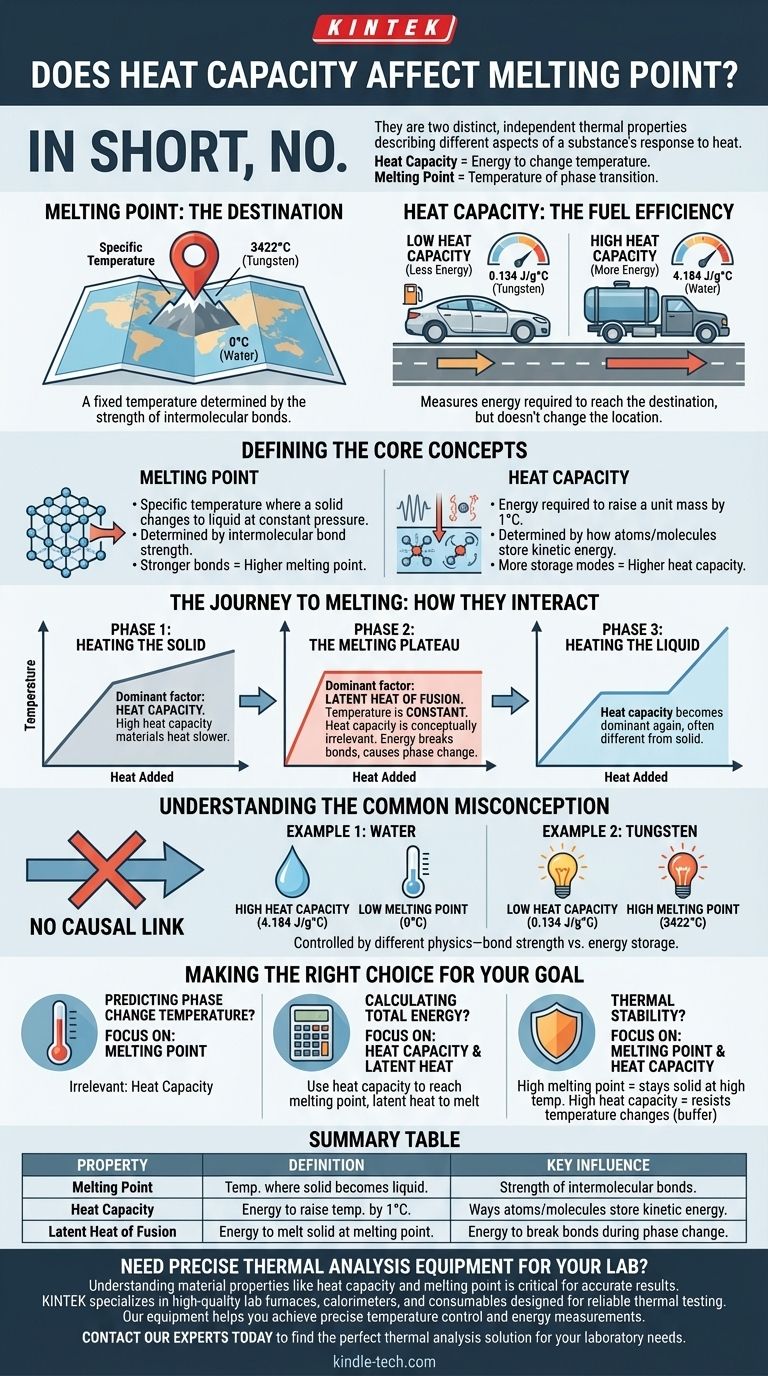
En bref, non. La capacité thermique n'affecte pas ou ne détermine pas directement le point de fusion d'un matériau. Ce sont deux propriétés thermiques distinctes et indépendantes qui décrivent différents aspects de la réponse d'une substance à la chaleur. La capacité thermique mesure l'énergie requise pour modifier la température d'un matériau, tandis que le point de fusion est la température spécifique à laquelle il passe de l'état solide à l'état liquide.
Considérez le point de fusion d'un matériau comme une destination fixe sur une carte (une température spécifique). La capacité thermique, en revanche, est comme l'efficacité énergétique de la voiture que vous utilisez pour vous y rendre. Une voiture avec une faible efficacité énergétique (capacité thermique élevée) nécessite plus de carburant (énergie) pour atteindre la destination, mais l'emplacement de la destination elle-même ne change pas.

Définition des concepts fondamentaux
Pour comprendre pourquoi ces propriétés sont distinctes, nous devons d'abord les définir clairement. Elles décrivent différents phénomènes physiques au niveau moléculaire.
Qu'est-ce que le point de fusion ?
Le point de fusion est la température spécifique à laquelle un solide cristallin pur, à pression constante, se transforme en liquide.
Cette température est déterminée par la force des liaisons intermoléculaires qui maintiennent les atomes ou les molécules ensemble dans un réseau cristallin fixe.
Pour faire fondre une substance, il faut fournir suffisamment d'énergie pour surmonter ces forces. Par conséquent, les matériaux avec des liaisons plus fortes nécessitent plus d'énergie et ont un point de fusion plus élevé.
Qu'est-ce que la capacité thermique ?
La capacité thermique spécifique est la quantité d'énergie thermique requise pour élever la température d'une unité de masse d'une substance d'un degré (par exemple, un Kelvin ou un Celsius).
Cette propriété est déterminée par le nombre de façons dont les atomes et les molécules d'un matériau peuvent stocker l'énergie cinétique. Cela inclut les vibrations, les rotations et les translations.
Une substance ayant une capacité thermique élevée peut absorber une grande quantité d'énergie thermique avec seulement une faible augmentation de sa température.
Le chemin vers la fusion : comment ils interagissent
Bien qu'elles soient des propriétés indépendantes, la capacité thermique et le point de fusion jouent tous deux des rôles séquentiels dans le processus de fusion d'une substance. Le processus se déroule en phases distinctes.
Phase 1 : Chauffage du solide
C'est la phase où la capacité thermique est le facteur dominant. Lorsque vous ajoutez de l'énergie thermique à un solide, sa température augmente.
Un matériau avec une capacité thermique élevée chauffera plus lentement qu'un matériau avec une faible capacité thermique, en supposant le même taux d'apport d'énergie. Il "absorbe" plus d'énergie pour chaque degré d'augmentation de température.
Phase 2 : Le plateau de fusion
Une fois que le matériau atteint son point de fusion, quelque chose de crucial se produit : sa température cesse d'augmenter, même si vous continuez à ajouter de la chaleur.
Toute l'énergie ajoutée est maintenant utilisée exclusivement pour rompre les liaisons de la structure solide, un processus régi par une autre propriété appelée la chaleur latente de fusion.
Pendant ce changement de phase, la capacité thermique est conceptuellement non pertinente car la température est statique. L'énergie provoque un changement d'état, pas un changement de température.
Phase 3 : Chauffage du liquide
Une fois que tout le solide s'est transformé en liquide, la température de la substance recommencera à augmenter à mesure que plus de chaleur est ajoutée.
La phase liquide de la substance a sa propre capacité thermique distincte, qui est souvent différente de la capacité thermique de sa forme solide.
Comprendre l'idée fausse courante
La confusion entre ces deux propriétés découle souvent du fait qu'elles sont toutes deux fondamentales pour le comportement thermique d'un matériau. Cependant, confondre leur corrélation avec la causalité est une erreur critique.
Le piège de la corrélation vs la causalité
Il n'y a aucun lien de causalité fiable entre la capacité thermique et le point de fusion. Une capacité thermique élevée n'implique pas un point de fusion élevé, et vice versa.
Considérez ces exemples :
- L'eau a une capacité thermique spécifique très élevée (4,184 J/g°C) mais un point de fusion bas de 0°C.
- Le tungstène a une capacité thermique spécifique beaucoup plus faible (0,134 J/g°C) mais l'un des points de fusion les plus élevés de tous les éléments, à 3 422°C.
Cela démontre qu'une propriété ne peut pas être utilisée pour prédire l'autre. Elles sont contrôlées par des physiques sous-jacentes différentes – la force de liaison pour le point de fusion et les modes de stockage d'énergie pour la capacité thermique.
Faire le bon choix pour votre objectif
Lors de l'analyse des propriétés thermiques d'un matériau, concentrez-vous sur la propriété qui répond directement à votre question.
- Si votre objectif principal est de prédire la température d'un changement de phase : Ne regardez que le point de fusion. La capacité thermique est sans importance quant à la température à laquelle il fondra.
- Si votre objectif principal est de calculer les besoins énergétiques totaux : Vous devez utiliser la capacité thermique pour trouver l'énergie nécessaire pour atteindre le point de fusion, puis la chaleur latente de fusion pour trouver l'énergie nécessaire pour achever la fusion.
- Si votre objectif principal est la stabilité thermique : Un point de fusion élevé signifie qu'un matériau reste solide à des températures élevées. Une capacité thermique élevée signifie que le matériau résiste aux changements de température, ce qui en fait un bon tampon thermique.
Comprendre les rôles distincts de la capacité thermique et du point de fusion est la clé pour prédire et concevoir avec précision le comportement des matériaux sous contrainte thermique.
Tableau récapitulatif :
| Propriété | Définition | Influence clé |
|---|---|---|
| Point de fusion | La température spécifique à laquelle un solide devient liquide. | Force des liaisons intermoléculaires. |
| Capacité thermique | L'énergie nécessaire pour élever la température d'un matériau de 1°C. | Façons dont les atomes/molécules stockent l'énergie cinétique. |
| Chaleur latente de fusion | L'énergie requise pour faire fondre un solide à son point de fusion. | Énergie pour rompre les liaisons pendant le changement de phase. |
Besoin d'équipement d'analyse thermique précis pour votre laboratoire ? Comprendre les propriétés des matériaux comme la capacité thermique et le point de fusion est essentiel pour des résultats précis. KINTEK est spécialisé dans les fours de laboratoire, les calorimètres et les consommables de haute qualité conçus pour des tests thermiques fiables. Notre équipement vous aide à obtenir un contrôle précis de la température et des mesures d'énergie, garantissant que votre recherche et votre contrôle qualité sont basés sur des données solides. Contactez nos experts dès aujourd'hui pour trouver la solution d'analyse thermique parfaite pour les besoins de votre laboratoire.
Guide Visuel