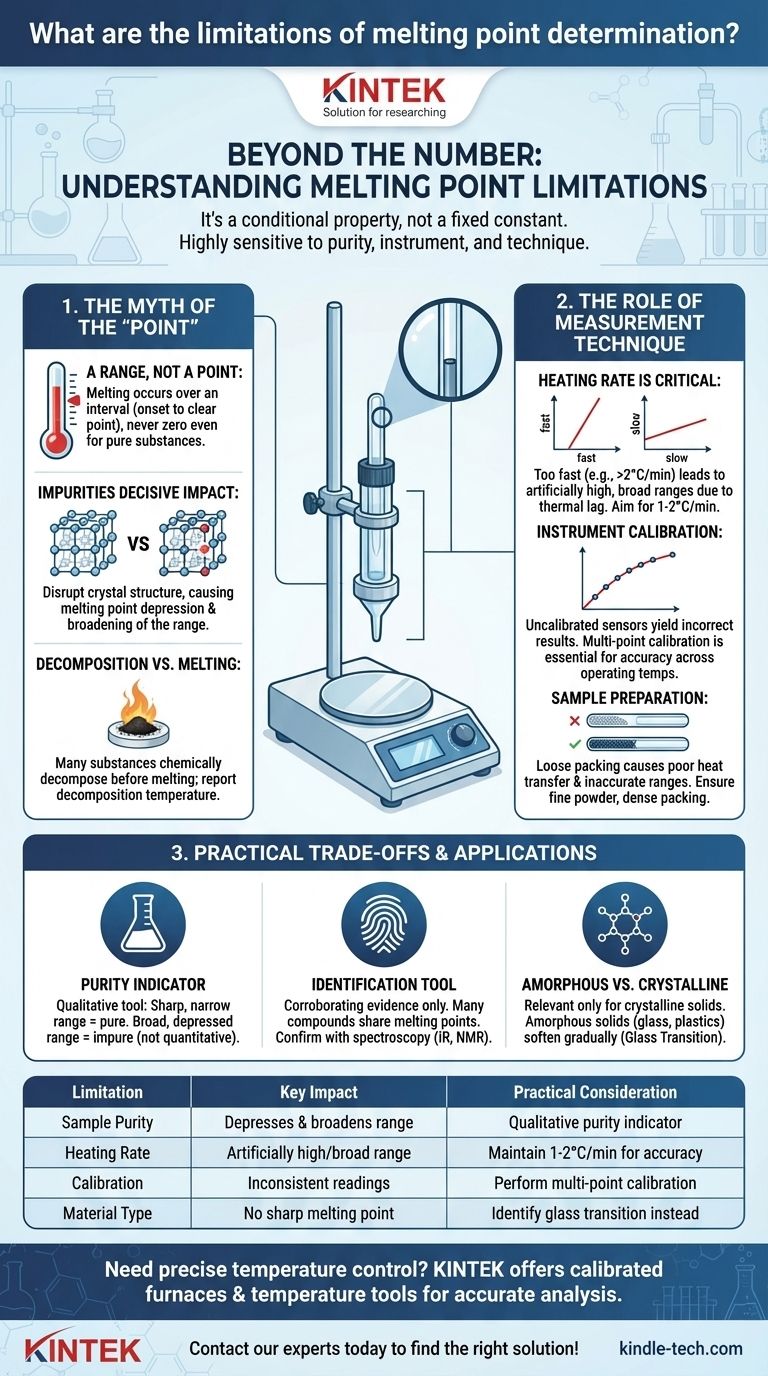
Au-delà d'un simple chiffre sur une fiche technique, le point de fusion d'une substance présente plusieurs limitations critiques que vous devez comprendre. Sa valeur n'est pas une constante absolue mais est très sensible à la pureté de l'échantillon, à la précision de l'instrument de mesure et à la technique spécifique utilisée pendant la mesure. De plus, certains matériaux ne présentent pas de point de fusion net et clair, mais se décomposent ou ramollissent sur une large plage de températures.
La principale limitation de la détermination du point de fusion est qu'il ne s'agit pas d'une propriété intrinsèque et fixe, mais plutôt d'une propriété conditionnelle. Le considérer comme un identifiant définitif sans tenir compte de la pureté de l'échantillon et du contexte de mesure peut entraîner des erreurs significatives dans l'analyse des matériaux et le contrôle des processus.
Le mythe du "point de fusion"
Le terme lui-même suggère une température unique et discrète, ce qui est la première idée fausse à aborder. En pratique, la fusion est un processus qui se produit sur un intervalle de température.
C'est une plage, pas un point
Même pour une substance très pure, la fusion ne se produit pas instantanément. Elle commence à une température (début) et se termine à une autre (point clair). Pour les composés cristallins très purs, cette plage de fusion peut être très étroite (moins de 1-2°C), mais elle n'est jamais nulle.
L'impact décisif des impuretés
C'est la limitation la plus courante et la plus significative. Les impuretés perturbent le réseau cristallin d'une substance, ce qui entraîne presque toujours deux effets : une dépression du point de fusion et un élargissement de la plage de fusion. Une petite quantité de contaminant peut provoquer une chute notable et un processus de fusion large et indistinct.
Lorsque les substances se décomposent, au lieu de fondre
De nombreux composés organiques et polymères n'ont pas de véritable point de fusion. Lorsque vous les chauffez, ils se décomposent chimiquement ou se carbonisent avant de pouvoir passer à l'état liquide. Dans ces cas, une "température de décomposition" est rapportée, qui est souvent variable et dépend du taux de chauffage.
Le rôle de la technique de mesure
La manière dont vous effectuez la mesure est tout aussi importante que la substance elle-même. Une technique incohérente est une source majeure de données peu fiables.
Le taux de chauffage est critique
Si l'échantillon est chauffé trop rapidement, la température du bloc chauffant ou du bain augmentera plus vite que la température de l'échantillon ne peut s'équilibrer. Ce décalage entraîne une plage de fusion observée artificiellement élevée et souvent plus large qu'elle ne devrait l'être. Un taux de chauffage lent et contrôlé (par exemple, 1-2°C par minute) est essentiel pour la précision.
Étalonnage et précision de l'instrument
Le thermomètre ou le capteur utilisé pour mesurer la température doit être étalonné avec précision. Un instrument non étalonné peut produire des résultats constamment incorrects, rendant les données inutilisables pour autre chose que des comparaisons relatives.
Comme on le voit dans les applications industrielles comme les fours céramiques, un étalonnage en un seul point (par exemple, en utilisant de l'argent) peut être insuffisant. Pour les processus nécessitant une précision sur un large spectre, un étalonnage multipoint est nécessaire pour garantir la fiabilité de l'instrument à la fois à basse et à haute température de fonctionnement.
Préparation et emballage de l'échantillon
La manière dont un échantillon solide est emballé dans un tube capillaire peut affecter le résultat. Un échantillon mal tassé aura un mauvais transfert de chaleur, ce qui entraînera une plage de fusion imprécise et large. L'échantillon doit être finement pulvérisé et densément tassé pour assurer un chauffage uniforme.
Comprendre les compromis
Connaître ces limitations vous permet d'utiliser efficacement les données de point de fusion tout en évitant les interprétations erronées courantes.
Comme indicateur de pureté
Le point de fusion est un excellent indicateur qualitatif de pureté. Une plage de fusion nette et étroite qui correspond à la valeur de la littérature suggère un composé pur. Inversement, une plage large et déprimée est un signe fort d'impureté. Cependant, c'est un mauvais outil quantitatif ; vous ne pouvez pas déterminer avec précision le pourcentage d'impureté à partir de la seule plage de fusion.
Comme outil d'identification
Un point de fusion mesuré peut aider à confirmer l'identité d'un composé connu ou à réduire les possibilités pour un composé inconnu. Cependant, ce n'est pas une confirmation définitive. De nombreux composés différents ont des points de fusion similaires ou identiques. Par conséquent, il doit toujours être utilisé comme preuve corroborante aux côtés d'autres techniques analytiques comme la spectroscopie (IR, RMN) ou la chromatographie.
Solides amorphes vs. cristallins
Le point de fusion n'est pertinent que pour les solides cristallins, qui ont une structure atomique ordonnée à longue portée. Les solides amorphes, comme le verre et de nombreux plastiques, n'ont pas cette structure. Ils n'ont pas de point de fusion net mais ramollissent progressivement sur une large plage de températures, un phénomène connu sous le nom de transition vitreuse.
Comment appliquer cela à votre analyse
Votre interprétation des données de point de fusion doit dépendre entièrement de votre objectif.
- Si votre objectif principal est d'évaluer la pureté : Examinez l'étendue de la plage de fusion. Une plage étroite (par exemple, <2°C) est votre indicateur clé de haute pureté.
- Si votre objectif principal est l'identification de composés : Utilisez le point de fusion comme une preuve à confirmer avec des méthodes analytiques plus spécifiques.
- Si votre objectif principal est le contrôle de processus : Priorisez un étalonnage multipoint rigoureux et régulier de l'instrument sur toute votre plage de température de fonctionnement pertinente.
En fin de compte, traiter le point de fusion comme une plage diagnostique plutôt que comme un nombre unique et absolu libère sa véritable puissance analytique.

Tableau récapitulatif :
| Limitation | Impact clé | Considération pratique |
|---|---|---|
| Pureté de l'échantillon | Déprime et élargit la plage de fusion | Utiliser comme indicateur qualitatif de pureté |
| Taux de chauffage | Plage artificiellement élevée/large | Maintenir 1-2°C/min pour la précision |
| Étalonnage de l'instrument | Lectures de température incohérentes | Effectuer un étalonnage multipoint |
| Type de matériau (ex. amorphe) | Pas de point de fusion net | Identifier la transition vitreuse à la place |
Besoin d'un contrôle précis de la température pour vos analyses de laboratoire ? Chez KINTEK, nous comprenons qu'une détermination précise du point de fusion est essentielle pour évaluer la pureté et assurer la fiabilité des processus. Notre équipement de laboratoire de haute qualité, y compris les fours étalonnés et les outils de mesure de température, est conçu pour offrir la cohérence et la précision que votre laboratoire exige. Ne laissez pas les limitations de mesure compromettre vos résultats—contactez nos experts dès aujourd'hui pour trouver la solution adaptée à vos besoins spécifiques !
Guide Visuel
Produits associés
- Sonde de détermination de l'hydrogène pour mesurer rapidement la teneur en hydrogène avec un taux de réussite élevé
- Sonde à lance mobile pour la mesure de la température, de la teneur en carbone et en oxygène de l'acier en fusion et le prélèvement d'échantillons d'acier
- Four de Fusion par Induction sous Vide à l'Échelle du Laboratoire
- Four de fusion par induction à arc sous vide
- Potentiostat de poste de travail électrochimique de laboratoire pour une utilisation en laboratoire
Les gens demandent aussi
- À quelle température l'acier se liquéfie-t-il ? Comprendre la plage de fusion pour vos applications
- Quelle chose est déterminée dans la teneur en cendres ? Mesurer les matières inorganiques pour le contrôle qualité
- Pourquoi un four à induction à haute fréquence est-il préféré à un four à résistance ? Optimiser la recherche sur la solubilité de l'hydrogène
- Pourquoi déterminons-nous la teneur en cendres du charbon ? Découvrez sa véritable valeur énergétique et évitez des temps d'arrêt coûteux.
- Quel rôle le gaz d'hydrogène à haute pression joue-t-il dans la production d'acide formique ? Perspectives d'experts sur la synthèse hydrothermale








