Dans de nombreuses applications industrielles courantes, oui. La calcination est un processus de chauffage, et lorsqu'elle est appliquée à des matériaux contenant des carbonates comme le calcaire, elle provoque une décomposition chimique qui libère des quantités importantes de dioxyde de carbone (CO2). La production de chaux à partir de calcaire est un exemple principal de cette réaction.
Le point essentiel à comprendre est que la calcination est un processus, et non une réaction spécifique unique. La production de CO2 dépend entièrement de la composition chimique du matériau chauffé.

Qu'est-ce que la calcination fondamentalement ?
Un processus de décomposition thermique
La calcination est un processus de traitement thermique où un matériau solide est chauffé à une température élevée, mais en dessous de son point de fusion. Cela se fait en l'absence ou avec un apport très limité d'air.
L'objectif principal est d'induire une décomposition thermique, ce qui signifie décomposer le composé à l'aide de la chaleur.
L'objectif : induire un changement
L'objectif de la calcination n'est pas toujours le même. Elle peut être utilisée pour :
- Éliminer une substance volatile, comme le CO2 du calcaire ou l'eau d'un minéral hydraté.
- Éliminer les impuretés d'un minerai.
- Provoquer une transition de phase, modifiant la structure cristalline et les propriétés du matériau.
Le rôle de l'atmosphère
L'atmosphère contrôlée (air limité) est cruciale. Elle empêche le matériau de brûler ou de s'oxyder, distinguant la calcination d'autres traitements thermiques comme le grillage.
Quand la calcination produit-elle du CO2 ?
La connexion avec les carbonates
La calcination produit du dioxyde de carbone lorsque la matière première est un carbonate. Les carbonates sont des minéraux qui contiennent l'ion carbonate (CO3²⁻).
Lorsqu'ils sont chauffés, ces minéraux se décomposent, brisant leurs liaisons chimiques et libérant les atomes de carbone et d'oxygène sous forme de gaz CO2.
Exemple : production de chaux à partir de calcaire
L'exemple le plus classique est la calcination du calcaire (carbonate de calcium, CaCO₃).
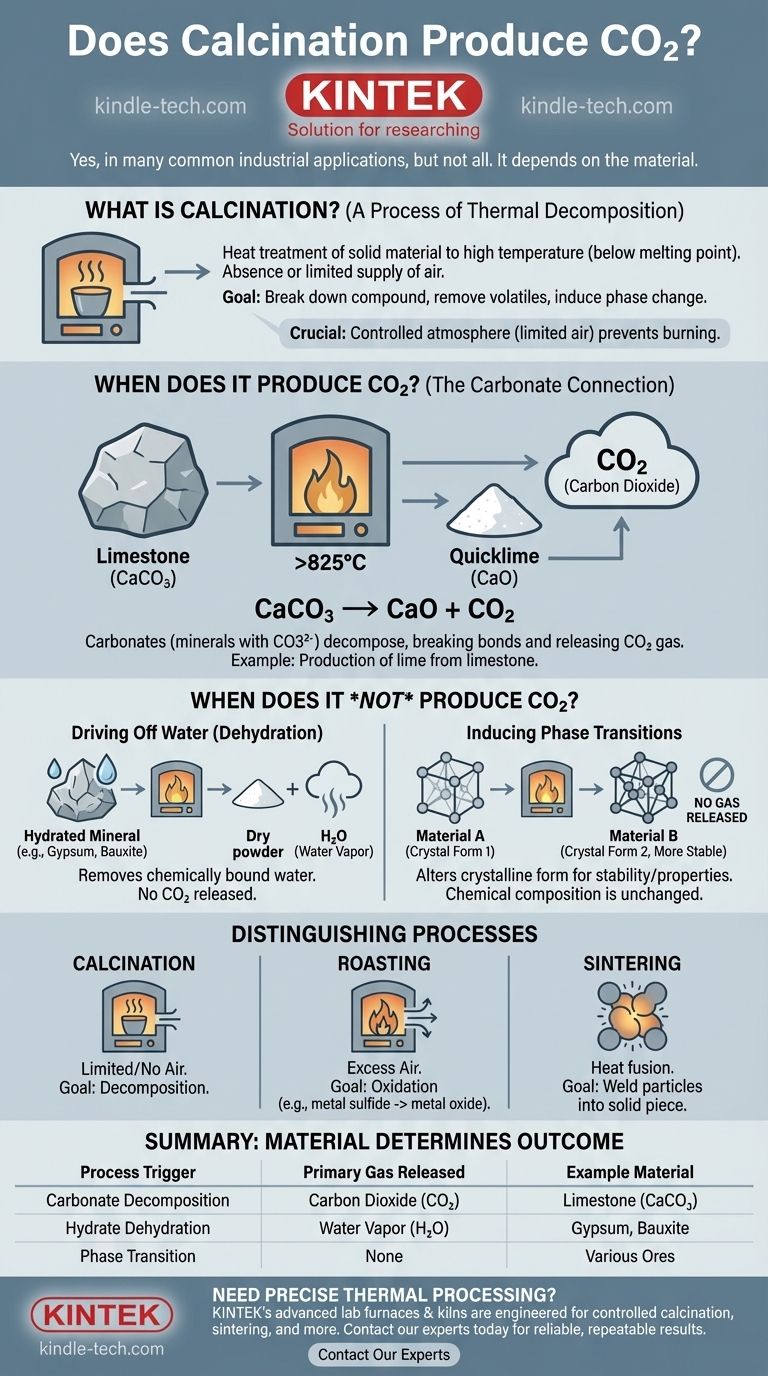
Lorsqu'il est chauffé à plus de 825°C (1517°F), il se décompose en oxyde de calcium (CaO), également connu sous le nom de chaux vive, et libère du dioxyde de carbone. La réaction chimique est : CaCO₃ → CaO + CO₂.
Autres minerais carbonatés
Ce principe s'applique également à d'autres minerais carbonatés, tels que la magnésite (MgCO₃) ou la dolomite (CaMg(CO₃)₂), qui libèrent également du CO2 lors du chauffage.
Quand la calcination ne produit-elle pas de CO2 ?
Élimination de l'eau (déshydratation)
De nombreux minéraux sont calcinés simplement pour éliminer l'eau (H₂O) qui est chimiquement liée à leur structure cristalline.
Par exemple, la calcination du minerai de bauxite pour produire de l'alumine (oxyde d'aluminium) ou le chauffage du gypse pour produire du plâtre de Paris libèrent tous deux de la vapeur d'eau, et non du dioxyde de carbone.
Induction de transitions de phase
Parfois, un matériau est calciné simplement pour modifier sa forme cristalline. Cela peut le rendre plus stable, plus réactif ou lui conférer des propriétés physiques différentes.
Dans ces cas, la composition chimique ne change pas et aucun gaz n'est libéré.
Distinguer la calcination des processus similaires
Calcination vs. Grillage
Le grillage consiste à chauffer un minerai en présence d'un excès d'air. Son objectif est généralement l'oxydation, comme la conversion d'un sulfure métallique en un oxyde métallique. La calcination se produit avec peu ou pas d'air pour provoquer la décomposition.
Calcination vs. Frittage
Le frittage utilise la chaleur pour fusionner de petites particules en une seule pièce solide, souvent après que les impuretés ont déjà été éliminées. La calcination décompose un matériau ; le frittage le soude.
Faire le bon choix pour votre objectif
Comprendre le matériau de départ est la clé pour prédire le résultat.
- Si votre matériau est un carbonate (comme le calcaire ou la dolomite) : Attendez-vous à une production significative de CO2 comme résultat principal du processus.
- Si votre matériau est un hydrate (comme la bauxite ou le gypse) : L'émission principale sera de la vapeur d'eau (vapeur), pas du CO2.
- Si votre objectif est de modifier la structure cristalline d'un matériau : Le processus peut ne libérer aucun gaz.
En fin de compte, la calcination est un outil polyvalent défini par la chaleur et une atmosphère contrôlée, tandis que ses résultats spécifiques sont dictés par la chimie.
Tableau récapitulatif :
| Déclencheur du processus | Gaz primaire libéré | Exemple de matériau |
|---|---|---|
| Décomposition des carbonates | Dioxyde de carbone (CO₂) | Calcaire (CaCO₃) |
| Déshydratation des hydrates | Vapeur d'eau (H₂O) | Gypse, Bauxite |
| Transition de phase | Aucun | Divers minerais |
Besoin d'un traitement thermique précis pour vos matériaux ? Les fours et fours de laboratoire avancés de KINTEK sont conçus pour la calcination, le frittage et bien plus encore. Que vous traitiez des carbonates, des hydrates ou d'autres matériaux, notre équipement assure un contrôle précis de la température et de l'atmosphère pour des résultats fiables et reproductibles. Contactez nos experts dès aujourd'hui pour trouver la solution thermique parfaite pour les besoins spécifiques de votre laboratoire.
Guide Visuel
Produits associés
- Fourneuse de pyrolyse de four rotatif électrique Machine calcineuse Petit four rotatif Four rotatif
- Petite usine de pyrolyse continue à four rotatif électrique pour le chauffage
- Four de graphitisation sous vide vertical à haute température
- Four de graphitisation de film de haute conductivité thermique sous vide de graphite
- Four de graphitation sous vide à ultra-haute température au graphite
Les gens demandent aussi
- Quelles sont les caractéristiques des modes de mouvement du lit par glissement, affaissement et roulement ? Optimisez votre processus rotatif
- Quelle est la température d'un four rotatif ? Cela dépend de votre matériau et de votre objectif de processus
- Le four rotatif est-il un four ? Découvrez les différences clés pour le traitement industriel
- Quels sont les principes d'un four rotatif ? Maîtriser la mécanique du traitement à haute température
- Quels sont les avantages du four rotatif ? Obtenez une uniformité et une efficacité supérieures



















