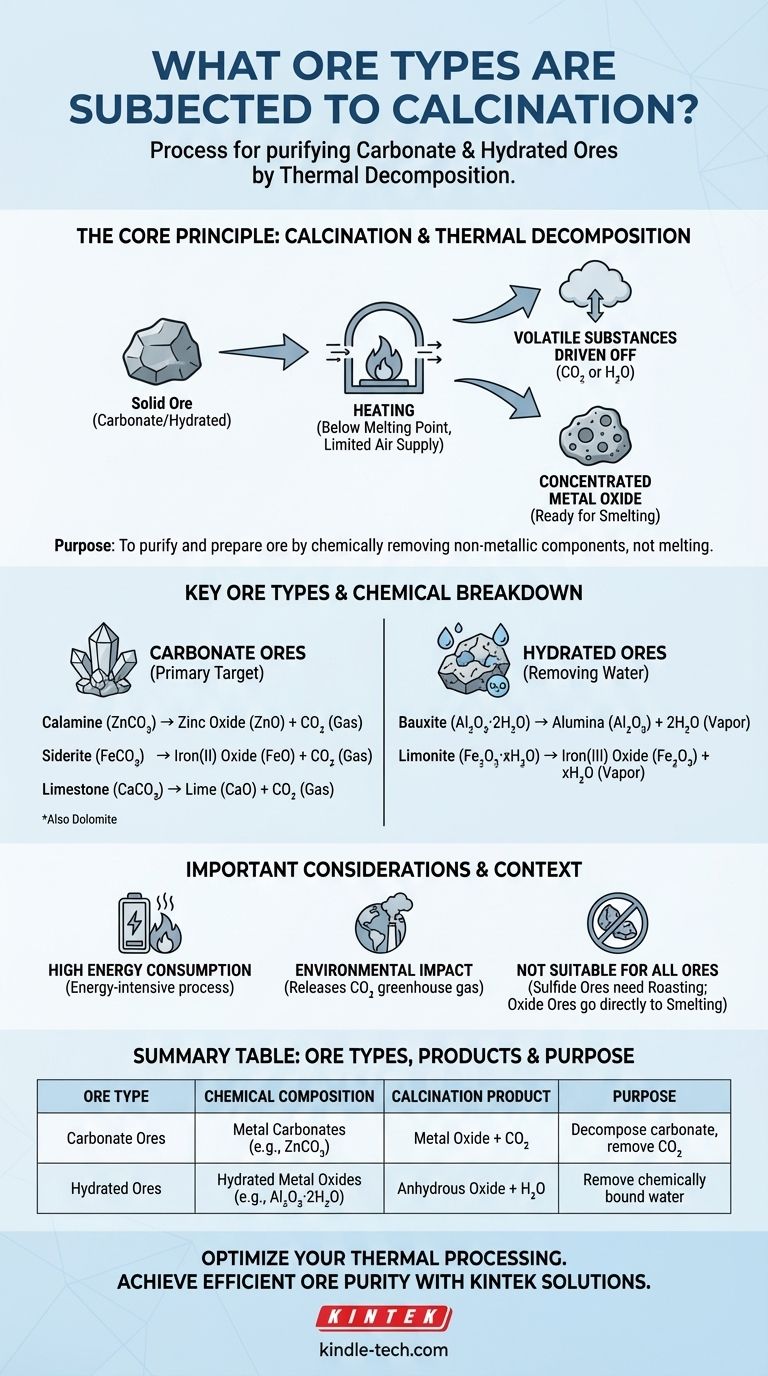
En bref, la calcination est un processus principalement appliqué aux minerais carbonatés et hydratés. Ce processus de chauffage métallurgique est spécifiquement conçu pour décomposer thermiquement le minerai, en chassant les substances volatiles telles que le dioxyde de carbone (CO2) des carbonates ou l'eau (H2O) des minéraux hydratés afin de produire un oxyde métallique concentré.
L'objectif central de la calcination n'est pas de faire fondre le minerai, mais de le purifier et de le préparer pour la fusion. En chauffant le minerai en dessous de son point de fusion, on élimine chimiquement les composants non métalliques, ce qui rend l'extraction ultérieure du métal final plus efficace et économique.

Le principe fondamental de la calcination : la décomposition thermique
La calcination est une étape de traitement thermique très spécifique en métallurgie extractive. Comprendre son objectif chimique principal est essentiel pour savoir quels minerais conviennent à ce processus.
Qu'est-ce que la calcination ?
La calcination est le processus de chauffage d'un matériau solide, tel qu'un minerai, à une température élevée en l'absence ou en présence d'une quantité limitée d'air. Cette atmosphère contrôlée est essentielle.
La température est maintenue suffisamment élevée pour provoquer une décomposition chimique (décomposition thermique) mais reste en dessous du point de fusion du minerai.
L'objectif chimique : éliminer les substances volatiles
L'objectif principal est d'éliminer les substances volatiles qui sont chimiquement liées à la structure du minerai. Cela purifie le minerai en augmentant la concentration de l'oxyde métallique désiré.
Ce processus rend le minerai plus poreux, ce qui améliore sa réactivité pour l'étape suivante d'extraction du métal, qui est généralement la réduction (fusion).
Pourquoi une alimentation limitée en air est-elle cruciale ?
L'alimentation limitée en air distingue la calcination d'un processus similaire appelé grillage. Le grillage est effectué avec un excès d'air pour provoquer intentionnellement une oxydation, ce qui est nécessaire pour les minerais sulfurés.
La calcination évite spécifiquement l'oxydation et se concentre uniquement sur la décomposition.
Types de minerais clés nécessitant une calcination
Les minerais soumis à la calcination sont définis par leur composition chimique, en particulier la présence de composants qui peuvent être éliminés par la chaleur.
Minerais carbonatés (La cible principale)
Ce sont les candidats les plus courants à la calcination. Le processus décompose le carbonate métallique en un oxyde métallique et en dioxyde de carbone gazeux.
- Calamine (Carbonate de zinc, ZnCO₃) → Oxyde de zinc (ZnO) + CO₂
- Sidérite (Carbonate de fer(II), FeCO₃) → Oxyde de fer(II) (FeO) + CO₂
- Calcaire (Carbonate de calcium, CaCO₃) → Chaux (CaO) + CO₂
- Dolomite (Carbonate de calcium et de magnésium, CaMg(CO₃)₂)
Minerais hydratés (Élimination de l'eau)
Pour ces minerais, le but de la calcination est d'éliminer les molécules d'eau qui sont chimiquement intégrées dans la structure cristalline du minéral.
- Bauxite (Oxyde d'aluminium hydraté, Al₂O₃·2H₂O) → Alumine (Al₂O₃) + 2H₂O
- Limonite (Oxyde de fer(III) hydraté, Fe₂O₃·xH₂O) → Oxyde de fer(III) (Fe₂O₃) + xH₂O
Comprendre les limites et le contexte
Bien qu'essentielle pour certains minerais, la calcination n'est pas une solution universelle. Son application est très spécifique et comporte des considérations importantes.
Consommation d'énergie
Le chauffage de quantités massives de minerai à haute température est un processus énergivore. Cela représente un coût opérationnel important dans toute usine métallurgique.
Ne convient pas à tous les minerais
La calcination est inefficace ou inappropriée pour d'autres grandes classes de minerais.
- Les minerais sulfurés (ex. : Galène, PbS) doivent être grillés (chauffés en excès d'air) pour être convertis en oxydes.
- Les minerais oxydés (ex. : Hématite, Fe₂O₃) sont déjà à l'état oxydé et ne nécessitent pas de décomposition, ils peuvent donc passer directement à la fusion.
Impact environnemental
La décomposition des minerais carbonatés libère de grands volumes de dioxyde de carbone (CO₂), un gaz à effet de serre puissant. C'est une considération environnementale majeure pour les industries qui dépendent de ce processus.
Comment appliquer cela à votre processus
Le choix entre la calcination et d'autres traitements thermiques dépend entièrement de la chimie de départ de votre minerai.
- Si votre objectif principal est un minerai carbonaté (comme ZnCO₃) : La calcination est l'étape initiale essentielle pour le décomposer en son oxyde métallique (ZnO) avant la réduction.
- Si votre objectif principal est un minerai hydraté (comme Al₂O₃·2H₂O) : La calcination est nécessaire pour éliminer l'eau chimiquement liée et produire l'oxyde anhydre (Al₂O₃).
- Si votre objectif principal est un minerai sulfuré (comme PbS) : Le grillage, et non la calcination, est le processus correct pour convertir le sulfure en oxyde par oxydation.
En fin de compte, la calcination est une étape de purification ciblée conçue pour simplifier la chimie du minerai avant le début de l'extraction finale.
Tableau récapitulatif :
| Type de minerai | Composition chimique | Produit de calcination | Objectif |
|---|---|---|---|
| Minerais carbonatés | Carbonates métalliques (ex. : ZnCO₃, FeCO₃) | Oxyde métallique + CO₂ | Décomposer le carbonate, éliminer le CO₂ |
| Minerais hydratés | Oxydes métalliques hydratés (ex. : Al₂O₃·2H₂O) | Oxyde anhydre + H₂O | Éliminer l'eau chimiquement liée |
Besoin d'optimiser votre traitement thermique des minerais carbonatés ou hydratés ? KINTEK est spécialisé dans les fours de laboratoire haute performance et les équipements conçus pour des processus de calcination précis. Nos solutions vous aident à obtenir une décomposition thermique efficace, à améliorer la pureté du minerai et à optimiser votre flux de travail métallurgique global. Contactez nos experts dès aujourd'hui pour discuter de la manière dont nos équipements de laboratoire peuvent répondre à vos besoins spécifiques de traitement des minerais !
Guide Visuel