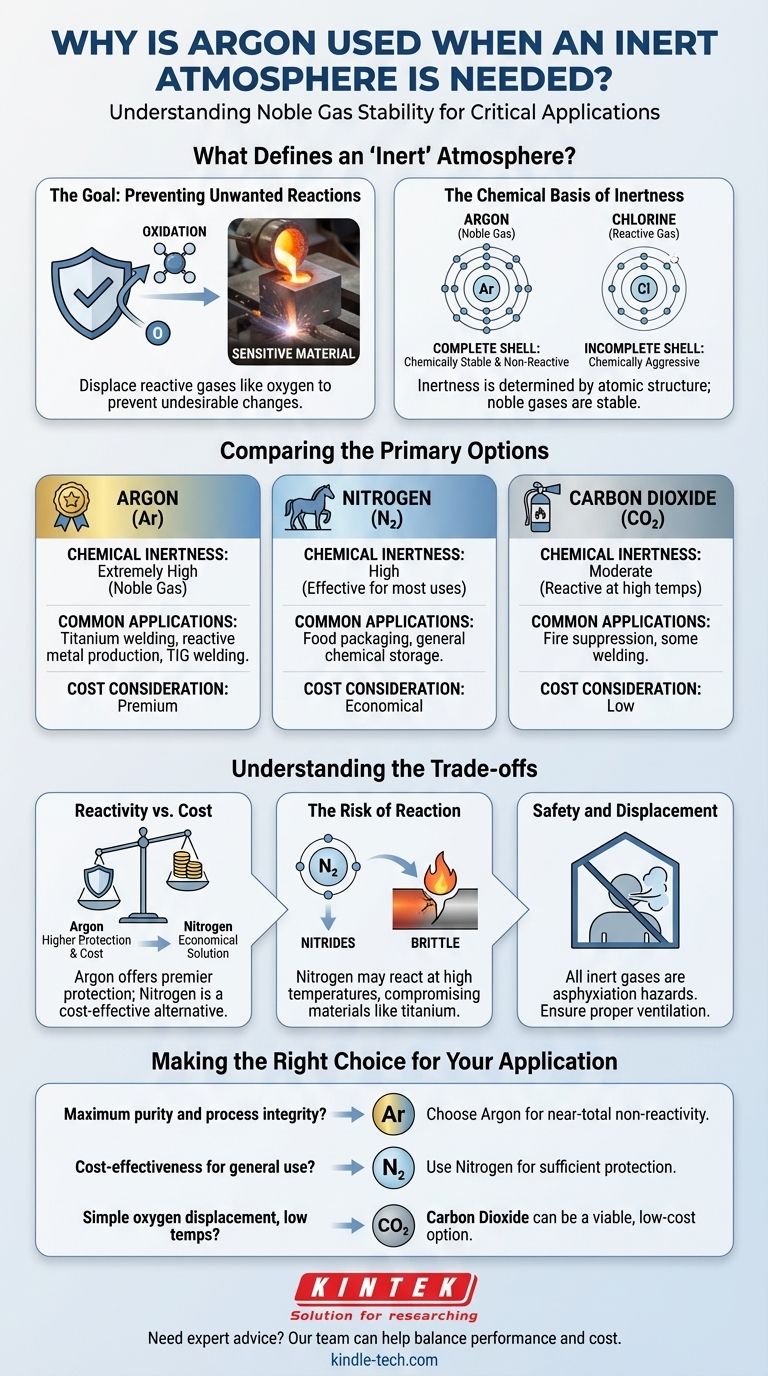
L'argon est utilisé pour les atmosphères inertes car c'est un gaz noble, ce qui le rend presque complètement non réactif dans une vaste gamme de températures et de pressions. Cette stabilité chimique extrême empêche les réactions indésirables comme l'oxydation, en particulier avec des matériaux très sensibles ou en fusion comme le titane ou lors du soudage à haute température.
Bien que l'argon offre une inertie chimique suprême, le choix d'un gaz inerte est une décision stratégique. Il nécessite d'équilibrer le niveau de non-réactivité requis pour votre processus spécifique avec des facteurs pratiques comme le coût, où des gaz comme l'azote offrent souvent une solution plus économique.

Qu'est-ce qui définit une atmosphère "inerte" ?
Le terme "inerte" n'est pas seulement une étiquette ; il décrit une fonction chimique spécifique. Comprendre cette fonction est essentiel pour choisir le bon gaz pour une application technique.
L'objectif : prévenir les réactions indésirables
Le but principal d'une atmosphère inerte est de déplacer les gaz réactifs — le plus souvent l'oxygène — pour prévenir les changements chimiques indésirables.
Pensez à la rouille sur le fer. C'est une oxydation, une réaction lente avec l'oxygène à température ambiante. Aux températures élevées rencontrées lors du soudage ou de la production de métaux, ces réactions oxydatives se produisent presque instantanément et peuvent ruiner le matériau.
Une atmosphère inerte crée une barrière protectrice, enveloppant le matériau sensible et l'empêchant d'entrer en contact avec les éléments réactifs de l'air.
La base chimique de l'inertie
L'inertie d'un gaz est déterminée par sa structure atomique. L'argon est un gaz noble, ce qui signifie que sa couche électronique la plus externe est complètement remplie.
Cela le rend chimiquement stable et "désintéressé" de réagir avec d'autres éléments. Il ne partagera, ne gagnera ni ne perdra facilement des électrons.
En revanche, un gaz très réactif comme le chlore est chimiquement agressif car il veut désespérément gagner un électron pour compléter sa couche externe. C'est pourquoi il est un désinfectant efficace mais totalement inadapté à un processus d'inertage.
Comparaison des principales options
Bien que l'argon soit un excellent choix, ce n'est pas le seul. Les gaz les plus couramment utilisés pour l'inertage sont l'argon, l'azote et, dans une moindre mesure, le dioxyde de carbone.
Argon (Ar) : La référence
L'argon est le premier choix lorsque la non-réactivité absolue est critique. Il reste inerte même dans des conditions extrêmes.
Cela le rend essentiel pour les processus de grande valeur comme la production de titane et d'autres métaux réactifs, ainsi que dans des types spécifiques de soudage à haute température (par exemple, le soudage TIG) où même une contamination minimale peut compromettre l'intégrité structurelle.
Azote (N₂) : Le cheval de bataille
L'azote représente environ 78 % de notre atmosphère et est nettement moins cher à produire sous forme pure que l'argon.
Le gaz azote existe sous forme de deux atomes fortement liés (N₂). Bien que cette liaison puisse être rompue dans des conditions de très haute énergie, elle est suffisamment stable pour être considérée comme effectivement inerte pour une vaste gamme d'applications, de l'emballage alimentaire au stockage chimique général.
Dioxyde de carbone (CO₂) : Un acteur de niche
Le dioxyde de carbone est parfois utilisé pour l'inertage, principalement parce qu'il est peu coûteux et plus dense que l'air, ce qui lui permet de déplacer efficacement l'oxygène par le bas.
Cependant, le CO₂ est plus réactif que l'azote ou l'argon et peut réagir avec certains matériaux, surtout à des températures plus élevées. Son utilisation est généralement limitée à des applications comme la suppression d'incendie ou certaines formes de soudage où sa réactivité n'est pas un problème.
Comprendre les compromis
Le choix d'un gaz inerte est une décision technique qui dépend de l'équilibre entre les exigences du processus et le coût.
Réactivité vs. Coût
C'est le compromis central. L'argon offre le plus haut niveau de protection et de pureté du processus, mais il a un prix élevé.
L'azote offre une solution très efficace et économique pour la majorité des applications industrielles où une inertie absolue n'est pas strictement requise. Les économies de coûts sont souvent substantielles.
Le risque de réaction
L'"inertie" de l'azote n'est pas absolue. Dans certains processus métallurgiques à haute température, l'azote peut réagir avec les métaux pour former des nitrures indésirables, ce qui peut rendre le métal cassant.
C'est une raison essentielle pour laquelle l'argon, malgré son coût, reste non négociable pour le soudage ou le traitement d'alliages sensibles comme le titane, l'aluminium et certains aciers inoxydables.
Sécurité et déplacement
Tous les gaz inertes, y compris l'argon et l'azote, présentent des risques d'asphyxie. Ils sont incolores et inodores et agissent en déplaçant l'oxygène. Dans tout espace clos ou mal ventilé, une accumulation de gaz inerte peut réduire les niveaux d'oxygène à un point dangereux, entraînant une perte de conscience.
Faire le bon choix pour votre application
Votre choix dépend entièrement de la sensibilité chimique de votre processus, des températures impliquées et de votre budget.
- Si votre objectif principal est une pureté maximale et l'intégrité du processus : Choisissez l'argon pour sa non-réactivité quasi totale, en particulier en métallurgie à haute température ou avec des éléments très réactifs.
- Si votre objectif principal est la rentabilité pour l'inertage à usage général : Utilisez l'azote, qui offre une protection suffisante pour une vaste gamme d'applications comme la conservation des aliments et l'inertage chimique.
- Si votre objectif principal est un simple déplacement d'oxygène dans un environnement à basse température et non réactif : Le dioxyde de carbone peut être une option viable et peu coûteuse, à condition qu'il ne réagisse pas avec vos matériaux.
En comprenant ces principes fondamentaux, vous pouvez sélectionner le gaz approprié pour protéger votre processus de manière efficace et efficiente.
Tableau récapitulatif :
| Gaz | Inertie chimique | Applications courantes | Considération de coût |
|---|---|---|---|
| Argon | Extrêmement élevée (gaz noble) | Soudage du titane, production de métaux réactifs | Premium |
| Azote | Élevée (efficace pour la plupart des utilisations) | Emballage alimentaire, stockage chimique général | Économique |
| Dioxyde de carbone | Modérée (réactif à hautes températures) | Suppression d'incendie, certains soudages | Faible |
Besoin de conseils d'experts pour choisir le bon gaz inerte pour vos processus de laboratoire ? Chez KINTEK, nous sommes spécialisés dans la fourniture d'équipements de laboratoire et de consommables de haute pureté, y compris des systèmes de manipulation de gaz adaptés à des applications telles que le soudage, la métallurgie et la synthèse chimique. Notre équipe peut vous aider à équilibrer performance et coût pour protéger efficacement vos matériaux sensibles. Contactez-nous dès aujourd'hui pour optimiser votre installation d'atmosphère inerte !
Guide Visuel