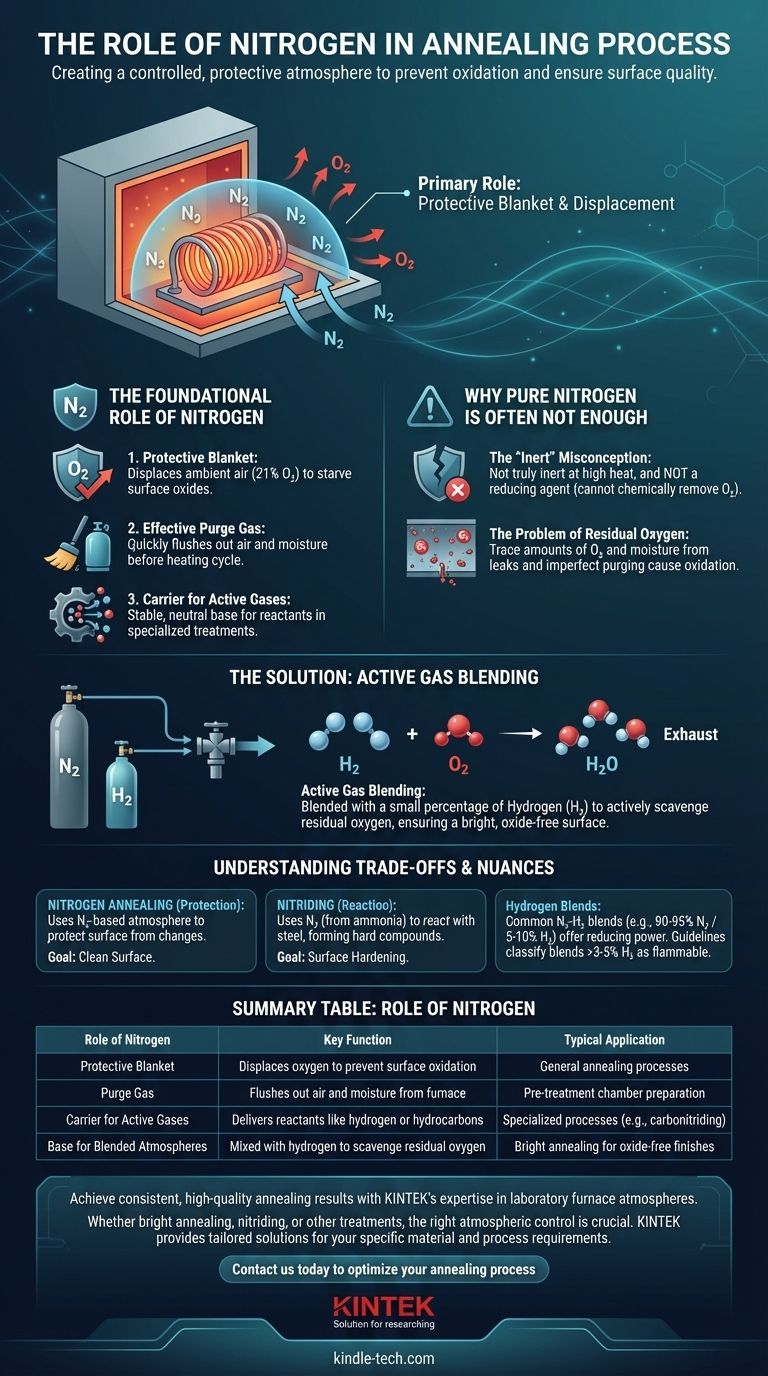
Dans les processus de recuit, le rôle principal de l'azote est de créer une atmosphère contrôlée et protectrice qui déplace l'oxygène, empêchant ainsi l'oxydation, la formation de calamine et la décoloration à la surface du métal. Il sert de « couverture » gazeuse fondamentale et peut également agir comme gaz porteur pour d'autres gaz chimiquement actifs requis pour des traitements thermiques plus spécialisés.
L'azote doit être compris non pas comme un bouclier inerte parfait, mais comme le point de départ essentiel pour le contrôle de l'atmosphère. Parce qu'il ne peut pas éliminer chimiquement l'oxygène résiduel, il est presque toujours mélangé à une petite quantité de gaz actif — généralement de l'hydrogène — pour obtenir un environnement véritablement protecteur et sans oxyde.

Le rôle fondamental de l'azote
L'azote est le gaz de travail pour créer une atmosphère de base dans de nombreuses opérations de traitement thermique. Sa fonction peut être décomposée en trois rôles distincts mais liés.
Un bouclier protecteur
L'objectif le plus fondamental de l'introduction d'azote dans un four de recuit est de déplacer l'air ambiant, qui contient environ 21 % d'oxygène.
En créant un environnement riche en azote, vous privez la surface de la pièce métallique chaude de l'oxygène dont elle a besoin pour former des oxydes (calamine ou ternissure).
Un gaz de purge efficace
Avant le début du cycle de chauffage, la chambre du four doit être purgée de tout air résiduel. L'azote est idéal pour cette tâche.
Son débit élevé peut évacuer rapidement et de manière rentable l'oxygène et l'humidité, préparant le four pour l'atmosphère de traitement souhaitée.
Un porteur pour les gaz actifs
Dans les processus plus complexes comme la carbonitruration ou certains types de brasage, l'azote sert de gaz porteur stable et neutre.
Des quantités spécifiques de gaz actifs, tels que les hydrocarbures (méthane, propane) ou l'ammoniac, sont mélangées au flux d'azote de base. Le rôle de l'azote ici est de délivrer ces réactifs à la surface du métal d'une manière hautement contrôlée et diluée.
Pourquoi l'azote pur n'est souvent pas suffisant
Bien que l'azote soit excellent pour déplacer l'oxygène, il présente une limitation critique qui empêche son utilisation à l'état pur pour un recuit de haute qualité.
L'idée fausse de l'« inerte »
Bien qu'on l'appelle souvent inerte, l'azote n'est pas vraiment inerte, surtout à des températures de recuit élevées. Plus important encore, il n'est pas un agent réducteur.
Cela signifie qu'il peut déplacer l'oxygène, mais il n'a aucune capacité à réagir chimiquement avec et à éliminer tout oxygène qui reste ou pénètre dans le four par de petites fuites.
Le problème de l'oxygène résiduel
Aucun four n'est parfaitement scellé, et la purge n'est jamais efficace à 100 %. Des traces d'oxygène et d'humidité seront toujours présentes.
Lorsque le métal est chauffé, cet oxygène résiduel est plus que suffisant pour provoquer une oxydation de surface, ce qui va à l'encontre de l'objectif d'une atmosphère protectrice pour les applications nécessitant une finition brillante et propre.
La solution : le mélange de gaz actifs
Pour contrecarrer l'oxygène résiduel, l'azote est presque toujours mélangé à un petit pourcentage de gaz réducteur, le plus souvent de l'hydrogène (H₂).
L'hydrogène « piège » activement tout oxygène libre (O₂) en réagissant avec lui pour former de la vapeur d'eau (H₂O), qui est ensuite évacuée du four. Cette action de nettoyage chimique est ce qui garantit une surface véritablement brillante et sans oxyde.
Comprendre les compromis et les nuances
Utiliser l'azote efficacement nécessite de comprendre la distinction entre les différents processus et l'importance d'un contrôle précis.
Recuit à l'azote contre Nitruration
Ces termes sont souvent confondus mais décrivent des processus fondamentalement différents.
Le recuit à l'azote utilise une atmosphère à base d'azote pour protéger le métal contre les changements chimiques tels que l'oxydation. L'objectif est une surface propre.
La nitruration, en revanche, est un processus de durcissement de surface qui utilise l'azote (souvent à partir d'ammoniac dissocié) pour réagir avec l'acier, formant des composés nitrurés durs à la surface.
Le rôle des mélanges d'hydrogène
Les mélanges azote-hydrogène (N₂-H₂) sont courants, mais le pourcentage d'hydrogène est important. Un mélange typique peut être 90-95 % d'azote et 5-10 % d'hydrogène pour un fort pouvoir réducteur.
Cependant, pour des raisons de sécurité, certaines directives classent désormais tout mélange contenant plus de 3 à 5 % d'hydrogène comme inflammable. Les mélanges inférieurs à ce seuil peuvent être considérés comme non inflammables, offrant un moyen plus sûr d'obtenir une élimination de l'oxygène.
Le contrôle est primordial
Le succès de tout processus de recuit dépend d'un contrôle atmosphérique strict. Les débits et les rapports de mélange des gaz sont déterminés par une « recette » prédéfinie spécifique au matériau, à la géométrie de la pièce et au résultat souhaité.
Sans contrôle approprié, l'atmosphère peut ne pas être protectrice ou, dans le cas de mélanges de gaz actifs, peut modifier involontairement la chimie de surface de la pièce.
Faire le bon choix pour votre objectif
Pour sélectionner l'atmosphère correcte, vous devez d'abord définir votre objectif principal pour le processus de traitement thermique.
- Si votre objectif principal est d'empêcher l'oxydation de base sur des pièces non critiques : Une purge à l'azote de haute pureté peut suffire, mais elle comporte un risque de décoloration de surface.
- Si votre objectif principal est d'obtenir une finition brillante et sans oxyde (Recuit brillant) : Un mélange azote-hydrogène (N₂-H₂) est essentiel pour éliminer activement tout oxygène résiduel et assurer une surface propre.
- Si votre objectif principal est de modifier la chimie de surface (par exemple, le durcissement) : Vous avez besoin d'une atmosphère spécialisée où l'azote est un porteur pour les gaz actifs, comme on le voit dans les processus de nitruration ou de carbonitruration.
En fin de compte, comprendre l'azote non pas comme un bouclier parfait mais comme une base contrôlable pour l'atmosphère de votre four est la clé pour obtenir des résultats cohérents et de haute qualité.
Tableau récapitulatif :
| Rôle de l'azote | Fonction clé | Application typique |
|---|---|---|
| Bouclier protecteur | Déplace l'oxygène pour prévenir l'oxydation de surface | Processus de recuit généraux |
| Gaz de purge | Évacue l'air et l'humidité du four | Préparation de la chambre de prétraitement |
| Porteur pour gaz actifs | Délivre des réactifs comme l'hydrogène ou les hydrocarbures | Processus spécialisés (par exemple, carbonitruration) |
| Base pour atmosphères mélangées | Mélangé à de l'hydrogène pour éliminer l'oxygène résiduel | Recuit brillant pour des finitions sans oxyde |
Obtenez des résultats de recuit cohérents et de haute qualité grâce à l'expertise de KINTEK en matière d'atmosphères de fours de laboratoire.
Que vous travailliez sur le recuit brillant, la nitruration ou d'autres traitements thermiques, le contrôle atmosphérique approprié est crucial. KINTEK est spécialisé dans les équipements de laboratoire et les consommables, offrant des solutions adaptées à vos exigences spécifiques en matière de matériaux et de processus.
Contactez-nous dès aujourd'hui pour discuter de la manière dont nous pouvons vous aider à optimiser votre processus de recuit pour une qualité de surface et des performances supérieures.
Guide Visuel
Produits associés
- Four à atmosphère d'hydrogène contrôlée à l'azote
- Four de traitement thermique sous vide avec revêtement en fibre céramique
- Four à moufle haute température pour déliantage et pré-frittage en laboratoire
- Four à moufle de laboratoire à moufle à levage par le bas
- Four de graphitisation de film de haute conductivité thermique sous vide de graphite
Les gens demandent aussi
- Pourquoi un four à atmosphère contrôlée est-il nécessaire pour la préparation de catalyseurs métalliques actifs ?
- Quel est l'usage de l'hydrogène dans un four ? Une clé pour le traitement à haute température sans oxygène
- Quel rôle joue un four à atmosphère contrôlée avec un flux de gaz argon dans la production d'oxyde de graphène réduit (rGO) ?
- L'hydrogène peut-il être utilisé dans les fours ? Oui, pour le traitement des métaux sans oxydation et le chauffage rapide
- Quel est le rôle d'un four à atmosphère d'hydrogène dans le post-traitement des composites diamant/cuivre après dépôt de cuivre chimique?



















